| Информационная система |  |
Государственное
санитарно-эпидемиологическое нормирование
Российской Федерации
2.1.10. ГИГИЕНА. КОММУНАЛЬНАЯ ГИГИЕНА.
СОСТОЯНИЕ ЗДОРОВЬЯ НАСЕЛЕНИЯ В СВЯЗИ
С СОСТОЯНИЕМ ОКРУЖАЮЩЕЙ ПРИРОДНОЙ СРЕДЫ И
УСЛОВИЯМИ ПРОЖИВАНИЯ НАСЕЛЕНИЯ
Применение показателей и критериев
нарушения биотрансформации бензола
в организме детей для задач
гигиенических оценок,
санитарно-эпидемиологических
расследований и экспертиз
Методические рекомендации
MP 2.1.10.0077-13
1. Разработаны Федеральным бюджетным учреждением науки «Федеральный научный центр медико-профилактических технологий управления рисками здоровью населения» (Н.В. Зайцева, М.А. Землянова, Ю.В. Кольдибекова, Т.С. Уланова, О.В. Долгих, Д.А. Кирьянов, В.М. Чигвинцев, В.Н. Звездин).
2. Утверждены руководителем Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, Главным государственным санитарным врачом Российской Федерации Г.Г. Онищенко 20 августа 2013 г.
СОДЕРЖАНИЕ
|
УТВЕРЖДАЮ Руководитель Федеральной службы Г.Г. Онищенко 20 августа 2013 г. Дата введения: с момента утверждения |
2.1.10. ГИГИЕНА. КОММУНАЛЬНАЯ ГИГИЕНА.
СОСТОЯНИЕ ЗДОРОВЬЯ НАСЕЛЕНИЯ В СВЯЗИ
С СОСТОЯНИЕМ ОКРУЖАЮЩЕЙ ПРИРОДНОЙ СРЕДЫ И
УСЛОВИЯМИ ПРОЖИВАНИЯ НАСЕЛЕНИЯ
Применение показателей и критериев
нарушения
биотрансформации бензола в организме детей
для задач гигиенических оценок, санитарно-
эпидемиологических расследований и экспертиз
Методические
рекомендации
MP 2.1.10.0077-13
1. Общие положения
1.1. Настоящие методические рекомендации разработаны для повышения эффективности гигиенических оценок, санитарно-эпидемиологических расследований и экспертиз по выявлению нарушений состояния здоровья в связи с воздействием химических факторов. В настоящих методических рекомендациях определены показатели и критерии нарушения биотрансформации бензола в организме детей при хроническом внешнесредовом аэротехногенном воздействии.
1.2. Проведение исследований осуществляется по запросу органов и организаций Роспотребнадзора научно-исследовательскими организациями, а также иными научно-исследовательскими или лечебно-профилактическими учреждениями, привлекаемыми в соответствии с п. 6.4 постановления Правительства Российской Федерации от 30.06.2004 № 322 «Об утверждении Положения о Федеральной службе по надзору в сфере защиты прав потребителей и благополучия человека», аккредитованными в установленном порядке для проведения работ по оценке риска для здоровья населения, исследований биологических объектов, материалов и сред, а также имеющих лицензию на осуществление медицинской деятельности.
1.3. Все исследования осуществляются в строгом соответствии с требованиями действующих нормативных правовых и методических документов.
1.4. Планирование и проведение исследований осуществляется с обязательным соблюдением принципов надлежащей лабораторной практики Principles of Good Laboratory Practice (ENV/MC/CHEM (98)17) в соответствии с Национальным стандартом Российской Федерации ГОСТ Р 53434-09 «Принципы надлежащей лабораторной практики».
1.5. В настоящих рекомендациях использованы результаты исследования и оценки нарушений биотрансформации бензола и его метаболита - фенола в организме детей, связанных с хроническим внешнесредовым аэротехногенным воздействием бензола и отсутствием, аэрогенного поступления фенола, и сравнительно с результатами исследований у детей, проживающих в условиях отсутствия аэрогенного воздействия данных химических соединений.
2. Область применения
2.1. Методические рекомендации предназначены для органов и организаций Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека при проведении санитарно-гигиенических экспертиз, расследований, исследований в области гигиенической оценки по установлению причинно-следственных связей между факторами среды обитания и здоровьем населения субъектов Российской Федерации.
Рекомендации также могут быть использованы научно-исследовательскими, лечебно-профилактическими и другими организациями, занимающимися вопросами гигиенической оценки, предотвращения и снижения неблагоприятных последствий воздействия факторов среды обитания на здоровье человека.
3. Основная часть
3.1. Термины и определения
Биотрансформация - энзиматическое превращение жирорастворимых экзогенных или эндогенных соединений в полярные водорастворимые метаболиты, легко выводимые из организма.
Конъюгация - реакция синтеза чужеродного вещества с эндогенными молекулами или их группировками (аминокислоты, глюкуроновая или серная кислоты и др.), в результате чего образуются конъюгаты - более полярные, гидрофильные соединения, легко выводимые го организма.
Элиминация - удаление чужеродного вещества го организма, состоящее из двух процессов: нейтрализации путем биотрансформации и собственно экскреции.
Глутатионовая система - многокомпонентная система, включающая в себя комплекс ферментов (глутатионпероксидаза, глутатионредуктаза, глутатион-6-трансфераза, глюкозо-6-фосфатдегидрогеназа), осуществляющих конъюгационно-элиминационную функцию соединений во II фазе биотрансформации веществ.
Глутатионпероксидаза - фермент, защищающий от окислительного повреждения восстановительный глутатион, участие которого необходимо в эндогенном связывании чужеродного вещества.
Глутатионредуктаза - фермент, катализирующий реакцию восстановления глутатиона из его окисленной формы.
Глюкозо-6-фосфатдегидрогеназа - фермент, обеспечивающий образование клеточного НАДФ-Н, необходимого для поддержания восстановленного глутатиона.
Глутатион-S-трансфераза - фермент, катализирующий присоединение глутатиона к эндогенному или чужеродному соединению.
3.2. Перечень сокращений
Гл-6-Ф - глюкозо-6-фосфатдегидрогеназа
ГлSТр - гутатион-S-трансфераза
ГлПО – глутатионпероксидаза
ГлР – глутатионредуктаза
ИФА - иммуноферментный анализ
НАДФ-Н - никотинамиддинуклеотидфосфат восстановленный
Rfcchi - референтная концентрация для хронического ингаляционного воздействия
3.3. Введение
На промышленно развитых территориях с размещением предприятий органического синтеза, химической, нефтеперерабатывающей, нефтехимической отраслей и развитой транспортной инфраструктурой к одним из приоритетных и распространенных загрязнителей атмосферного воздуха относится бензол, являющийся истинным ксенобиотиком и высоко опасным химическим веществом для здоровья человека [1].
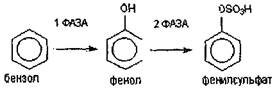
При ингаляционном поступлении в организм большая часть бензола (до 84 %) подвергается биотрансформации, которая осуществляется в основном в печени [2]. В процессе биотрансформации происходит окисление бензола через промежуточный метаболит - фенол, с образованием конечного продукта - фенилсульфата [3, 4]. Схематическое изображение биотрансформации бензола представлено на рис. 1 [4].
Рис. 1. Биотрансформация бензола
Биотрансформацию бензола и его метаболита фенола в организме осуществляет система цитохромов Р-450 и глутатионовая система [5]. В первой фазе биотрансформации система цитохромов Р-450 обеспечивает переход бензола в полярное и гидрофильное относительно исходного соединение - фенол, что обусловливает возможность его быстрой экскреции из организма. Во вторую фазу биотрансформации глутатионовая система обеспечивает конъюгацию фенола с эндогенным глутатионом, в результате чего образуется конечный метаболит - фенилсульфат, который в дальнейшем легко подвергается элиминации из организма. При этом фенол, по сравнению с фенилсульфатом, представляет большую опасность для здоровья человека [6].
Хроническое внешнесредовое аэротехногенное воздействие бензола может обусловливать наличие бензола и увеличение концентрации его метаболита - фенола в биосредах (кровь, моча) в результате нарушения процесса биотрансформации. Это может являться следствием дисфункции систем, обеспечивающих процесс биотрансформации бензола. Наличие бензола и повышенное содержание фенола в биосредах может обусловить развитие заболеваний крови и кроветворных органов, центральной нервной, иммунной, сердечно-сосудистой систем, печени, почек [3].
Выявление и оценка нарушений биотрансформации бензола в организме при хроническом ингаляционном поступлении в организм включает поэтапное выполнение следующих процедур:
1) исследование и оценку содержания бензола и фенола в крови и моче. Количественное определение бензола в крови и моче осуществляется газохроматографическим методом в соответствии с методическими рекомендациями, действующими в Российской Федерации (МУК 4.1.764-99 и 4.1.765-99). Определение массовой концентрации фенола в крови и моче осуществляется газохроматографическим методом в соответствии с методическими рекомендациями, действующими в Российской Федерации (МУК 4.1.2107-06 и 4.1.2108-06);
2) исследование и оценку состояния функций систем, обеспечивающих первую и вторую фазы биотрансформации бензола, по комплексу показателей:
а) состояние системы цитохрома Р-450 (гена CYP1A1), участвующего в первой фазе биотрансформации.
Методика основана на принципе полимеразной цепной реакции, в основе которой лежит амплификация и детекция продуктов этой реакции в режиме реального времени с помощью флюоресцентных меток, которыми предварительно помечают используемые для реакции амплификации праймеры в соответствии с инструкцией к тест-системе;
б) активность ферментов глутатионовой системы, участвующей во второй фазе биотрансформации:
- активность глутатионпероксидазы - фермента, защищающего от окислительного повреждения восстановленный глутатион, необходимый в эндогенном связывании фенола. Активность глутатионпероксидазы в сыворотке крови определяется фотометрическим методом, основанным на принципе «сэндвич» иммуноферментного анализа в соответствии с инструкцией к тест-системе ИФА;
- активность глутатионредуктазы - фермента, катализирующего реакцию восстановления глутатиона из его окисленной формы. Активность глутатионредуктазы определяется кинетическим методом по принципу каталитического восстановления глутатиона в присутствии восстановленного НАДФ-Н по степени уменьшения абсорбции этого процесса в соответствии с инструкцией к тест-системе биохимического анализа;
- активность глюкозо-6-фосфатдегидрогеназы - фермента, обеспечивающего образование клеточного НАДФ-Н, необходимого для поддержания восстановленного глутатиона для эндогенного связывания фенола. Активность глюкозо-6-фосфатдегидрогеназы определяется кинетическим методом по степени увеличения абсорбции в результате превращения НАДФ+ в соответствии с инструкцией к тест-системе биохимического анализа;
- активность глутатион-S-трансферазы - фермента, катализирующего присоединение глутатиона к эндогенно образованному фенолу. Активность глутатион-S-трансферазы в сыворотке крови определяется фотометрическим методом, основанным на принципе твердофазного иммуноферментного анализа в соответствии с инструкцией к тест-системе ИФА.
Требования и перечень необходимого оборудования, расходных материалов, реактивов и тест-систем для выполнения исследований представлены в прилож. 2, 3.
3.4. Специальная часть
3.4.1. Нарушение биотрансформации бензола возникает:
· при наличии патологического аллеля цитохрома Р-450, что свидетельствует о наследственной предрасположенности к нарушению процесса биотрансформации;
· при дисфункции ферментов глутатионовой системы, обеспечивающих связывание и выведение бензола и его метаболита - фенола из организма, обусловленной ингаляционным поступлением бензола в концентрациях, превышающих референтные уровни хронического ингаляционного воздействия (Rfcchr) (Р 2.1.10.1920-04).
3.4.2. Показателями нарушения биотрансформации бензола в организме является наличие бензола и повышенных концентраций фенола (как метаболита бензола) в крови и моче.
3.4.3. Гигиеническими критериями для проведения химико-аналитического исследования биосред у детей на содержание бензола и фенола являются:
· наличие бензола в атмосферном воздухе селитебной застройки выше предельно допустимой концентрации (более 1 ПДКсс - 0,1 мг/м3) и референтной концентрации при ингаляционном поступлении (более 1 Rfcchr - 0,03 мг/м3);
· отсутствие фенола в атмосферном воздухе селитебной зоны для исключения его экзогенного поступления в организм.
3.4.4. Критериями нарушения биотрансформации бензола являются следующие показатели:
· идентификация бензола в крови и моче выше предела обнаружения (0,0035 мг/дм3);
· наличие фенола в крови и моче выше фоновых уровней (в крови - (0,010 ± 0,005) мг/дм3, моче - (0,278 ± 0,021) мг/дм3) в 1,2 раза;
· распространенность минорного аллеля по гену цитохрома Р-450 CYP1A1 выше 10 %;
· повышение активности глутатионпероксидазы в сыворотке крови в 1,2 - 1,4 раза относительно контроля и границы чувствительности метода (> 54,7 нг/см3);
· повышение активности глутатионредуктазы в сыворотке крови в 1,6 - 1,8 раза относительно контроля и границы чувствительности метода (> 80 Е/дм3);
· повышение активности глюкозо-6-фосфатдегидрогеназы в сыворотке крови в 1,2 - 1,3 раза относительно контроля и границы чувствительности метода (> 4,1 Е/дм3);
· понижение активности глутатион-8-трансферазы в сыворотке крови в 2,5 - 2,6 раза относительно контроля и границы чувствительности метода. (< 110 нг/см3).
3.4.5. При наличии нарушения связывания и выведения бензола и фенола из организма необходимо контролировать развитие нарушений у детей со стороны:
· крови и кроветворных органов (нарушение процессов костно-мозгового кроветворения - анемия неуточненная - D64.9, апластическая анемия, вызванная внешними агентами - D61.2);
· центральной нервной системы и сердечно-сосудистой системы (функциональные расстройства нервной системы - астеноневротический синдром - R45.0, астеновегетативные нарушения и другие расстройства вегетативной нервной системы - G90.8);
· иммунной системы (супрессия процессов иммунной защиты и неспецифической резистентности - вторичное иммунодефицитное состояние - D83.9).
Реализация предложенной методики исследования представлена в прилож. 4.
Нормативные правовые и методические документы
· Федеральный закон от 30.03.1999 № 52-ФЗ «О санитарно-эпидемиологическом благополучии населения».
· Постановление Правительства Российской Федерации от 30.06.2004 № 322 (с изменениями) «Об утверждении Положения о Федеральной службе по надзору в сфере защиты прав потребителей и благополучия человека».
· Приказ Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека от 19.07.2007 № 224 «О санитарно-эпидемиологических экспертизах, обследованиях, исследованиях, испытаниях и токсикологических, гигиенических и иных видах оценок».
· ГОСТ 8.207-76 «Государственная система обеспечения единства измерений. Прямые измерения с многократными наблюдениями. Методы обработки результатов наблюдений. Основные положения».
· МУК 4.1.765-99 «Газохроматографический метод количественного определения ароматических (бензол, толуол, этилбензол, о-, м-, п-ксилол) углеводородов в биосредах (кровь)».
· МУК 4.1.764-99 «Газохроматографический метод количественного определения предельных (гексан, гептан) и ароматических (бензол, толуол, этилбензол, о-, м-, п-ксилол) углеводородов в биосредах (моча)».
· МУК 4.1.2108-06 «Определение массовой концентрации фенола в биосредах (кровь) газохроматографическим методом».
· МУК 4.1.2107-06 «Определение массовой концентрации фенола в биосредах (моча) газохроматографическим методом».
· Р 2.1.10.1920-04 «Руководство по оценке риска здоровью населения при воздействии химических веществ».
Библиографические данные
2. Вредные вещества в промышленности: Справочник в 3 томах. Том I. Органические вещества /Под ред. Н.В. Лазарева, Э.Н. Левиной. Л.: Химия, 1976. 592 с.
3. Токсикологическая химия. Аналитическая токсикология: Учебник /Под ред. Р.У. Хабриева, Н.И. Калетиной. М.: ГОЭТАР - Медиа, 2010. 752 с.
4. Онищенко Г.Г. Гигиеническая индикация последствий для здоровья при внешнесредовой экспозиции химических факторов /Г.Г. Онищенко, Н.В. Зайцева, М.А. Землянова; под ред. Г.Г. Онищенко. Пермь: Книжный формат, 2011. С. 126 - 130.
5. Землянова М.А., Кольдибекова Ю.В. Современные подходы к оценке нарушений метаболизма ксенобиотиков при поступлении в организм из внешней среды //Экология человека. 2012. № 8. С. 8 - 14.
6. Зайцева Н.В. Гигиеническая диагностика нарушений метаболизма ароматических углеводородов для эпидемиологических исследований влияния внешнесредовых факторов /Н.В. Зайцева, М.А. Землянова, В.Н. Звездин, Е.Р. Комлева, Д.А. Кирьянов, Т.С. Уланова, В.М. Чигвинцев. М.: ВНТИЦ, № гос. рег. 02201150764.
Приложение 1
(справочное)
Перечень средств измерений, вспомогательных устройств и реактивов, необходимых для количественного определения бензола и фенола в биосредах (кровь, моча) газохроматографическим методом
При выполнении исследований применяют следующие средства измерений, вспомогательные устройства, материалы и реактивы. Допускается применение других типов средств измерений, вспомогательного оборудования и химреактивов с аналогичными метрологическими характеристиками.
1. Перечень средств измерений
|
Хроматограф газовый с пламенно-ионизационным детектором |
|
|
Весы лабораторные аналитические |
ГОСТ 24104-80Е |
|
Секундомер |
2. Вспомогательные устройства
|
Хроматографическая колонка стальная длиной 3 м и внутренним диаметром 3 мм |
|
|
Бидистиллятор |
|
|
Редуктор кислородный |
ТУ 26-05-235-70 |
|
Микрошприцы |
ТУ 5Е2.833.106 |
|
Шприцы медицинские стеклянные вместимостью 5 см3 |
ТУ 64-1-378-83 |
|
Колбы мерные вместимостью 1000 см3 |
|
|
Пипетки вместимостью 1, 5, 10 см3 |
ГОСТ 20292-74 |
|
Пробирки с притертыми пробками вместимостью 10 см3 |
3. Вспомогательные материалы и реактивы
Приложение 2
(справочное)
Требования и перечень оборудования, необходимого для реализации исследования и оценки состояния цитохрома Р-450 и глутатионовой системы
1. Оборудование должно иметь государственный сертификат соответствия техническому регламенту, свидетельство о прохождении метрологического контроля аккредитованными для этого организациями в установленном порядке и в установленные сроки.
2. Для каждого прибора, используемого в исследованиях, в журнале фиксируются следующие сведения: наименование прибора, наименование производителя, страна-изготовитель, модель прибора, серийный (заводской) номер, дата приобретения и постановки на учет в лаборатории, дата запуска в эксплуатацию, инвентарный номер, дата и номер свидетельства метрологического контроля на момент исследования, место расположения прибора.
3. Эксплуатация оборудования проводится в соответствии с техническим паспортом и руководством пользователя. Выполнение исследований проводят при нормальных климатических условиях в соответствии с ГОСТ 15150: температура воздуха (20 ± 1) °С; атмосферное давление 630 - 800 мм рт.ст.; влажность воздуха не более 80 % при температуре 25 °С. Результаты проведения калибровки, поверки и текущего ремонта оборудования фиксируются в специальном журнале, датируются и заверяются подписью сотрудника, эксплуатирующего оборудование. Журнал должен быть доступен для сотрудников, обеспечивающих его обслуживание.
Весы лабораторные 2-го класса точности (максимальная нагрузка до 200 г, основная погрешность при измерении не более 0,2 мг) для взвешивания сухих ингредиентов при подготовке рабочих растворов
Ионометр (рН-метр) для определения рН буферных растворов
6. Вспомогательные материалы и лабораторная посуда
|
Бидистиллятор |
|
|
Редуктор кислородный |
ТУ 26-05-235-70 |
|
Регулируемые автоматические дозаторы 1-канальные (10 - 100, 100 - 1000, 500 - 5000 мкл), погрешность ±1 мкл |
|
|
Регулируемые автоматические дозаторы 8-канальные (5 - 50, 50 - 300 мкл) погрешность ±1 мкл |
|
|
Стаканы стеклянные химические объемом 50, 500 см3 |
ГОСТ 10394-72 |
|
Лабораторные штативы |
ТУ 64-1-2669-73 |
|
Наконечники пластиковые для автоматических дозаторов объемом 10 - 300 мкл, 200 - 1000 мкл, 1000 - 5000 мкл |
|
|
Перчатки резиновые |
|
|
Пробирки вакуумные пластиковые Improve без коагулянта объемом 9 см3 |
|
|
Зонд урогенитальный, одноразовый, стерильный |
|
|
Транспортная среда для хранения и транспортирования респираторных мазков |
|
|
Пробирки |
ГОСТ 10515-75 |
Приложение 3
(справочное)
Требования и перечень используемых реактивов и тест-систем, необходимых для исследования и оценки состояния цитохрома Р-450 и глутатионовой системы
1. Реактивы и тест-системы, используемые в исследованиях, должны иметь государственный сертификат соответствия. Характеристики реактивов и тест-систем должны быть паспортизированы и иметь документированный сертификат гарантированного срока использования. Условия проведения исследований на тест-системах должны выполняться строго по инструкции производителя или специально разработанным стандартным операционным процедурам и исключать воздействие внешних факторов, способных повлиять на качество выполнения исследований.
2. Реактивы и тест системы
|
Вода бидистиллированная |
|
|
Магния хлорид, х.ч. |
|
|
Натрия хлорид, х.ч. |
|
|
Натрия додецилсульфат |
|
|
Спирт этиловый (ректификат) |
|
|
Спирт изоамиловый |
|
|
Натрия гидроокись |
|
|
Двуокись кремния с размером частиц 0,5 - 10,0 микрон |
|
|
Фенол |
|
|
Хлороформ |
ГОСТ 1248-72 |
|
тРНК |
|
|
Трис-(оксиметил)-аминометан |
ТУ 6-09-4292-76 |
|
Тест-система для проведния полимеразной цепной реакции с гибридизационно-флуорисцентной детекцией в режиме реального времени или аналогичная |
|
|
Тест-система ИФА для определения активности глутатион-S-трансферазы |
|
|
Тест-система ИФА для определения активности глутатионпероксидазы |
|
|
Тест-система биохимического анализа для определения активности глутатионредуктазы |
|
|
Тест-система биохимического анализа для определения активности глюкозо-6-фосфатдегидрогеназы |
Приложение 4
(справочное)
Пример апробации методики исследования показателей нарушения биотрансформации бензола в организме детей, проживающих в условиях хронического внешнесредового воздействия бензола
Результаты апробации предложенной методики показали: содержание бензола в атмосферном воздухе селитебной зоны по данным мониторинговых и натурных наблюдений в 2009 - 2010 гг. зафиксировано на уровне до 1,2 ПДКсс или 4 RfCchr.; отсутствие фенола в атмосферном воздухе, что исключает его экзогенное ингаляционное поступление в организм.
В результате химико-аналитического обследования детей, проживающих в условиях хронического внешнесредового воздействия бензола и отсутствия аэрогенного поступления фенола (группа наблюдения, п = 188), установлено, что у детей группы наблюдения, по сравнению с детьми, проживающими вне зоны аэрогенного воздействия исследуемых химических веществ (контрольная группа, п = 93), в крови регистрируется бензол в 55 % случаев от числа обследованных детей, в моче - в 64 % случаев (табл. 1).
Таблица 1
Содержание бензола и фенола в биосредах детей, мг/дм3
|
Биосреда |
Группа наблюдения |
Контрольная группа |
Достоверность различий (р ≤ 0,05) |
|
|
Бензол |
кровь |
0,0182 ± 0,0025 |
нпо* |
0,000 |
|
Фенол |
0,118 ± 0,031 |
0,011 ± 0,008 |
0,004 |
|
|
Бензол |
моча |
0,0105 ±0,0046 |
нпо* |
0,000 |
|
Фенол |
0,291 ±0,097 |
0,208 ± 0,069 |
0,000 |
|
|
нпо* - ниже предела обнаружения: нпо бензола - 0,0035 мг/дм3. При идентификации вещества в крови детей группы наблюдения ниже предела обнаружения в расчете средней концентрации использована 1/2 предела обнаружения |
||||
Кроме этого, у 70 % детей группы наблюдения в крови установлена повышенная концентрация фенола, превышающая данный показатель у детей в группе сравнения в 10 раз. У 26 % детей группы наблюдения установлено повышенное содержание фенола в моче. При этом средняя концентрация данного соединения достоверно превысила в 1,4 раза аналогичный показатель у детей в группе сравнения.
При выполнении исследования состояния гена цитохрома Р-450, обеспечивающего первую фазу биотрансформации бензола, подсчитывали процент гомозигот и гетерозигот. Анализ полученных данных выявил наличие патологической гомозиготы у 4 % детей исследуемой группы при отсутствии таковой в контроле. При этом распространенность минорного аллеля у детей группы наблюдения превышала его частоту в контроле (10 и 6 % соответственно). Распределение частот генов цитохрома Р-450 CYP1A1 у детей представлены в табл. 2.
Таблица 2
Распределение частот генов цитохрома Р-450 CYP1A1 у детей
|
Генотип |
Группа наблюдения, % |
Контрольная группа, % |
|
|
Ген цитохорма Р-450 CYP1A1 |
А/А* |
4 (3) |
0(0) |
|
A/G** |
17 (32) |
23 (21) |
|
|
G/G*** |
81 (153) |
77 (72) |
|
|
G*** |
90 |
89 |
|
|
А***** |
10 |
6 |
|
|
______________ * Патологическая гомозигота. ** Гетерозигота. *** Нормальная гомозигота. *** Нормальный аллель. ***** Патологический аллель (минорный, мутантный) |
|||
При исследовании и оценке показателей глутатионовой системы, обеспечивающих вторую фазу биотрансформации бензола, анализировали средние значения активности ферментов и частоты регистрации выявленных отклонений показателей в группе наблюдения и контрольной группе. Результаты исследований представлены в табл. 3.
Таблица 3
Сравнительный анализ показателей функций глутатионовой системы у детей
|
Группа наблюдения |
Контрольная группа |
Достоверность различий по средним значениям показателей (Р ≤ 0,05) |
|||||
|
среднее значение в группе (М ± т) |
частота регистрации проб с отклонением от физиологической нормы, % |
среднее значение в группе (М ± т) |
частота регистрации проб с отклонением от физиологической нормы, % |
||||
|
ниже |
выше |
ниже |
выше |
||||
|
ГлПО, нг/см3 |
40,84 ± 4,15 |
21,7 |
17,4 |
30,64 ± 1,21 |
18,9 |
4,9 |
0,000 |
|
ГлР, Е/дм3 |
80,55 ± 3,09 |
1,61 |
35,48 |
47,58 ± 3,42 |
0,0 |
48,28 |
0,000 |
|
Гл-6-Ф, Едм3 |
3,18 ± 0,37 |
1,43 |
60,0 |
2,89 ± 0,43 |
18,2 |
9,1 |
0,308 |
|
ГлSTp, нг/см3 |
79,04 ± 15,86 |
23,1 |
19,2 |
200,11 ± 35,8 |
25,4 |
5,08 |
0,000 |
При выполнении исследования анализируются средние значения активности ферментов и частота регистрации выявленных отклонений показателей в группе наблюдения и контрольной группе.
У детей группы наблюдения среднее значение активности глутатионпероксидазы (40,84 ± 4,15) нг/см3 в сыворотке крови достоверно превысило в 1,3 раза значение данного показателя у детей в контроле. При этом частота регистрации проб с повышенной активностью глутатионпероксидазы (17 % случаев от общего количества обследованных детей) в 4 раза превысила показатель в контрольной группе, что свидетельствует о реализации функции глутатионпероксидазы - защита глутатиона от окислительного повреждения бензолом.
Средняя активность глутатионредуктазы в сыворотке крови детей группы наблюдения составила (80,55 ± 3,09) Е/дм3, что в 1,7 раза выше данного показателя у детей контрольной группы. Доля проб с повышенной активностью глутатионредуктазы у детей группы наблюдения составила 35 % от общего количества обследованных, что достоверно в 1,4 раза ниже частоты регистрации повышенной активности данного фермента у детей контрольной группы (р = 0,000). Зарегистрирована повышенная активность глюкозо-6-фосфатдегидрогеназы в сыворотке крови детей группы наблюдения в 60 % случаев, что в 7 раз выше данного показателя в контрольной группе.
Отмечается дисфункция глутатион-S-трансферазы в виде снижения ее активности у детей группы наблюдения (79.04 ± 15,86) нг/см3 в 2,5 раза относительно аналогичного показателя у детей контрольной группы, что свидетельствует о низкой конъюгации глутатиона с промежуточным метаболитом бензола - фенолом.
Полученные результаты свидетельствуют о сохранении функции ферментов глутатионовой системы, обеспечивающих восстановление глутатиона для дальнейшего связывания его с фенолом, и нарушении процесса конъюгации и выведения фенола из организма, что может привести к его накоплению в биосредах.
Учитывая выявленную дисфункцию глутатион-S-трансферазы для подтверждения нарушения процесса биотрансформации бензола, необходимо в дальнейшем оценивать состояние гена данного фермента - GSTP1 (A313G, C341G), ответственного за вторую фазу детоксикации бензола. То есть, для определения степени распространенности наследственно-обусловленных генетических изменений у лиц, подвергающихся хроническому внешнесредовому аэротехногенному воздействию бензола (для последующего исключения их из исследований), необходимо оценивать состояние гена цитохрома Р-450 CYP1A1 (T6235C-9893A/G), ответственного за первую фазу детоксикации, и гена GSTP1 (A313G, C341G), ответственного за вторую фазу детоксикации.
Накопление бензола и фенола в крови и моче может привести к развитию неинфекционных соматических заболеваний критических органов и систем. Выполненная оценка заболеваемости обследованных детей группы наблюдения показала, что частота регистрации анемии (23 % случаев от общего числа обследованных) и астеноневротического синдрома (19 %) превышает в 1,3 и 1,7 раза соответственно встречаемость аналогичных заболеваний у детей контрольной группы (16 и 10 % соответственно). Достоверно установлена причинно-следственная связь между содержанием бензола в атмосферном воздухе и уровнем заболеваемости детей анемией (OR = 1,3; DI = 1,11 - 3,38), астеноневротическим синдромом (OR = 2,40; DI = 1,80 - 4,23).
Полученные результаты свидетельствуют о нарушении процесса биотрансформации бензола в организме детей, проживающих в условиях внешнесредового аэрогенного воздействия.