 | Информационная система |  |
Федеральная
служба по надзору в сфере защиты прав потребителей
и благополучия человека
Сборник
методических документов, необходимых
для обеспечения применения
Федерального закона от 12 июня 2008 г. № 88-ФЗ
«Технический регламент на молоко
и молочную продукцию»
Часть 5
В сборник включены методические документы, содержащие правила и методы исследований (испытаний) и измерений, а также правила отбора образцов для проведения исследований (испытаний) и измерений, в соответствии с постановлением Главного государственного санитарного врача Российской Федерации Г.Г. Онищенко от 08.12.2008 № 67.
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение остаточных количеств
ивермектина в печени, почках, мясе, жире
сельскохозяйственных животных и молоке
методом высокоэффективной
жидкостной хроматографии
Методические
указания
МУК 4.1.1821-03
1. Подготовлены: Федеральным научным центром гигиены им. Ф.Ф. Эрисмана (проф. Юдина Т.В.), Московской сельскохозяйственной академией им. К.А. Тимирязева (проф. Калинин В.А.), при участии Департамента Госсанэпиднадзора Минздрава России (гл. специалист Веселов А.П.).
2. Методические указания рекомендованы к утверждению Комиссией по государственному санитарно-эпидемиологическому нормированию при Минздраве России (прот. № 20 от 2 декабря 2003 г.).
3. Утверждены Главным государственным санитарным врачом Российской Федерации, Первым заместителем Министра здравоохранения Российской Федерации, академиком РАМН Г.Г. Онищенко 18 декабря 2003 г.
|
|
УТВЕРЖДАЮ Главный
государственный санитарный Г.Г. Онищенко 18 декабря 2003 г. Дата введения: 1 апреля 2004 г. |
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение
остаточных количеств
ивермектина в печени, почках, мясе, жире
сельскохозяйственных животных и молоке методом
высокоэффективной жидкостной хроматографии
Методические указания
МУК 4.1.1821-03
Вводная часть
Настоящие методические указания устанавливают метод высокоэффективной жидкостной хроматографии для определения в печени, почках, мясе, жире сельскохозяйственных животных и молоке массовой концентрации ивермектина в диапазонах 0,001 - 0,02 мг/кг (печень, почки, мясо, молоко); 0,002 - 0,04 мг/кг (жир).
Ивермектин - действующее вещество ветеринарных препаратов:
ЦЕВАМЕК 1 % ИР, фирма-производитель «CEVA Sante Animate»;
ГАНАМЕКТИН, фирма-производитель «Invesa»;
ИВОМЕК 1 % ИР, ИВОМЕК Плюс ИР, фирма-производитель «Мериал».
Ивермектин - смесь компонентов Н2В1а и Н2В1. Содержание компонента Н2В1а и не менее 90 %.
Компонент H2B1a - (2аЕ, 4Е, 8Е) - (5'S, 6S, 'R, 7S, 11R, 13R, 15S, 17aR, 20R, 20aR, 20bS) - 20, 20b - дигидрокси - 5', 6, 8, 19 - тетраметил - 7 - [[(3-О-метил - 4-0 - (3-О-метил - 2, 6 - дидеокси-α-L-арабино-гексапиранозил) - 2, 6 - дидеокси - α-L-арабино-гексапиранозил] - окси] - 6' - [(1S) - I-метилпропил] - 3', 4', 5', 6, 6', 7, 10, 11, 14, 15, 17а, 20, 20a-, 20b - тетрадека - гидроспиро [11, 15 - метано - 2Н, 13Н, 17Н - фуро [4, 3, 2pq] [2, 6] бензодиоксациклооктадецен - 13, 2' - [2Н] пиран] - 17-он (или 5-О-деметил - 22, 23 - дигидроавермектин А1a).
Компонент H2B1б - (2aE, 4E, 8E) - (5'S, 6S, 'R, 7S, 11R, 13R, 15S, 17aR, 20R, 20аR, 20bS) - 20, 20b - дигидрокси - 5', 6, 8, 19 - тетраметил - 6' - (1-метилэтил) - 7 - [[(3-O-метил - 4-O-(3-O-метил - 2, 6-дидеокси-α-L-арабино-гексапиранозил) - 2, 6-дидеокси-α-L-арабино-гексапиранозил]-окси] - 3', 4', 5', 6, 6', 7, 10, 11, 14, 15, 17а, 20, 20а-, 20b - тетрадекагидроспиро [11, 15 - метано - 2Н, -13Н, 17Н - фуро [4, 3, 2pq] [2, 6] бензодиоксациклооктадецен - 13, 2' - [2Н] пиран] - 17-он (или 25 - (1-метилэтил) - 5-O-диметил) - 25-де (1-метилпропил) - 22, 23 - дигидроавермектин A1a).
Содержание компонента H1B1a не менее 90 %.
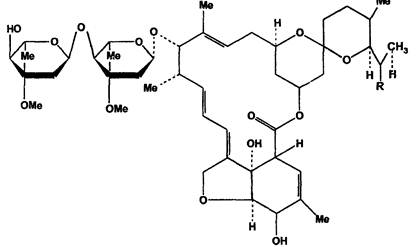
Структурная формула не приводится.
|
Компонент |
R |
Эмпирическая формула |
Молекулярная масса |
|
Н2В1а |
СНН2 - СНН3 |
C48H74O14 |
875 |
|
H2B1b |
СН3 |
С47Н72O14 |
861 |
Ивермектин - кристаллический порошок, без запаха, цвет от белого до желтовато-белого. Насыпная плотность от 1,1 до 1,3 г/см3. Практически нерастворим в воде (около 4 мкг/мл), алифатических углеводородах и циклогексане. Растворим в этиловом спирте, хорошо растворим в метиленхлориде, метилэтилкетоне, пропиленгликоле, полиэтиленгликоле. Ивермектин получают путем селективного каталитического восстановления абамектина, который в свою очередь является продуктом жизнедеятельности почвенных организмов Streptomyces averraitilis.
Ивермектин не имеет определенной точки плавления, при нагревании обугливается. Ввиду очень слабой растворимости в воде стабильность водных растворов ивермектина не изучена.
Краткая токсикологическая характеристика
Ивермектин обладает нервно-паралитическим действием. ЛД50 для лабораторных животных при однократном пероральном введении 15 - 60 мг/кг м.т.
Данные о максимально допустимом уровне (MRL) ивермектина в тканях и органах сельскохозяйственных животных в соответствии с рекомендациями Европейского комитета ветеринарных продуктов и Всемирной организации здравоохранения (1998) представлены в таблице 1.
Таблица 1
|
Животные |
Ткани, органы |
Максимально допустимый уровень |
|
Крупный рогатый скот |
Мышцы* |
0,01 мг/кг |
|
Печень |
0,1 мг/кг |
|
|
Жир |
0,04 мг/кг |
|
|
Молоко* |
0,005 мг/дм3 |
|
|
Свиньи, овцы |
Мышцы* |
0,01 мг/кг |
|
Печень |
0,015 мг/кг |
|
|
Жир |
0,02 мг/кг |
|
|
__________________ * Рекомендации Объединенного совещания ФАО/ВОЗ по остаточным количествам пестицидов в продуктах питания, 20 - 29 сентября 2000 г. |
||
Область применения препарата
Ивермектин обладает инсектицидной, акарицидной и нематоцидной активностью. Антибактериальной и антигрибковой активности не обнаружено. Ивермектин рекомендуется к применению в качестве анти-паразитарного и антигельминтного препарата для сельскохозяйственных животных (свиней, крупного и мелкого рогатого скота).
Гигиенические нормативы в России не установлены.
1. Метрологические характеристики метода
Метрологические характеристики метода представлены в табл. 2 и 3.
Таблица 2
Метрологические параметры
|
Анализируемый объект |
Метрологические параметры, Р = 0,95, n = 20 |
||||
|
|
предел обнаружения, мг/кг |
диапазон определяемых концентраций, мг/кг |
среднее значение определения, % |
стандартное отклонение, S,% |
доверительный интервал среднего результата, % |
|
Печень |
0,001 |
0,001 - 0,02 |
81,36 |
2,27 |
3,31 |
|
Почки |
0,001 |
0,001 - 0,02 |
81,31 |
3,06 |
4,46 |
|
Мясо |
0,001 |
0,001 - 0,02 |
82,69 |
3,81 |
5,55 |
|
Жир свиной |
0,002 |
0,002 - 0,04 |
79,99 |
3,92 |
5,71 |
|
Молоко |
0,001 |
0,001 - 0,02 |
91,30 |
2,80 |
4,08 |
Полнота
извлечения ивермектина из проб печени, почек, мяса, жира и молока
сельскохозяйственных животных
(5 повторностей для каждой концентрации)
|
Среда |
Внесено ивермектина мг/кг |
Обнаружено ивермектина мг/кг |
Полнота извлечения, % |
|
Печень свиная |
0,001 |
0,0008073 ± 0,00006 |
80,73 |
|
0,002 |
0,0016324 ± 0,00009 |
81,62 |
|
|
0,01 |
0,008186 ± 0,00019 |
81,86 |
|
|
0,02 |
0,016248 ± 0,00054 |
81,24 |
|
|
Почки свиные |
0,001 |
0,0008124 ± 0,00007 |
81,24 |
|
0,002 |
0,0016164 ± 0,00010 |
80,82 |
|
|
0,01 |
0,008108 ± 0,00016 |
81,08 |
|
|
0,02 |
0,016418 ± 0,00062 |
82,09 |
|
|
Мясо |
0,001 |
0,0008385 ± 0,00006 |
83,85 |
|
0,002 |
0,0016490 ± 0,00010 |
82,45 |
|
|
0,01 |
0,008241 ± 0,00017 |
82,41 |
|
|
0,02 |
0,016412 ± 0,00060 |
82,06 |
|
|
Жир свиной (сало) |
0,002 |
0,0015934 ± 0,00014 |
79,67 |
|
0,004 |
0,0031968 ± 0,00022 |
79,92 |
|
|
0,02 |
0,016088 ± 0,00085 |
80,44 |
|
|
0,04 |
0,031980 ± 0,00142 |
79,95 |
|
|
Молоко |
0,001 |
0,0009060 ± 0,00005 |
90,60 |
|
0,002 |
0,0018316 ± 0,00008 |
91,58 |
|
|
0,01 |
0,009174 ± 0,00014 |
91,74 |
|
|
0,02 |
0,018260 ± 0,00047 |
91,30 |
2. Метод измерений
Методика основана на определении вещества с помощью высокоэффективной жидкостной хроматографии (ВЭЖХ) с флуориметрическим детектором после экстракции из анализируемой пробы молока, органов и тканей сельскохозяйственных животных ацетонитрилом, очистки экстракта перераспределением между двумя несмешивающимися фазами. Экстракты органов и тканей сельскохозяйственных животных подвергают дополнительной очистке на концентрирующем патроне с флоризилом.
Количественное определение проводится методом абсолютной калибровки.
3. Средства измерений, вспомогательные устройства, реактивы и материалы
3.1. Средства измерений
|
Жидкостный хроматограф с флуориметрическим детектором, с переменной длиной волны (фирмы Perkin-Elmer, США) |
Номер Госреестра 15945-97 |
|
Весы аналитические ВЛА-200 |
|
|
Весы лабораторные общего назначения, с наибольшим пределом взвешивания до 500 г и пределом допустимой погрешности ±0,038 г |
|
|
Колбы мерные вместимостью 50, 100 и 1000 см3 |
|
|
Пипетки градуированные 2-го класса точности вместимостью 1,0, 2,0, 5,0, 10 см3 |
|
|
Пипетки с одной меткой 2-го класса точности вместимостью 15 см3 |
|
|
Пробирки градуированные вместимостью 5 или 10 см3 |
|
|
Цилиндры мерные 2-го класса точности вместимостью 10, 25, 50, 100, 200, 500 и 1000 см3 |
|
|
Допускается использование средств измерения с аналогичными или лучшими характеристиками. |
|
3.2. Реактивы
3.3. Вспомогательные устройства, материалы
4. Требования безопасности
4.1. При работе с реактивами соблюдают требования безопасности, установленные для работ с токсичными, едкими, легковоспламеняющимися веществами по ГОСТ 12.1.005.
4.2. При выполнении измерений с использованием жидкостного хроматографа соблюдают правила электробезопасности в соответствии с ГОСТ 12.1.019 и инструкцией по эксплуатации прибора.
5. Требования к квалификации операторов
К выполнению измерений допускают специалистов, имеющих квалификацию не ниже лаборанта-исследователя, с опытом работы на жидкостном хроматографе.
6. Условия измерений
При выполнении измерений соблюдают следующие условия:
• процессы приготовления растворов и подготовки проб к анализу
• проводят при температуре воздуха (20 ± 5) °С
• и относительной влажности не более 80 %;
• выполнение измерений на жидкостном хроматографе проводят в условиях, рекомендованных технической документацией к прибору.
7. Подготовка к выполнению измерений
Выполнению измерений предшествуют следующие операции: очистка органических растворителей (при необходимости), приготовление растворов, подвижной фазы для ВЭЖХ, кондиционирование хроматографической колонки, установление градуировочной характеристики, подготовка патронов для очистки экстрактов, проверка хроматографического поведения вещества на патронах для твердофазной экстракции.
7.1. Подготовка органических растворителей
7.1.1. Очистка ацетонитрила
Ацетонитрил кипятят с обратным холодильником над пентоксидом фосфора не менее 1 ч, после чего перегоняют, непосредственно перед употреблением ацетонитрил повторно перегоняют над прокаленным карбонатом калия.
7.1.2. Очистка Н-гексана
Растворитель последовательно промывают порциями концентрированной серной кислоты до тех пор, пока она не перестанет окрашиваться в желтый цвет, далее водой до нейтральной реакции промывных вод, перегоняют над поташом.
7.2. Подготовка подвижной фазы для ВЭЖХ
В мерную колбу вместимостью 1000 см3 помещают 980 см3 метанола, добавляют 20 см3 бидистиллированной или деионизированной воды, перемешивают, фильтруют и дегазируют.
7.3. Кондиционирование хроматографической колонки
Промывают колонку подвижной фазой (приготовленной по п. 7.2) при скорости подачи растворителя 1,7 см3/мин. до установления стабильной базовой линии.
7.4. Приготовление реактива для дериватизации
Смешивают трифторуксусный ангидрид и свежеперегнанный ацетонитрил в объеме 1∶2. Реактив годен к употреблению в течение рабочего дня.
7.5. Приготовление градуировочных растворов
7.5.1. Исходный раствор ивермектина для градуировки (концентрация 100 мкг/см3). В мерную колбу вместимостью 100 см3 помещают 0,0100 г ивермектина, растворяют в 50 - 70 см3 метанола, доводят метанолом до метки, тщательно перемешивают. Раствор хранится в морозильной камере в течение месяца.
Растворы № 1 - 5 готовят объемным методом путем последовательного разбавления исходного стандартного раствора.
7.5.2. Раствор № 1 ивермектина для градуировки (концентрация 1 мкг/см3). В мерную колбу вместимостью 100 см3 помещают 1 см3 исходного стандартного раствора ивермектина концентрацией 100 мкг/см3 (п. 7.5.1), разбавляют метанолом до метки. Раствор хранится в морозильной камере в течение 10 дней.
Этот стандартный раствор используют для приготовления проб с внесением при оценке полноты извлечения ивермектина из исследуемых образцов.
7.5.3. Рабочие растворы № 2 - 5 ивермектина для градуировки (концентрация 0,005 - 0,1 мкг/см3). В 5 мерных колб вместимостью 100 см3 помещают по 0,5, 1,0, 2,5, 5,0 и 10,0 см3 стандартного раствора № 1 с концентрацией 1 мкг/см3 (п. 7.5.2), доводят до метки ацетонитрилом, тщательно перемешивают, получают рабочие растворы № 2 - 5 с концентрацией ивермектина 0,005, 0,01, 0,025, 0,05 и 0,10 мкг/см3 соответственно. Растворы хранятся в морозильной камере не более недели.
7.6. Установление градуированной характеристики
Градуировочную характеристику, выражающую зависимость площади пика (отн. единицы) от концентрации ивермектина в растворе (мкг/см3), устанавливают методом абсолютной калибровки по 5 растворам флуорогенного производного ивермектина для градуировки.
Для построения градуировочной характеристики в градуировочные пробирки вместимостью 5 см3 вносят по 1 см3 каждого из 5 рабочих растворов ивермектина № 2 - 5, прибавляют по 0,1 см3 1-N-метилимидазола, перемешивают. Смесь охлаждают до 0 - 5 °С, помещая пробирки в ледяную баню, добавляют по каплям 0,3 см3 реактива для дериватизации (п. 7.4), перемешивают и выдерживают 2 ч при комнатной температуре.
В инжектор хроматографа вводят по 20 мм3 каждого градуировочного раствора и анализируют в условиях хроматографирования по п. 9.4. Осуществляют не менее 3 параллельных измерений.
7.7. Подготовка патрона для очистки экстрактов
Патрон для твердофазной экстракции устанавливают на аллонж с прямым отводом для вакуума*, сверху в патрон вставляют шприц с разъемом Льюера объемом не менее 10 см3, используемый в качестве емкости для элюента.
Концентрирующий патрон промывают 5 см3 метанола, высушивают пропусканием воздуха (с использованием вакуума) в течение 5 мин. Затем через патрон пропускают 5 см3 гексана. Процедуру проводят с использованием вакуума, скорость потока растворов через патрон не должна превышать 5 см3/мин, при этом нельзя допускать высыхания поверхности патрона.
________________
* Примечание. В отсутствии специального аллонжа, жидкость продавливают через патрон с помощью шприца, скорость продавливания раствора не должна превышать 1 - 2 капли в секунду.
8. Отбор проб
Отбор продуктов питания осуществляется в соответствии с требованиями ГОСТ на исследуемые продукты: ГОСТ 7269-79 «Мясо», ГОСТ 3622-68 «Молоко и молочные продукты».
Отобранные образцы продуктов герметично упаковывают в полиэтиленовые мешки, стеклянные банки с притертыми крышками. Образцы анализируют непосредственно после отбора проб или хранят в морозильной камере при - 20 °С (допускается хранение до 2 мес.).
Непосредственно перед анализом образцы размораживают, пробы органов и тканей массой 200 - 300 г тщательно измельчают с использованием гомогенизатора. Пробу гомогенизированного образца печени, почек и мяса массой 10 г, жира массой 5 г, а также молока массой 5 г взвешивают на аналитических весах в плоскодонных колбах вместимостью 250 см3.
9. Выполнение определения
9.1. Экстракция
К пробе гомогенизированного образца (10 г печени, почек, мяса, 5 г жира и молока), помещенной в колбу вместимостью 250 см3, приливают 100 см3 ацетонитрила, тщательно перемешивают путем встряхивания, выдерживают на ультразвуковой бане 5 мин., помещают на встряхиватель на 30 мин., дополнительно выдерживают на ультразвуковой бане 5 мин. и снова помещают на встряхиватель на 30 мин.
Экстракты тканей и органов декантируют в центрифужные сосуды емкостью 100 см3 и центрифугируют при 4 °С со скоростью 3 000 об./мин. в течение 10 мин., экстракту пробы молока дают отстояться. Прозрачную надосадочную жидкость переносят в делительную воронку вместимостью 250 см3, фильтруя ее через тампон из стекловаты, помещенный в конусную воронку. Добавляют 70 см3 гексана, интенсивно встряхивают в течение 1 мин. После полного разделения фаз нижний ацетонитрильный слой сливают в круглодонную колбу и упаривают досуха на ротационном вакуумном испарителе при температуре не более 40 °С. Сухой остаток растворяют в смеси 14 см3 ацетонитрила и 56 см3 воды, помещая на ультразвуковую баню на 1 мин. Раствор переносят в делительную воронку вместимостью 250 см3, добавляют 70 см3 гексана, интенсивно встряхивают воронку в течение 1 мин. Верхний органический слой собирают в круглодонную колбу вместимостью 250 см3. Водно-ацетонитрильную фазу вновь переносят в делительную воронку и повторяют операцию экстракции, используя 70 см3 гексана.
Объединенную органическую фазу упаривают досуха на ротационном вакуумном испарителе при температуре не более 40 °С. Сухой остаток растворяют в 1 см3 ацетонитрила и подвергают дериватизации по п. 9.2.
9.2. Дериватизация
К ацетонитрильному раствору прибавляют 0,1 см3 l-N-метилимидазола, перемешивают. Смесь охлаждают до 0 - 5 °С, помещая колбу в ледяную баню, добавляют по каплям 0,3 см3 реактива для дериватизации (п. 7.4), перемешивают и выдерживают 2 ч при комнатной температуре.
Дериватизованные экстракты проб молока анализируют в условиях хроматографирования по п. 9.3.
Дериватизованные экстракты проб почек, печени, мяса и жира подвергают дополнительной очистке по п. 9.3.
9.3. Очистка экстракта
Аликвоту раствора после дериватизации объемом 0,7 см3 переносят в градуированную пробирку вместимостью 5 см3, добавляют 5 см3 гексана, интенсивно встряхивают в течение 1 мин., верхний гексановый слой отбирают с помощью пипетки, перенося в стакан вместимостью 50 см3, операцию экстракции повторяют новой порцией гексана объемом 5 см3. Верхний гексановый слой также переносят в химический стакан, объединяя с первым экстрактом. Объединенный гексановый экстракт вносят на патрон для твердофазной экстракции Florisil Sep Рак, подготовленный по п. 7.7. Скорость прохождения раствора через патрон не должна превышать 1 - 2 капли в с. Элюат собирают непосредственно в круглодонную колбу.
Флуорогенное производное ивермектина дополнительно элюируют с патрона 5 см3 гексана, также объединяя элюат с первой порцией в круглодонной колбе. Раствор упаривают досуха при температуре не выше 35 °С. Остаток в колбе растворяют в 1,4 см3 ацетонитрила и анализируют на содержание ивермектина по п. 9.4.
9.4. Условия хроматографирования
Колонка стальная, длиной 25 см, внутренним диаметром 4,0 мм, содержащая Кромасил 100 С18, зернением 7 мкм
Температура колонки: комнатная
Подвижная фаза: метанол - вода (98∶2 по объему)
Скорость потока элюента: 1,7 куб. см/мин.
Длина волны: возбуждение 364 нм
Эмиссия 470 нм
Показание аттенюатора: 64
Объем вводимой пробы: 20 мм3
Ориентировочное время выхода флуорогенного производного ивермектина: 11,1 - 11,5 мин.
Образцы, дающие пики большие, чем стандартный раствор ивермектина с концентрацией 0,005 мкг/см3, разбавляют ацетонитрилом.
10. Обработка результатов анализа
Содержание ивермектина в пробе рассчитывают по формуле:
![]()
X - содержание ивермектина в пробе, мг/кг;
А - концентрация ивермектина, найденная по градуировочному графику, мкг/см3;
V - объем экстракта, подготовленного для хроматографирования, см3;
m - масса анализируемого образца, г;
K - коэффициент пересчета, учитывающий объем реакционной смеси после дериватизации экстрактов проб, используемый для анализа, равный для молока - 1, печени, почек, мяса и жира - 2.
4. Разработчики
Юдина Т.В., д.б.н., проф., Федорова Н.Е., д.б.н., Волкова В.Н., к.х.н.
Федеральный научный центр гигиены им. Ф.Ф. Эрисмана (ФНЦГ им. Ф.Ф. Эрисмана).
141000, г. Мытищи Московской обл., ул. Семашко, д. 2, лаборатория аналитических методов контроля.
Содержание