| Информационная система |  |
|
СОВЕТ ЭКОНОМИЧЕСКОЙ ВЗАИМОПОМОЩИ |
СТАНДАРТ СЭВ
СТ СЭВ 2716-80
ПРЕПАРАТЫ РАДИОАКТИВНЫЕ
ВОДА ТРИТИРОВАННАЯ
Постановлением Государственного комитета СССР по стандартам от 17 июля 1981 г. № 3406 стандарт Совета Экономической Взаимопомощи СТ СЭВ 2716-80 «Препараты радиоактивные. Вода тритированная» введен в действие непосредственно в качестве государственного стандарта СССР
в народном хозяйстве СССР
с 01.01. 1984 г.
в договорно-правовых отношениях по сотрудничеству
с 01.01. 1983 г.
|
СТАНДАРТ СЭВ |
СТ СЭВ 2716-80 |
|
|
|
Препараты радиоактивные ВОДА ТРИТИРОВАННАЯ |
|||
|
Взамен |
|
||
|
Группа Ф14 |
|
Утвержден Постоянной Комиссией по
сотрудничеству
в области стандартизации
Берлин, декабрь 1980 г.
Настоящий стандарт СЭВ распространяется на воду, содержащую в своем составе радиоактивный изотоп водорода-тритий (далее препарат), используемую в биохимических исследованиях и в качестве радиоактивного сырья для получения меченых соединений и препаратов.
Формула воды тритированной: 3Н2О.
1. ТЕХНИЧЕСКИЕ ТРЕБОВАНИЯ
1.1. Препарат должен быть прозрачным, бесцветным, без посторонних частиц, видимых невооруженным глазом.
1.2. Измеренные значения удельной активности трития в препарате при доверительной вероятности Р = 0,95 должны лежать в следующих доверительных границах, TBq×g-1:
от 0,02 до 0,04
» 0,1 » 0,2
» 0,5 » 1,0
» 2,0 » 4,0
1.3. Примесь других радионуклидов не допускается.
1.4. Доверительные границы измеренных значений водородного показателя рН свежеперегнанной воды, тритированной при доверительной вероятности Р = 0,95, должны лежать в диапазоне от 5,0 до 7,0.
1.5. Номинальные значения активности препарата в ампуле должны соответствовать одному из значений, указанных в табл. 1.
Отклонение активности препарата в ампуле от указанных в табл. 1 номинальных значений не должно превышать 10 % при доверительной вероятности Р = 0,95.
Таблица 1
|
cm3 |
Номинальные значения активности трития в ампуле TBq при удельной активности (TBq×g-1) |
|||
|
от 0,02 до 0,04 |
от 0,1 до 0,2 |
от 0,5 до 1,0 |
от 2,0 до 4,0 |
|
|
0,1 |
от 0,002 до 0,004 |
от 0,01 до 0,02 |
от 0,05 до 0,10 |
от 0,2 до 0,4 |
|
0,2 |
свыше 0,004 до 0,008 |
свыше 0,02 до 0,04 |
свыше 0,1 до 0,2 |
свыше 0,4 до 0,8 |
|
0,5 |
от 0,01 до 0,02 |
от 0,05 до 0,10 |
от 0,25 до 0,50 |
от 1,0 до 2,0 |
|
1,0 |
свыше 0,02 до 0,04 |
свыше 0,1 до 0,2 |
свыше 0,5 до 1,0 |
свыше 2,0 до 4,0 |
|
2,0 |
от 0,04 до 0,08 |
от 0,2 до 0,4 |
от 1,0 до 2,0 |
- |
1.6. Поток бета-частиц, вызванный радиоактивным загрязнением поверхности ампул с препаратом, не должен превышать 100 s-1. Относительная суммарная погрешность измерения не должна превышать 100 % при доверительной вероятности Р = 0,68.
2. ТРЕБОВАНИЯ БЕЗОПАСНОСТИ
2.1. При вскрытии запаянной ампулы с препаратом следует учитывать, что в процессе хранения давление в ней за счет образования радиогенного гелия-3 постепенно возрастает и может достигать к концу срока хранения 150 kРа.
2.2. По истечении указанного на этикетке срока хранения препарата в стеклянной ампуле его следует перевести в металлический сосуд с герметизирующей крышкой.
3. ПРАВИЛА ПРИЕМКИ
3.1. Препарат, подготовленный для расфасовки в ампулы, предъявляют партиями. В партию включают продукт, однородный по своим качественным показателям, сопровождаемый одним документом о качестве.
3.2. Для проверки качества препарата от каждой партии продукта отбирают пробу массой от 0,5 до 2,0 g.
3.3. Последовательность проведения контроля должна соответствовать указанной в табл. 2.
Таблица 2
|
Пункт требования |
Пункт метода контроля |
|
|
Цвет, прозрачность, посторонние частицы |
||
|
Удельная активность |
||
|
Содержание примеси других радионуклидов |
||
|
Водородный показатель рН |
||
|
Активность трития в препарате |
||
|
Поверхностное загрязнение ампулы радиоактивными веществами |
4. МЕТОДЫ КОНТРОЛЯ
4.1. Метод измерения удельной активности трития
4.1.1. Сущность метода
Удельную активность трития в препарате определяют путем измерения активности трития, с использованием калориметрического метода и массы пробы, отобранной от партии продукта в специальную градуированную по объему и точно взвешенную ампулу.
Тепловой поток от контролируемой пробы, обусловленный выделением энергии при радиоактивном распаде трития, определяют относительным методом путем сличения показаний калориметрической установки при измерении тепловых потоков пробы и образцового электрического нагревателя (или образцового радиоактивного источника).
Допускается измерять активность трития любым другим методом, обеспечивающим погрешность измерения, не превышающую 6 % при доверительной вероятности Р = 0,95.
Массу препарата определяют путем взвешивания и вычисляют как разность величин, полученных при измерении массы калиброванной ампулы с препаратом и без него.
4.1.2. Аппаратура
4.1.2.1. Аналитические весы с пределом взвешивания до 200 g и с суммарной систематической погрешностью измерения массы не более 0,2 mg при доверительной вероятности Р = 0,95.
4.1.2.2. Калиброванная ампула с притертой пробкой объемом 5 cm3 и массой не более 10 g.
4.1.2.3. Шприц медицинский объемом 5 cm3.
4.1.2.4. Калориметрическая установка, в которую входят: дифференциальный микрокалориметр (типа Кальве) с диапазоном измерения теплового потока от 10-4 до 10-2 W, с чувствительностью не ниже 10-5 W и с суммарной систематической погрешностью измерения не более 0,5 % при доверительной вероятности Р = 0,95;
калиброванная ампула с герметичной крышкой объемом 3 cm3 и массой не более 10 g;
образцовые электрические нагреватели со стабилизированным источником питания (аккумуляторная батарея) и измерительной схемой, обеспечивающие регулирование и поддержание электрической мощности в нагревателях в диапазоне от 10-5 до 10-2 W и ее измерение с суммарной систематической погрешностью не более 0,05 % при доверительной вероятности Р = 0,95.
4.1.2.5. Помещение, в котором проводятся измерения, должно быть термостатировано (T £ ±1 °С), кондиционировано (влажность от 40 до 60 % при T = 25 °С).
4.1.3. Подготовка к измерениям
Помещают предварительно высушенную калиброванную ампулу с герметичной пробкой на чашку весов и производят пятикратное ее взвешивание.
Вводят в калиброванную ампулу с помощью медицинского шприца 2 cm3 препарата.
Помещают калиброванную ампулу с препаратом на весы и производят пятикратное взвешивание.
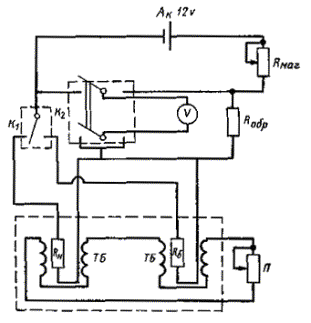
Для градуировки калориметрической установки устанавливают образцовый электрический нагреватель в ячейку дифференциального микрокалориметра. Изменяя мощность его нагрева, регистрируют установившиеся показания прибора на выходе микрокалориметра. Градуировку производят в диапазоне мощностей от 10-4 до 10-2 W вблизи номинальных значений, составляющих следующий ряд: 0,5; 1,0; 2,0; 5,0; 10,0; 50,0 mW.
Схема калибровки калориметра с помощью электрических нагревателей приведена на черт. 1.
В каждой из указанных точек проводят по три параллельных измерения.
По полученным данным определяют коэффициенты линейной регрессии а и b по формулам:
где у - тепловой поток, mW;
х - показания прибора на выходе микрокалориметра, mW.
 (2)
(2)
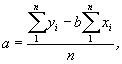 (3)
(3)
где n = 7´3 = 21 - полное число измерений в процессе градуировки.
Rн - нагреватель с сопротивлением 100 Ω; Rб - балластное сопротивление 100 Ω; Rобр - образцовое сопротивление; Rмаг - магазин сопротивлений (реостат); Ак - аккумуляторная батарея; К1, К2 - переключатели с медными контактами; V - вольтметр с диапазоном измеряемых напряжений от 0,001 до 10 V; ТБ - термобатареи калориметра; П - потенциометр постоянного тока
Оценку дисперсии S02 результатов, измеренных при градуировке значений теплового потока, относительно вычисленных по формуле (1), определяют по формуле
Оценки дисперсии для коэффициентов регрессии а и b вычисляют по формулам:
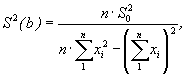 (5)
(5)
![]() (6)
(6)
Доверительные границы случайной погрешности результатов расчета для а и b при доверительной вероятности Р = 0,95 вычисляют по формулам:
где tg(P,f) - квантиль распределения Стьюдента при доверительной вероятности Р и степенях свободы f = n - 2.
При Р = 0,95 и f = 21 - 2 = 19; tg(0,95; 19) = 2,09.
4.1.4. Проведение измерений
Для определения теплового потока устанавливают калиброванную ампулу с контролируемой пробой тритированной воды с массой (2,0 ± 0,1) g в гнездо микрокалориметра и после установления теплового равновесия регистрируют показания прибора. Измерения повторять пять раз.
Примечание. Для повышения точности измерений во вторую ячейку микрокалориметра при градуировке и измерениях устанавливают вторую калиброванную ампулу с двумя граммами дистиллированной воды, идентичную ампуле с контролируемой пробой.
4.1.5. Обработка результатов измерения
Величину среднего значения
результатов взвешивания калиброванной ампулы с препаратом ![]() в миллиграммах определяют по формуле
в миллиграммах определяют по формуле
Величину среднего значения
результатов взвешивания калиброванной ампулы без препарата ![]() в миллиграммах определяют по формуле
в миллиграммах определяют по формуле
Среднее значение массы пробы
препарата ![]() в миллиграммах вычисляют по формуле
в миллиграммах вычисляют по формуле
Оценки средних квадратических отклонений результатов каждой из серий
взвешивания ![]() и
и ![]() вычисляют по формулам:
вычисляют по формулам:
Оценку среднего квадратического отклонения результатов
измерения массы пробы препарата ![]() определяют по формуле
определяют по формуле
Доверительные границы
случайной составляющей погрешности результата измерения массы
пробы препарата ![]() вычисляют по формуле
вычисляют по формуле
![]() (15)
(15)
где tg(P,f) - квантиль распределения Стьюдента при доверительной вероятности Р и степенях свободы f = n - 1;
п - число параллельных взвешиваний.
При Р = 0,95, n = 5 и f = 4; tg(0,95; 4) = 2,78.
Границы суммарной погрешности результата измерения массы пробы препарата ![]() вычисляют по формуле
вычисляют по формуле
где ![]() - границы неисключенной систематической погрешности результата
взвешивания, включающей следующие компоненты:
- границы неисключенной систематической погрешности результата
взвешивания, включающей следующие компоненты:
1) неравноплечность коромысла весов (Q1 £ 2 mg);
2) неточность навешивания встроенных гирь (Q2 £ 0,12 mg);
3) неточность разновесов (Q3 £ 0,1 mg);
Суммарная погрешность результата измерения массы пробы препарата не должна превышать 0,5 % при доверительной вероятности Р = 0,95.
Форма записи результатов
измерения массы в миллиграммах ![]() , Р = 0,95.
, Р = 0,95.
Среднее значение результатов наблюдения теплового потока контролируемой пробы в милливаттах вычисляют по формуле
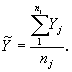 (17)
(17)
Оценку среднего квадратического отклонения результатов измерения теплового потока вычисляют по формуле
 (18)
(18)
где Yn - среднее значение теплового потока в п измерениях в процессе градуировки микрокалориметра.
Доверительную границу случайной погрешности результата измерения теплового потока вычисляют по формуле
![]() (19)
(19)
где tg(Р, f) - квантиль распределения Стьюдента при доверительной вероятности Р и степенях свободы f = n - 2.
Границу суммарной погрешности результата измерения теплового потока вычисляют по формуле
 (20)
(20)
где 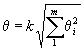 - граница неисключенной систематической погрешности результата
измерения теплового потока, включающей следующие компоненты:
- граница неисключенной систематической погрешности результата
измерения теплового потока, включающей следующие компоненты:
1) погрешность измерения падения напряжения на образцовом электрическом нагревателе и образцовой измерительной катушке (Q1 £ 0,02 %, Р = 0,95);
2) погрешность учета потерь теплового потока в токоподводящих проводах (Q2 £ 0,01 %, Р = 0,95);
3) погрешность, вносимую включением измерительного вольтметра в цепь (Q3 £ 0,01 %, P = 0,95);
4) погрешность измерения термоэлектродвижущей силы микрокалориметрических ячеек (Q4 £ 0,002 %, Р = 0,95);
5) неидентичность микрокалориметрических ячеек (Q5 £ 0,01 %, P = 0,95).
k = 1,1 при доверительной вероятности Р = 0,95.
Удельную активность препарата рассчитывают по формуле в TBq×g-1
где 1,1 - переводной коэффициент от теплового потока в милливаттах к активности трития в TBq.
Относительную суммарную погрешность результата измерения удельной активности вычисляют по формулам:
![]() (22)
(22)
где d(Q) - ошибка в определении средней энергии бета-частиц при распаде трития;
d(Q) = 0,05 при доверительной вероятности Р = 0,95.
Суммарная погрешность результата измерения удельной активности не должна превышать 6 % при доверительной вероятности Р = 0,95.
Форма записи
результатов измерения удельной активности препарата в Bq×g-1: ![]() , Р = 0,95,
, Р = 0,95,
4.2. Определение водородного показателя рН
Определение водородного показателя рН препарата осуществляется с помощью рН-метра, прокалиброванного по стандартным буферным растворам.
Для измерений используют стандартный рН-метр с диапазоном измерения от 2 до 10 рН с чувствительностью не ниже 0,05 рН и погрешностью измерения не более 2 % при доверительной вероятности Р = 0,95.
Калибровку прибора проводят по следующим трем стандартным буферным растворам:
1) Раствор калия фталевокислого, кислого (0,05 mol×l-1, рН = 4,0 при Т = 20 °С);
2) Раствор калия фосфорнокислого однозамещенного (0,025 mol×l-1) и раствор натрия фосфорнокислого двузамещенного (0,025 mol×l-1, рН = 6,88 при Т = 20 °С);
3) Раствор натрия тетраборного кислого (0,05 mol×l-1, рН = 9,22 при Т = 20 °С).
Относительная суммарная погрешность результата измерения значения рН контролируемой пробы препарата не должна превышать 3 % при доверительной вероятности Р = 0,95.
4.3. Проверка цвета и прозрачности
Цвет и прозрачность раствора воды тритированной контролируется визуально.
4.4. Контроль содержания примеси других радионуклидов
Отсутствие примеси других радионуклидов в препарате обеспечивается технологией производства.
4.5. Определение активности трития в ампулах с препаратом
Активность трития в ампулах с препаратом обеспечивается технологией дозировки.
4.6. Контроль радиоактивного загрязнения поверхности ампул
Отсутствие радиоактивного загрязнения поверхности ампул выше допустимого уровня обеспечивается процессом расфасовки, технологией герметизации и дезактивации ампул.
5. УПАКОВКА, МАРКИРОВКА, ТРАНСПОРТИРОВАНИЕ И ХРАНЕНИЕ
5.1. Упаковка
Препарат должен поставляться в запаянных ампулах из термостойкого стекла. Размеры ампул приведены на черт. 2.
Препараты объемом от 0,1 до 0,2 cm3 фасуют в ампулы объемом 1,0 cm3. В остальных случаях препарат фасуют в ампулы объемом 5,0 cm3.
Ампулу с препаратом помещают в герметичный пенал (черт. 3) и упаковывают в транспортный защитный контейнер.
В наружную упаковку транспортного защитного контейнера вкладывают инструкцию по его эксплуатации и паспорт на препарат.
5.2. Маркировка
Маркировка ампулы должна соответствовать требованиям СТ СЭВ 2713-80.
5.3. Транспортирование
Ампулы с препаратом, упакованные в соответствии с требованиями п. 5.1, транспортируют автомобильным, железнодорожным и авиационным транспортом без ограничения расстояния в условиях, обеспечивающих температуру ампул не ниже +5 °С.
мм
|
V, см3 |
D |
h |
Н |
|
5 |
14 |
50 |
70 |
|
1 |
10 |
20 |
30 |
Черт. 2
5.4. Хранение
5.4.1. Ампулы с препаратом должны храниться в складских помещениях при температуре окружающей среды от +5 ° до +50 °С.
5.4.2. Допустимый срок хранения препарата в ампулах: два месяца - для препаратов с удельной активностью от 2,0 до 4,0 TBq×g-1, шесть месяцев - для препаратов с удельной активностью от 0,5 до 1,0 TBq×g-1 и один год - для препаратов с удельной активностью от 0,1 до 0,2 TBq×g-1 и ниже, следующий за месяцем паспортизации препарата.
Конец
ИНФОРМАЦИОННОЕ ПРИЛОЖЕНИЕ 1
Взаимосвязь СТ СЭВ 2716-80 с «Правилами безопасной перевозки радиоактивных веществ» МАГАТЭ
|
Правила МАГАТЭ |
|
|
Правила безопасной перевозки радиоактивных веществ. Серия безопасности № 6. Пересмотренное издание, 1973 г., г. Вена |
ИНФОРМАЦИОННОЕ ПРИЛОЖЕНИЕ 2
1. ХАРАКТЕРИСТИКИ РАДИОНУКЛИДА ВОДОРОД-3
Радионуклид водород-3 - тритий - чистый бета-излучатель с периодом полураспада 12,34 года. Максимальная энергия бета-частиц составляет 2,98 fJ, а средняя их энергия 0,91 fJ.
Удельный тепловой поток, выделяемый при радиоактивном распаде трития, составляет 0,91 mW×TBq-1.
Максимальное (теоретически рассчитанное) значение удельной активности трития в препарате составляет 97,5 TBq×g-1.
2. ХАРАКТЕРИСТИКИ 3Н2O
Молярная активность трития в 3H2O составляет 292,5 TBq×mol-1; удельная активность - 41,8 TBq×g-1.
1. Автор - делегация СССР в Постоянной Комиссии по сотрудничеству в области использования атомной энергии в мирных целях.
2. Тема - 10.300.04-78.
3. Стандарт СЭВ утвержден на 48-м заседании ПКС.
4. Сроки начала применения стандарта СЭВ:
|
Страны - члены СЭВ |
Срок начала применения стандарта СЭВ в договорно-правовых отношениях по экономическому и научно-техническому сотрудничеству |
Срок начала применения стандарта СЭВ в народном хозяйстве |
|
НРБ |
Январь 1984 г. |
Январь 1984 г. |
|
ВНР |
Июнь 1983 г. |
Июнь 1984 г. |
|
ГДР |
|
|
|
Республика Куба |
|
|
|
МНР |
|
|
|
ПНР |
|
|
|
СРР |
Январь 1983 г. |
|
|
СССР |
Январь 1983 г. |
Январь 1984 г. |
|
ЧССР |
Январь 1983 г. |
Январь 1984 г. |
5. Срок первой проверки - 1989 г., периодичность проверки - 5 лет.
СОДЕРЖАНИЕ
|
5. Упаковка, маркировка, транспортирование и хранение. 8 Информационное приложение 1. 9 |

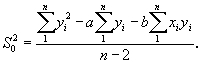 (
(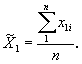 (
(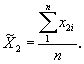 (
(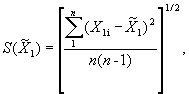 (
(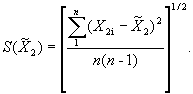 (
(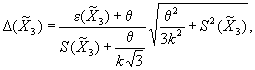 (
(