Информационная система |
| Карта сайта |
Скачать ГОСТ Р 54881-2011 Руководство по аудиту систем менеджмента качества изготовителей медицинских изделий на соответствие регулирующим требованиям. Часть 3. Отчет о проведении аудита
Дата актуализации: 10.08.2017


 ГОСТ Р 54881-2011
ГОСТ Р 54881-2011
Руководство по аудиту систем менеджмента качества изготовителей медицинских изделий на соответствие регулирующим требованиям. Часть 3. Отчет о проведении аудита
| Обозначение: |   ГОСТ Р 54881-2011 ГОСТ Р 54881-2011 |
| Обозначение англ: |   GOST R 54881-2011 GOST R 54881-2011 |
| Статус: | действует |
| Название рус.: | Руководство по аудиту систем менеджмента качества изготовителей медицинских изделий на соответствие регулирующим требованиям. Часть 3. Отчет о проведении аудита |
| Название англ.: | Guidelines for auditing of quality management systems of medical device manufacturers to conform to regulating requirements. Part 3. Audit report |
| Дата добавления в базу: | 01.09.2013 |
| Дата актуализации: | 05.05.2017 |
| Дата введения: | 01.01.2013 |
| Область применения: | Стандарт является руководством для регулирующих органов и организаций, проводящих аудиты, по составлению отчета о проведении аудита системы менеджмента качества изготовителя медицинских изделий на предмет соответствия данной системы регулирующим требованиям. Такой аудит должен быть основан на процессном подходе к требованиям к системам менеджмента качества. |
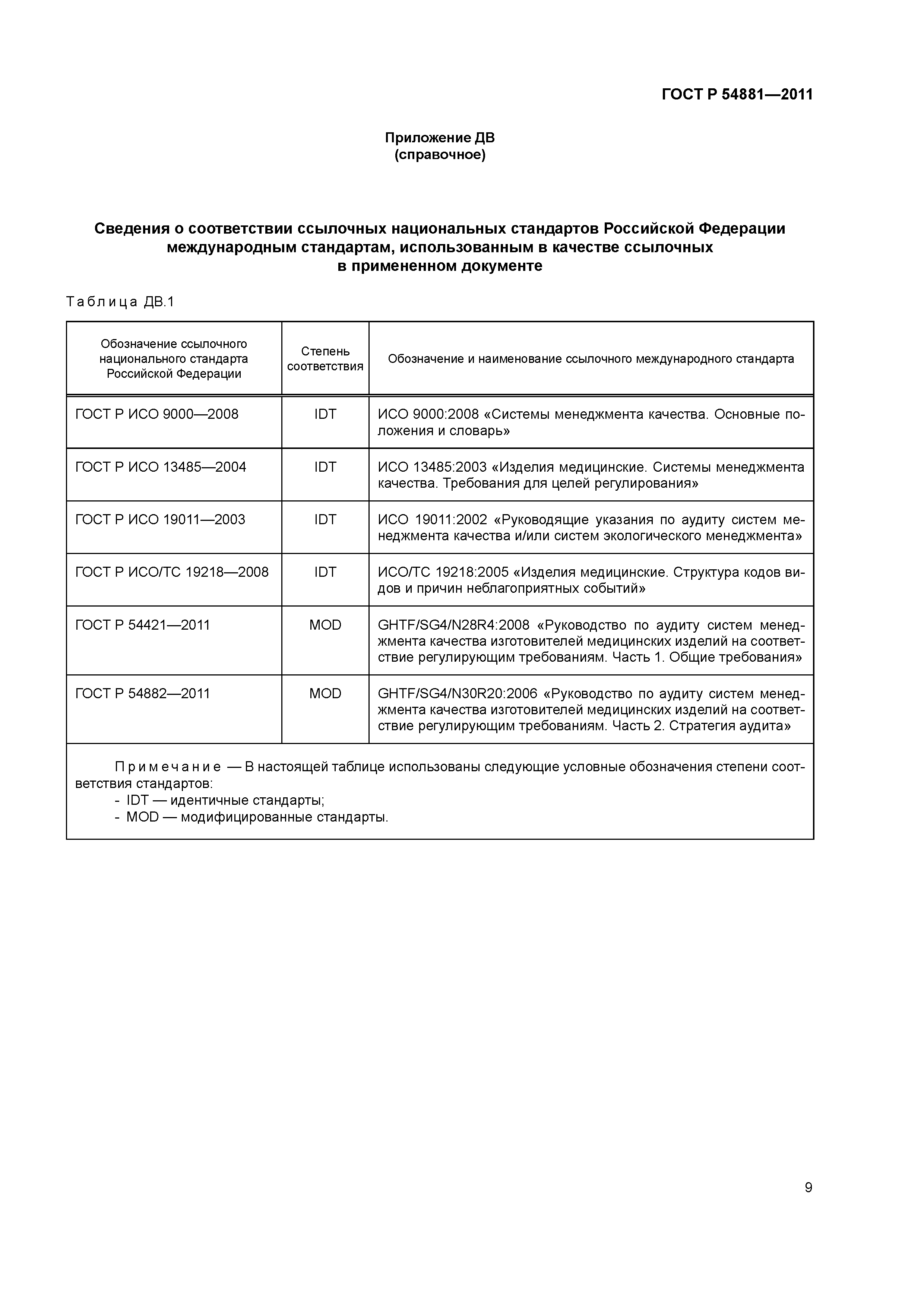
| Оглавление: | 1 Область применения 2 Нормативные ссылки 3 Термины и определения 4 Цели отчета о проведении аудита и удовлетворение потребностей пользователя 4.1 Цели отчета о проведении аудита 4.2 Ориентация на организации, проводящие аудиты, и/или регулирующие органы 4.3 Ориентация на уполномоченный федеральный орган, осуществляющий надзор за организациями, проводящими аудиты 4.4 Ориентация на изготовителя и/или проверяемую организацию 5 Основное содержание отчета о проведении аудита на соответствие регулирующим требованиям . 5.1 Данные, относящиеся к проверяемой организации 5.2 Данные, относящиеся к аудиту 5.3 Информация, полученная в ходе аудита 5.4 Аудиторское заключение 5.5 Дата и подписи 5.6 Приложения к отчету о проведении аудита Приложение ДА (обязательное) Сравнение структуры настоящего стандарта со структурой документа ОНТР/8О4/ГI33I16:2ОО7 «Руководство по аудиту систем менеджмента качества изготовителей медицинских изделий на соответствие регулирующим требованиям. Часть 3. Отчет о проведении аудита Приложение ДБ (обязательное) Текст измененных структурных элементов настоящего стандарта и документа ОНТР/8О4/ГI33I1б:2ОО7 «Руководство по аудиту систем менеджмента качества изготовителей медицинских изделий на соответствие регулирующим требованиям. Часть 3. Отчет о проведении аудита Приложение ДВ (справочное) Сведения о соответствии ссылочных национальных стандартов Российской Федерации международным стандартам, использованным в качестве ссылочных в примененном документе |
| Разработан: | ЗАО МЕДИ-ТЕСТ |
| Утверждён: | 13.12.2011 Федеральное агентство по техническому регулированию и метрологии (1188-ст) |
| Издан: | Стандартинформ (2012 г. ) |
| Расположен в: | |
| Нормативные ссылки: |
|














© 2013 Ёшкин Кот :-) Карта сайта
 ГОСТ Р ИСО 19011-2003 «Руководящие указания по аудиту систем менеджмента качества и/или систем экологического менеджмента»
ГОСТ Р ИСО 19011-2003 «Руководящие указания по аудиту систем менеджмента качества и/или систем экологического менеджмента»