Информационная система |
| Карта сайта |
Скачать ГОСТ Р ИСО 15197-2009 Системы диагностические in vitro. Требования к системам мониторного наблюдения за концентрацией глюкозы в крови для самоконтроля при лечении сахарного диабета
Дата актуализации: 10.08.2017

 ГОСТ Р ИСО 15197-2009
ГОСТ Р ИСО 15197-2009
Системы диагностические in vitro. Требования к системам мониторного наблюдения за концентрацией глюкозы в крови для самоконтроля при лечении сахарного диабета
| Обозначение: |  ГОСТ Р ИСО 15197-2009 ГОСТ Р ИСО 15197-2009 |
| Обозначение англ: |  GOST R ISO 15197-2009 GOST R ISO 15197-2009 |
| Статус: | отменен |
| Название рус.: | Системы диагностические in vitro. Требования к системам мониторного наблюдения за концентрацией глюкозы в крови для самоконтроля при лечении сахарного диабета |
| Название англ.: | In vitro diagnostic test systems. Requirements for blood-glucose monitoring systems for selftesting in managing diabetes mellitus |
| Дата добавления в базу: | 01.09.2013 |
| Дата актуализации: | 05.05.2017 |
| Дата введения: | 01.01.2013 |
| Область применения: | Стандарт устанавливает требования к системам мониторинга глюкозы in vitro, с помощью которых измеряют концентрацию глюкозы в пробах капиллярной крови, а также методы проверки и подтверждения эффективности этих систем пользователями. Такие системы предназначены для самоконтроля пользователей (непрофессионалов), страдающих сахарным диабетом. Стандарт применяется изготовителями таких систем и другими организациями (например, организациями по техническому регулированию и оценке соответствия), несущими ответственность за оценку эффективности работы таких систем. Стандарт - не обеспечивает всесторонней оценки всех возможных факторов, которые могут повлиять на рабочие характеристики таких систем, - не относится к измерению концентрации глюкозы для диагностирования сахарного диабета, - не касается медицинских аспектов лечения сахарного диабета и - не применяется к методам измерения, дающим результаты в порядковой шкале (например, визуальные, полуколичественные методы). |
| Оглавление: | 1 Область применения 2 Нормативные ссылки 3 Термины и определения 4 Проектирование и разработка 4.1 Общие требования 4.2 Безопасность 4.3 Прослеживаемость 4.4 Аспекты эргономического/человеческого фактора 4.5 Анализ рисков 4.6 Проверка, выполняемая пользователем 5 Информация, предоставляемая изготовителем 5.1 Этикетки для прибора, измеряющего концентрацию глюкозы в крови 5.2 Инструкции по применению системы мониторинга глюкозы в крови 5.3 Этикетки для системы реактивов и контрольного материала 5.4 Инструкции по применению реактивов и контрольного материала 6 Испытания надежности и безопасности 6.1 Общие требования 6.2 Защита от электрического удара 6.3 Защита от механических повреждений 6.4 Электромагнитная совместимость 6.5 Термостойкость 6.6 Стойкость к воздействию влаги и жидкостей 6.7 Защита от десорбированных газов, взрыва и имплозии 6.8 Компоненты измерительного устройства 6.9 Определение рабочих характеристик 6.10 Механическое сопротивление удару, вибрации и сотрясению 6.11 Пределы воздействия температуры на прибор 6.12 Протокол испытания на воздействие влажности на оборудование 6.13 Определение условий хранения и применения реактивов 7 Оценка аналитических характеристик 7.1 Общие требования 7.2 Оценка прецизионности 7.3 Оценка точности системы 7.4 Минимальная приемлемая точность системы 8 Оценка пользователя 8.1 Общие положения 8.2 Место выполнения оценки 8.3 Оценка пользователя 8.4 Оценка инструкций по применению Приложение А (обязательное) Дополнительные требования к электромагнитной совместимости Приложение В (справочное) Цепочка прослеживаемости Приложение С (справочное) Сведения о соответствии национальных стандартов Российской Федерации ссылочным международным стандартам Библиография |
| Разработан: | Лаборатория проблем клинико-лабораторной диагностики ГОУ ВПО ММА им. И.М. Сеченова Росздрава |
| Утверждён: | 09.12.2009 Федеральное агентство по техническому регулированию и метрологии (619-ст) |
| Издан: | Стандартинформ (2010 г. ) |
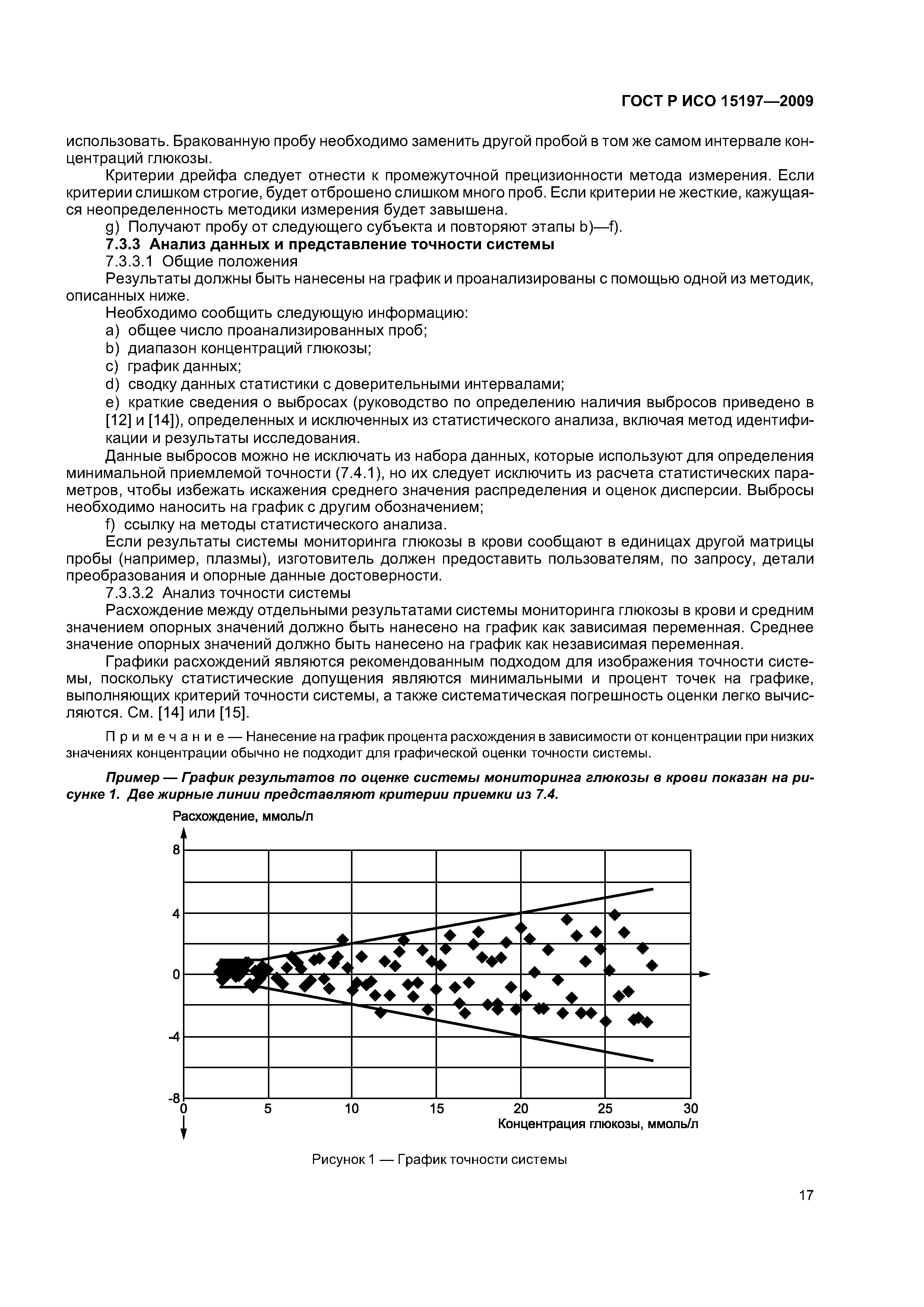
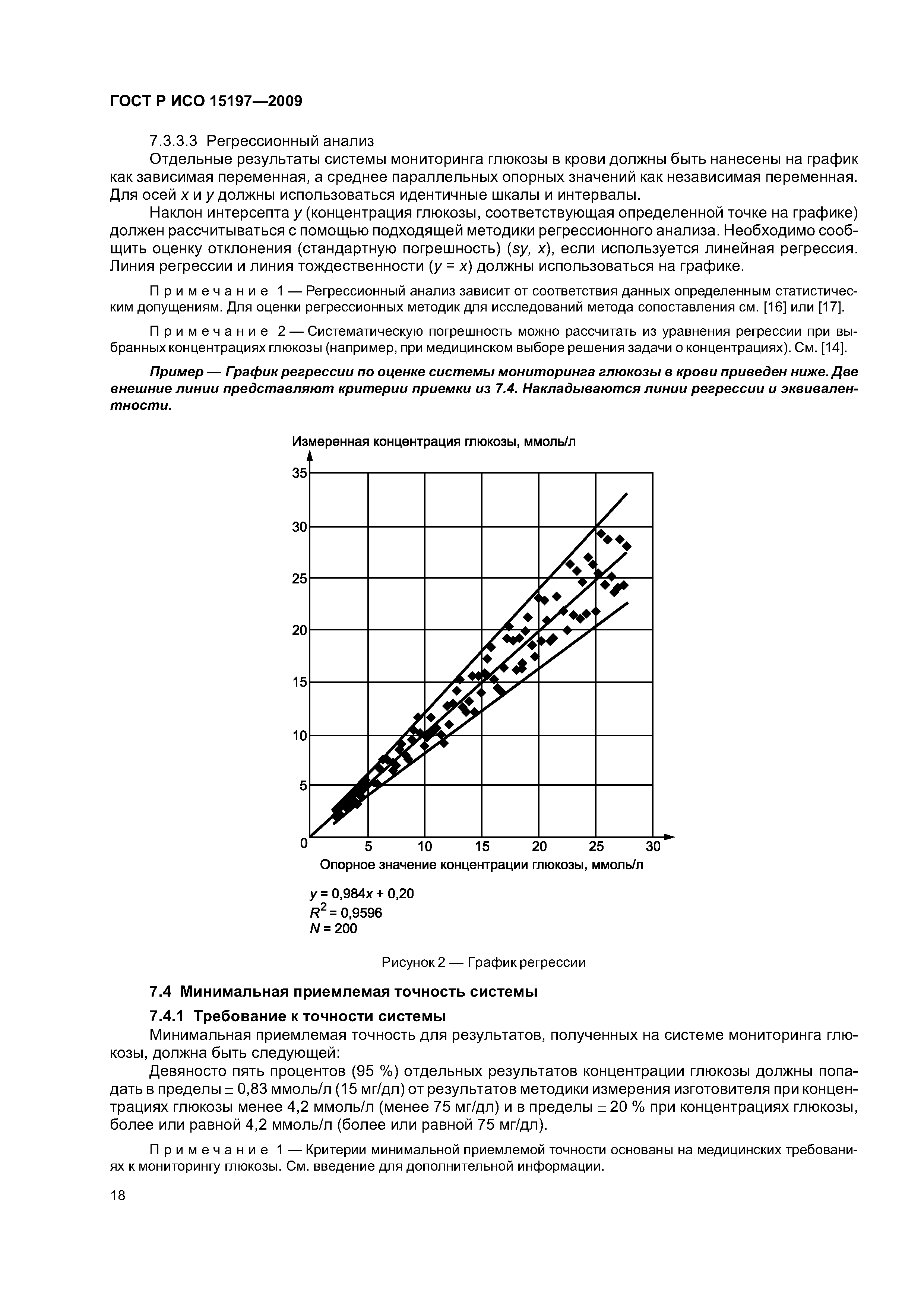
| Расположен в: | |
| Нормативные ссылки: |
|

























© 2013 Ёшкин Кот :-) Карта сайта
 ГОСТ Р 51317.4.2-99 «Совместимость технических средств электромагнитная. Устойчивость к электростатическим разрядам. Требования и методы испытаний»
ГОСТ Р 51317.4.2-99 «Совместимость технических средств электромагнитная. Устойчивость к электростатическим разрядам. Требования и методы испытаний»