Информационная система |
| Карта сайта |
Скачать ГОСТ Р ИСО 17593-2009 Клинические лабораторные исследования и изделия медицинские in vitro. Требования к системам мониторинга in vitro для самотестирования при пероральной терапии антикоагулянтами
Дата актуализации: 10.08.2017

 ГОСТ Р ИСО 17593-2009
ГОСТ Р ИСО 17593-2009
Клинические лабораторные исследования и изделия медицинские in vitro. Требования к системам мониторинга in vitro для самотестирования при пероральной терапии антикоагулянтами
| Обозначение: |  ГОСТ Р ИСО 17593-2009 ГОСТ Р ИСО 17593-2009 |
| Обозначение англ: |  GOST R ISO 17593-2009 GOST R ISO 17593-2009 |
| Статус: | отменен |
| Название рус.: | Клинические лабораторные исследования и изделия медицинские in vitro. Требования к системам мониторинга in vitro для самотестирования при пероральной терапии антикоагулянтами |
| Название англ.: | Clinical laboratory testing and in vitro medical devices. Requirements for in vitro monitoring systems for self-testing of oral anticoagulant therapy |
| Дата добавления в базу: | 01.09.2013 |
| Дата актуализации: | 05.05.2017 |
| Дата введения: | 01.01.2013 |
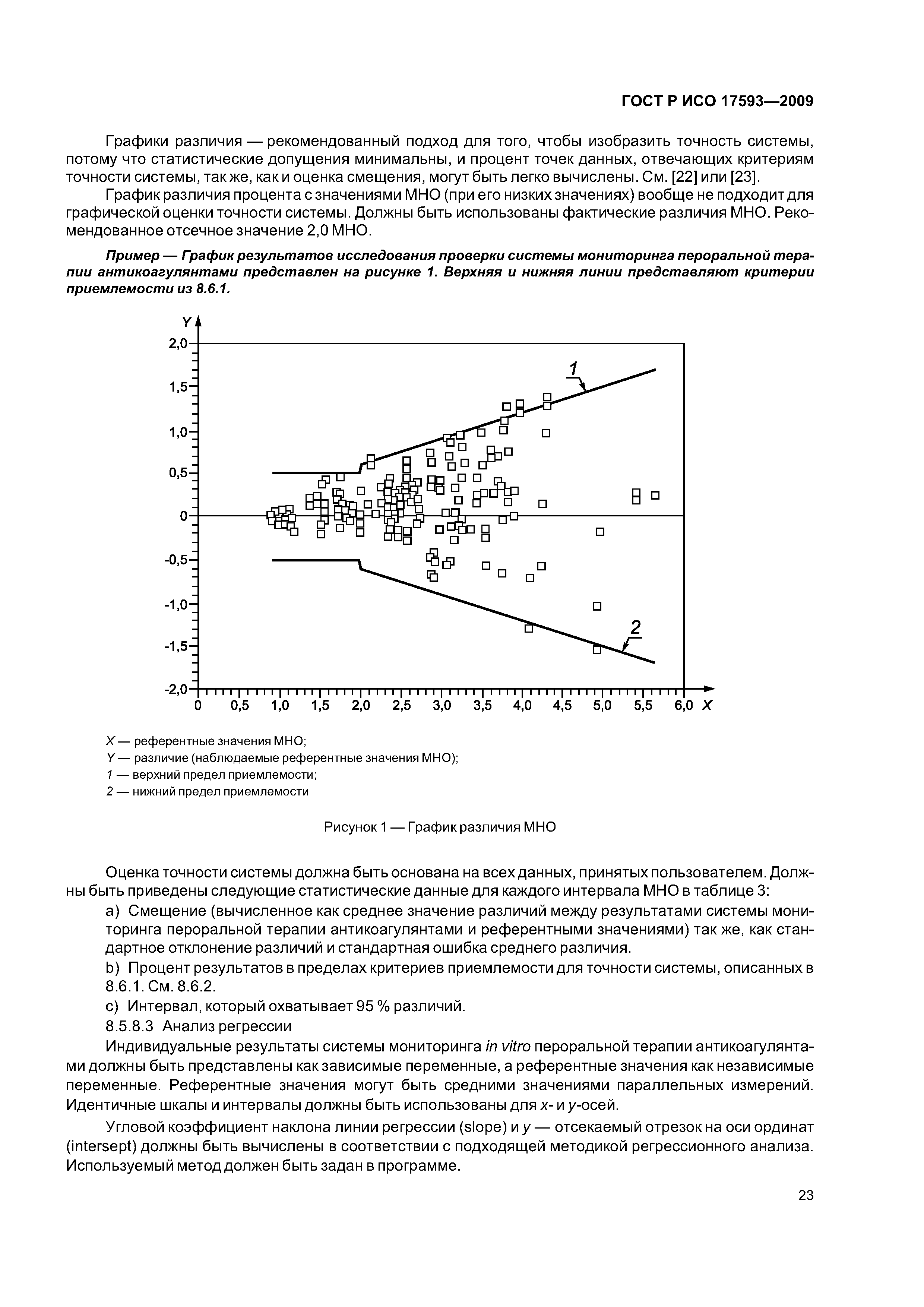
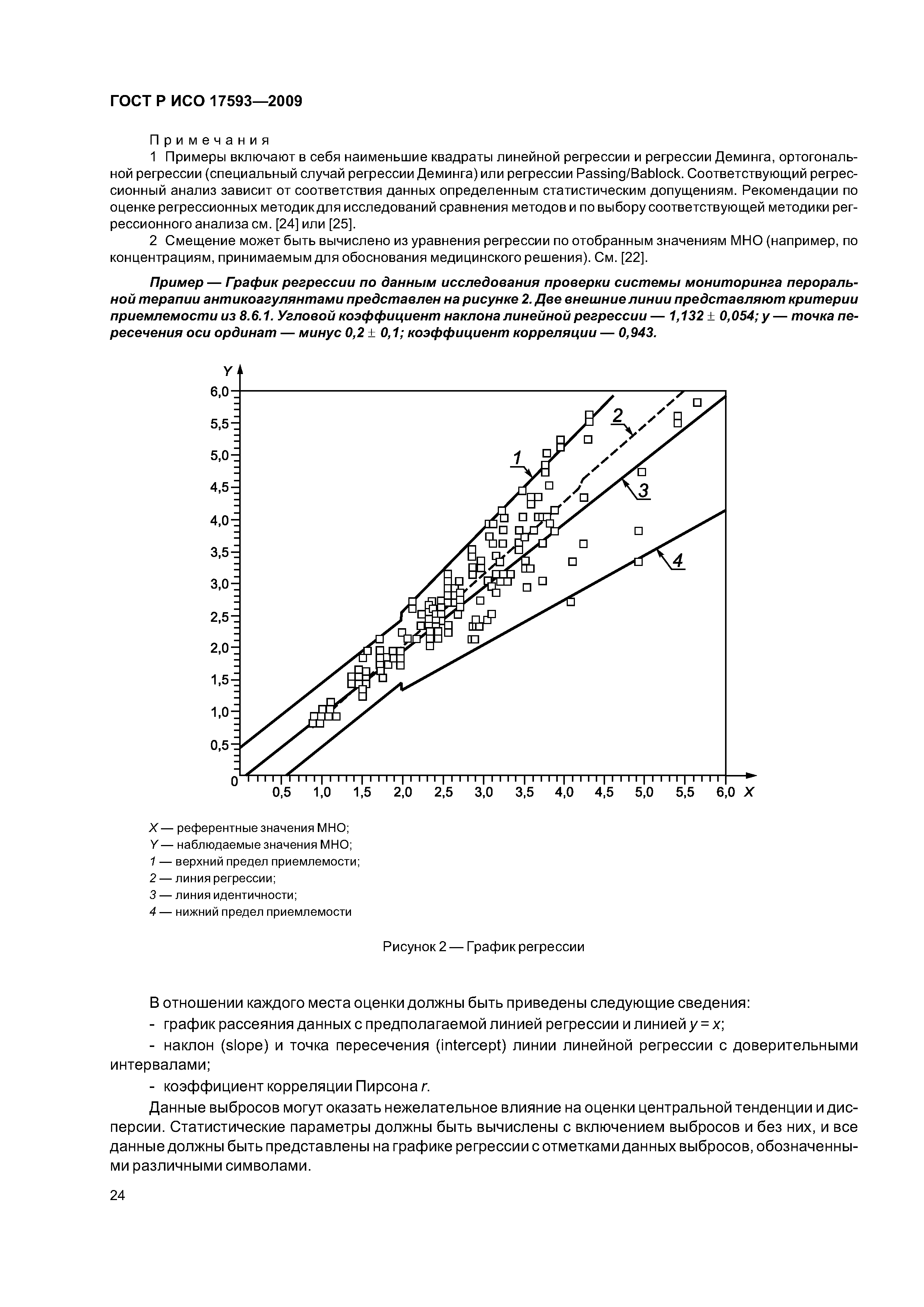
| Область применения: | Стандарт устанавливает требования к измерительным системам in vitro для самоконтроля лечения антагонистами витамина К, включая рабочие характеристики, обеспечение качества и обучение пользователей и методики верификации и валидации качества выполнения предполагаемыми пользователями при фактических и моделируемых условиях использования. Стандарт относится исключительно к системам измерения протромбинового времени, используемым людьми для контроля самостоятельного лечения антагонистами витамина K, и представляющим результаты как международное нормализованное отношение. Стандарт применим к изготовителям таких систем и к другим организациям (например, регулирующие органы и организации, оценивающие соответствие), ответственным за оценку работы данных систем. Действие стандарта не распространяется на: - измерительные системы in vitro для характеристик свертывания крови, оценивающих терапию антагонистами витамина K, используемых врачами или другими работниками здравоохранения; - всестороннюю оценку всех возможных факторов, которые могут повлиять на работу данных систем или - медицинские аспекты пероральной терапии антикоагулянтами. |
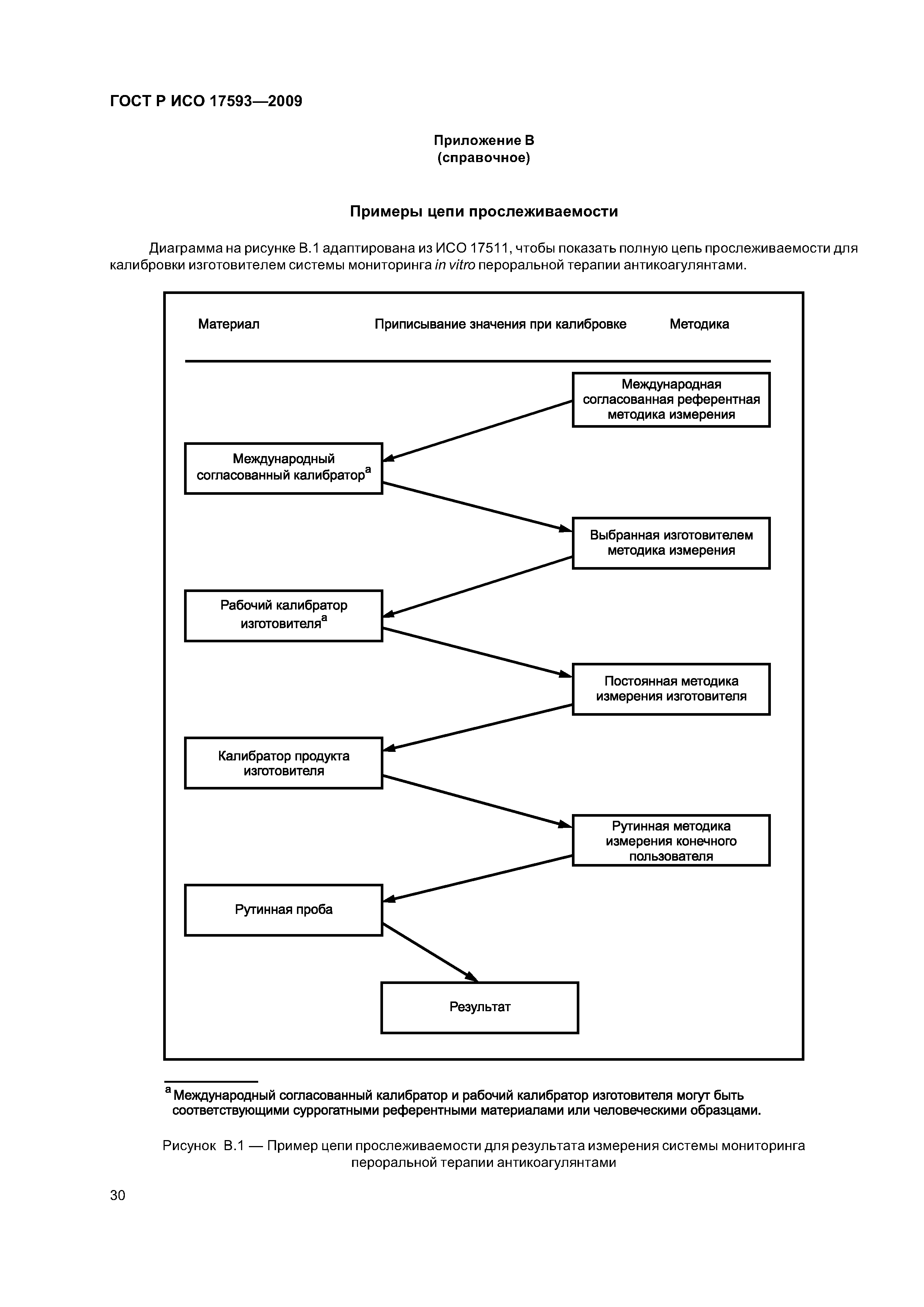
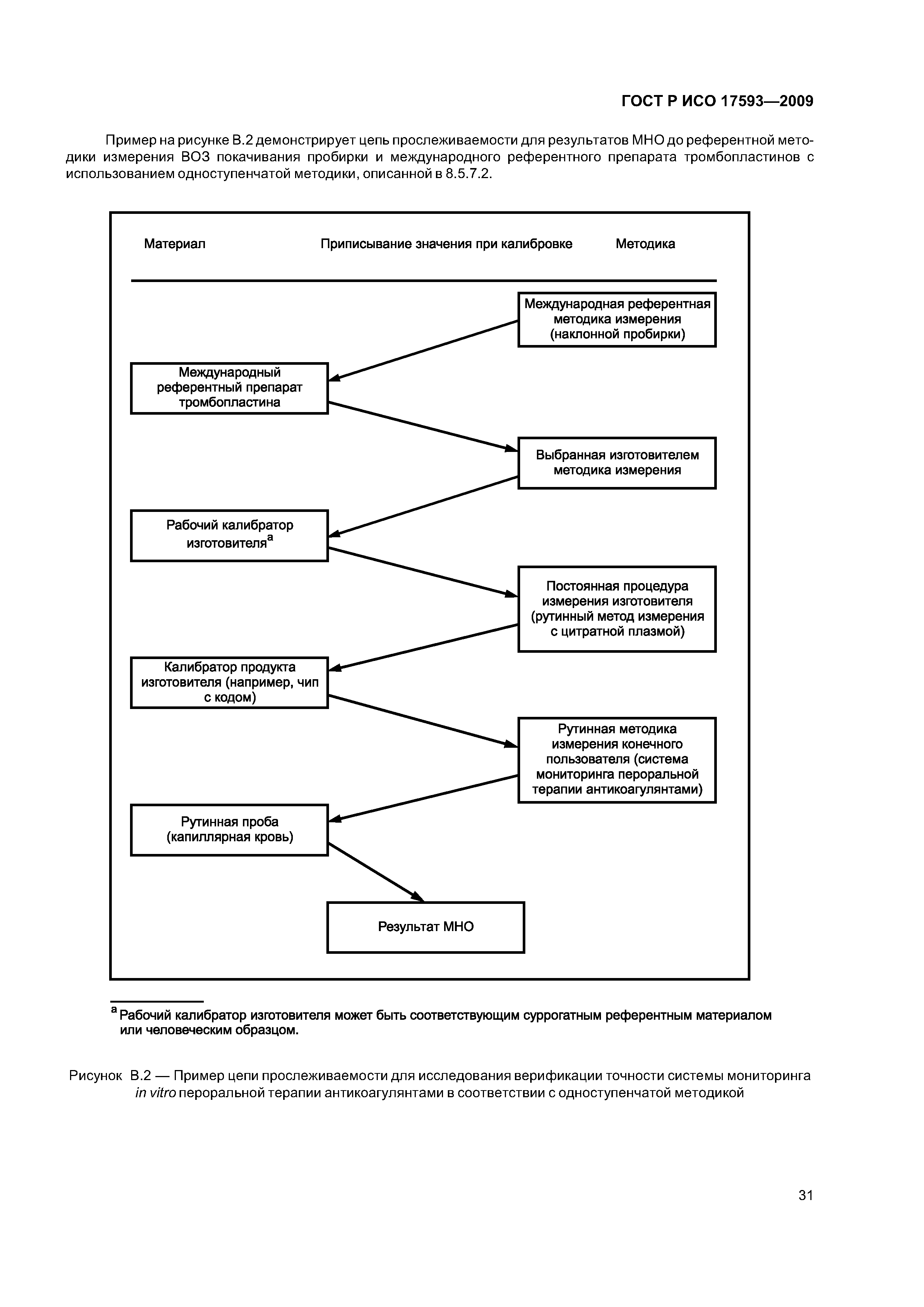
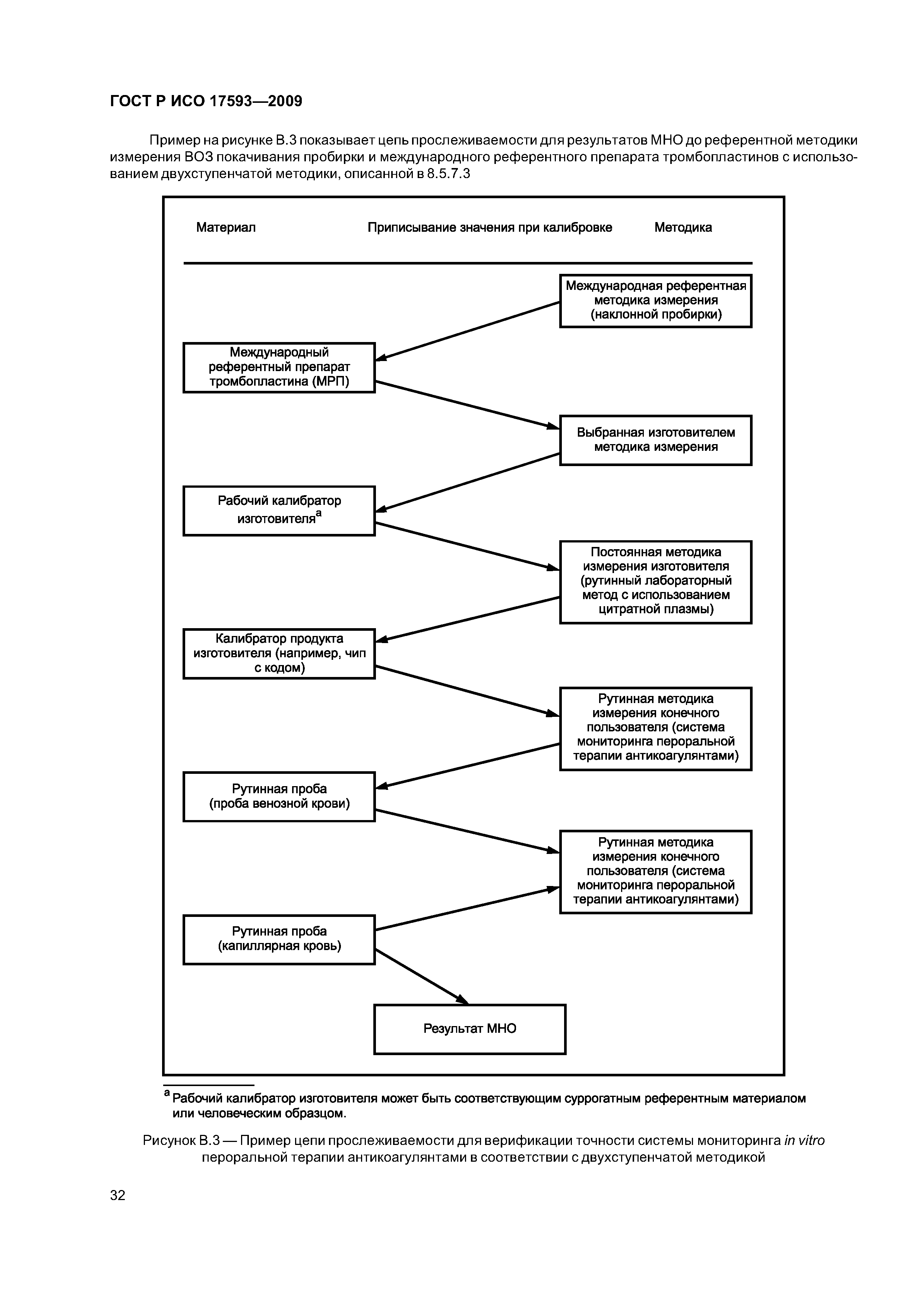
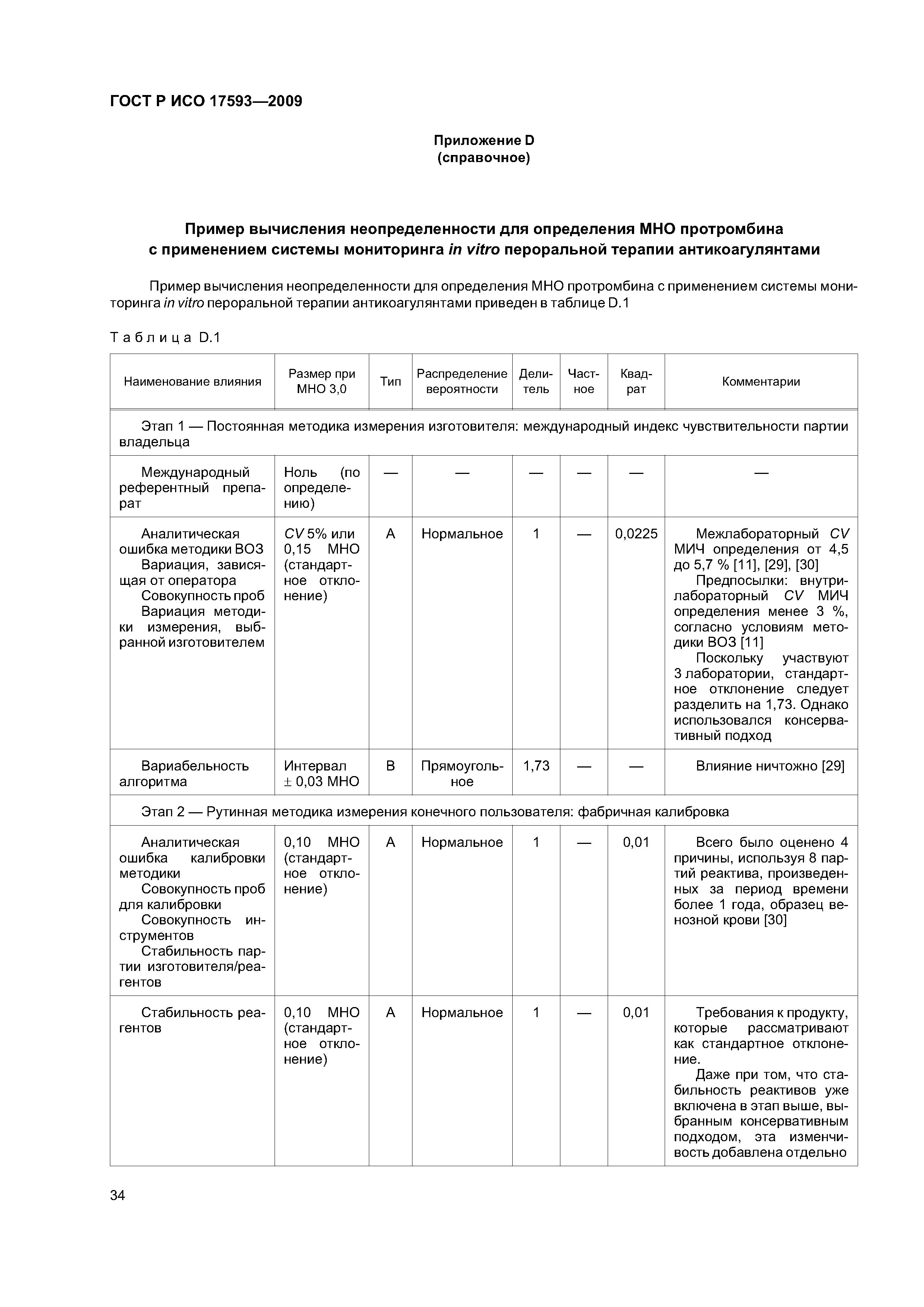
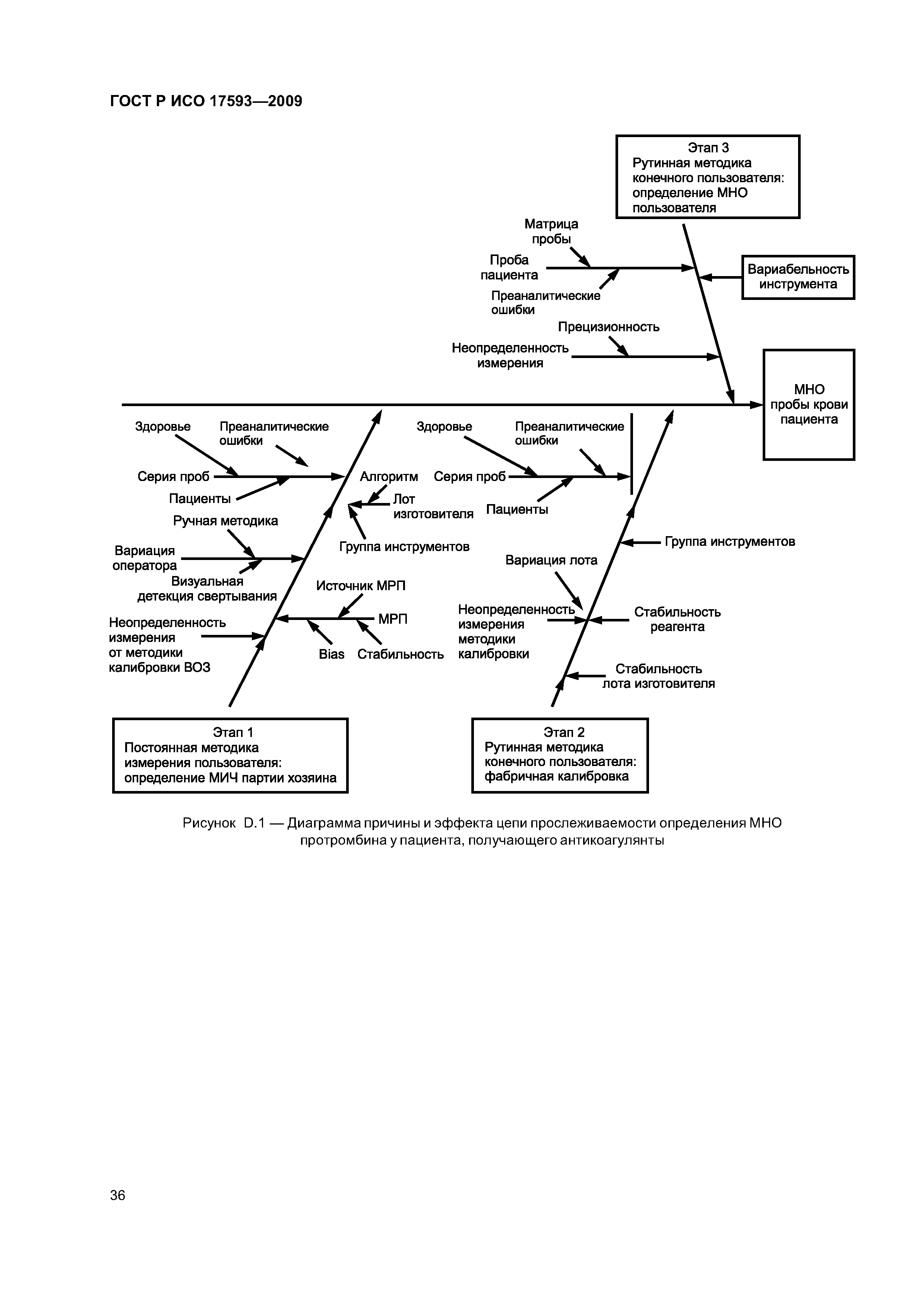
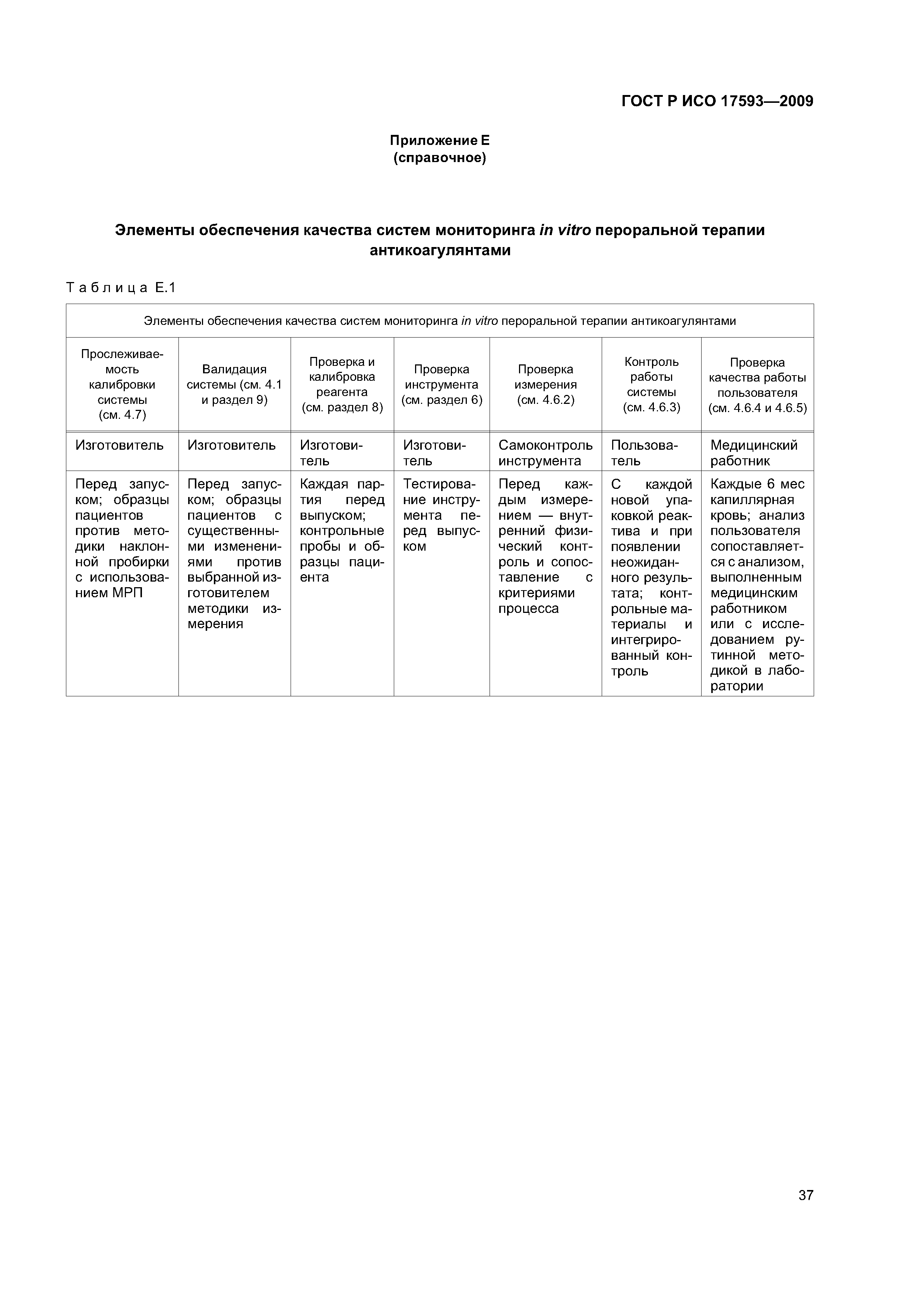
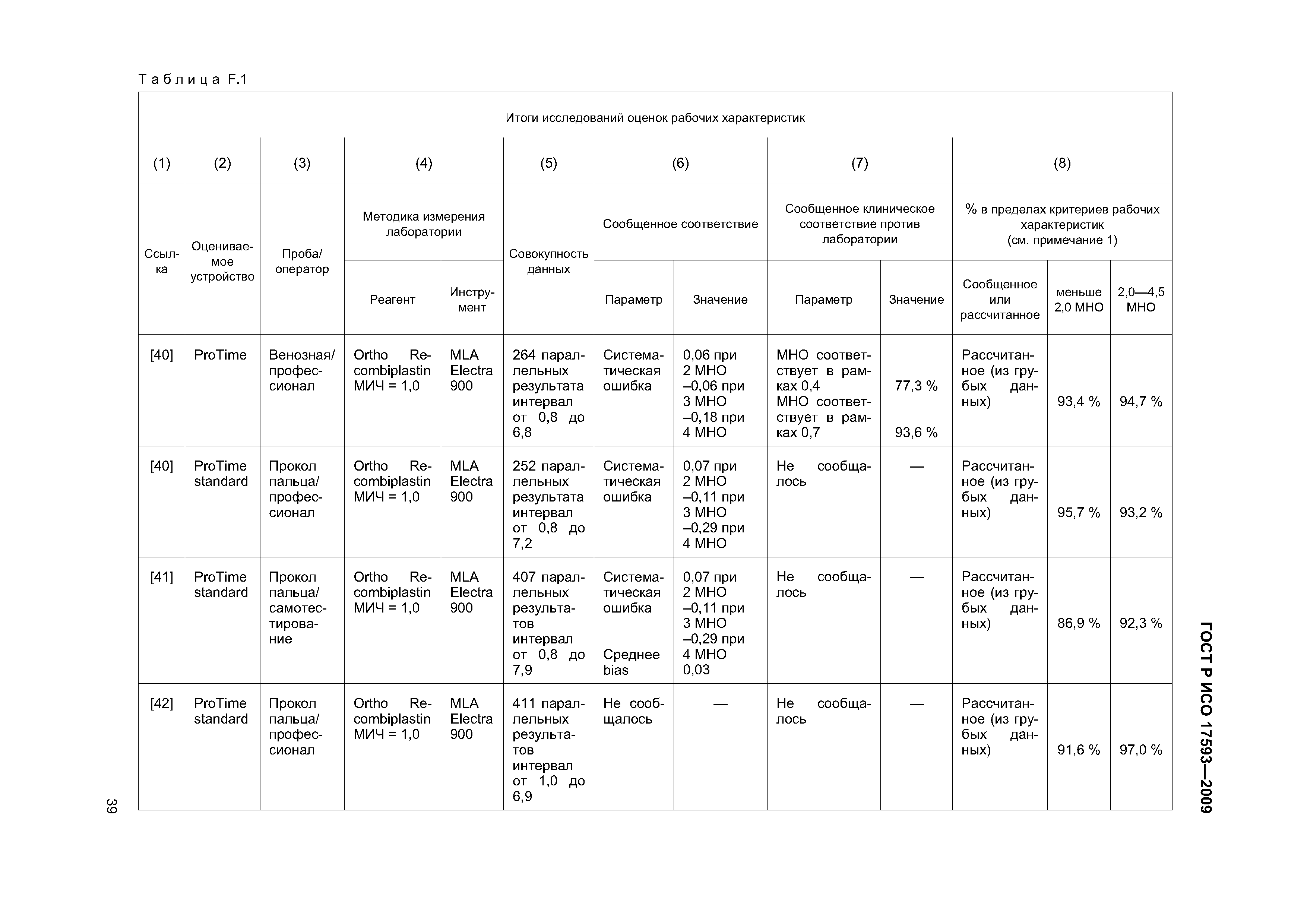
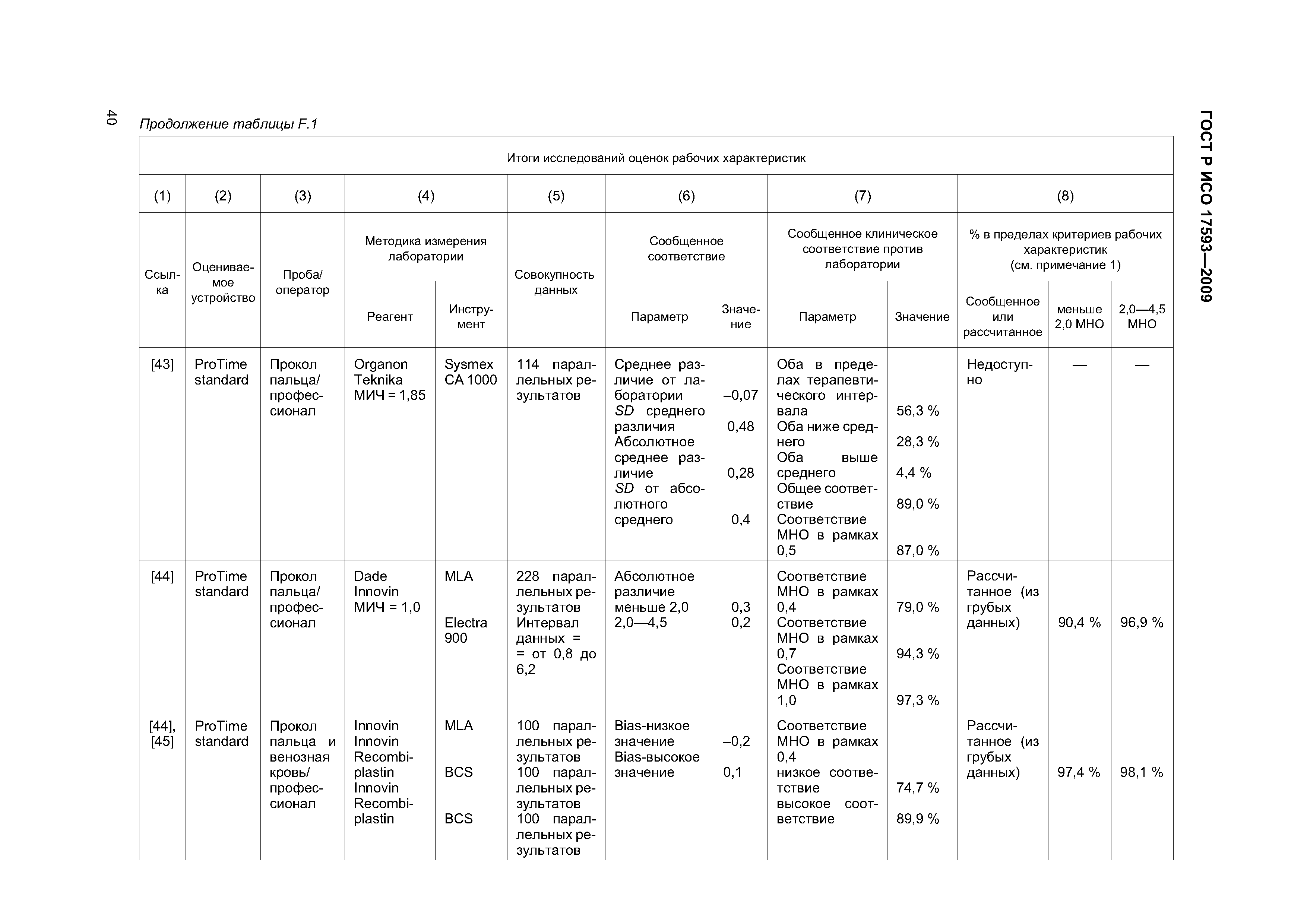
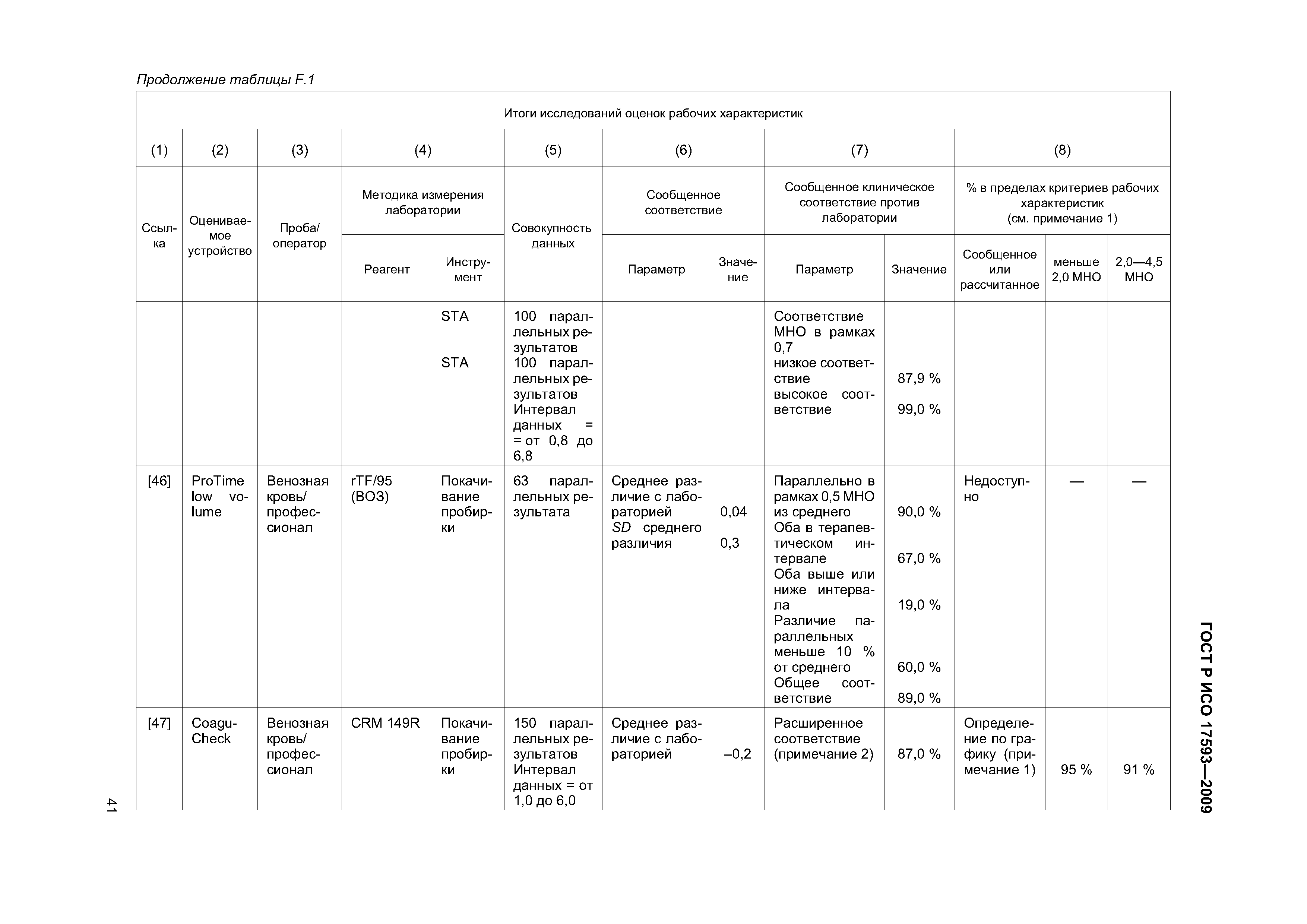
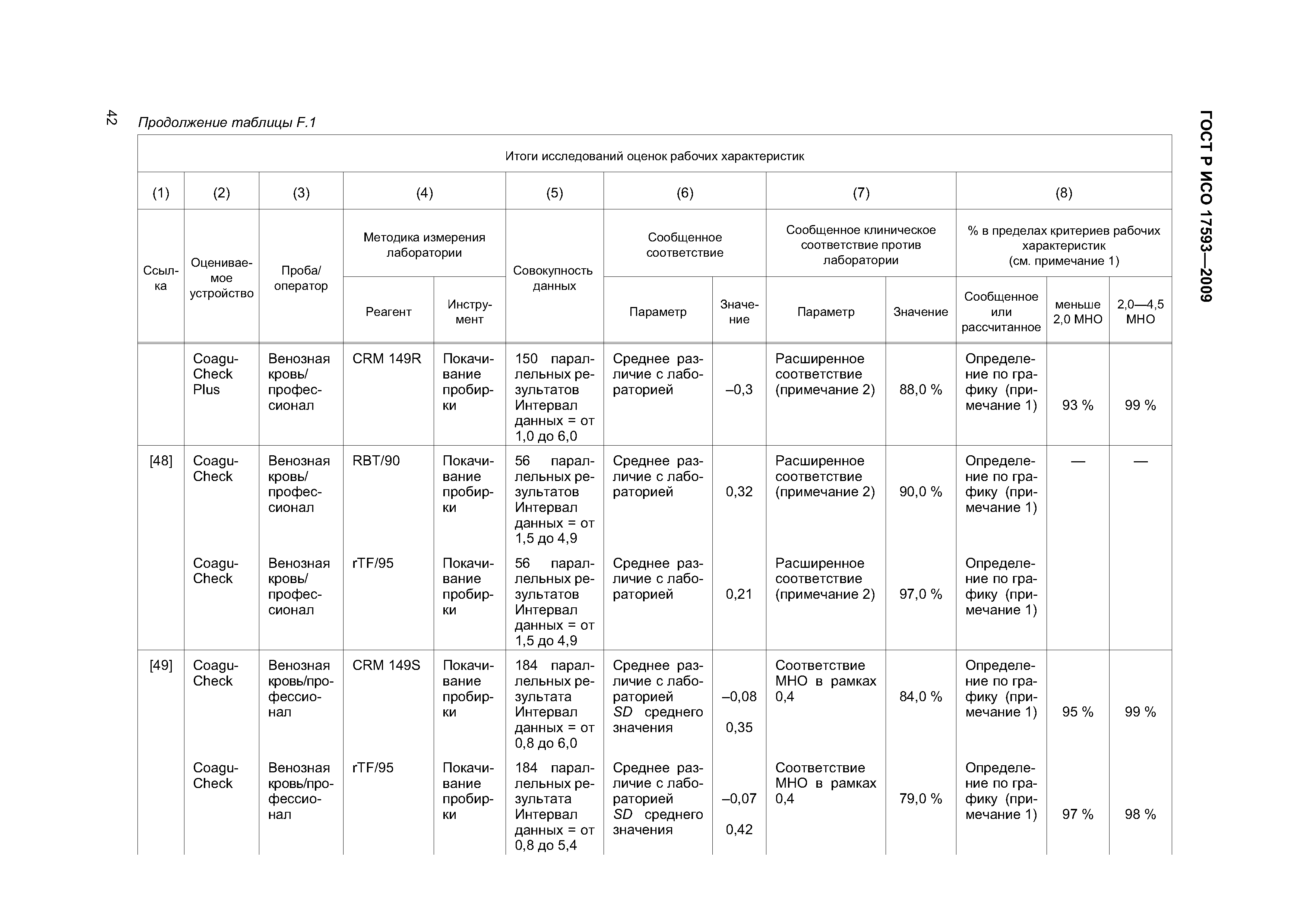
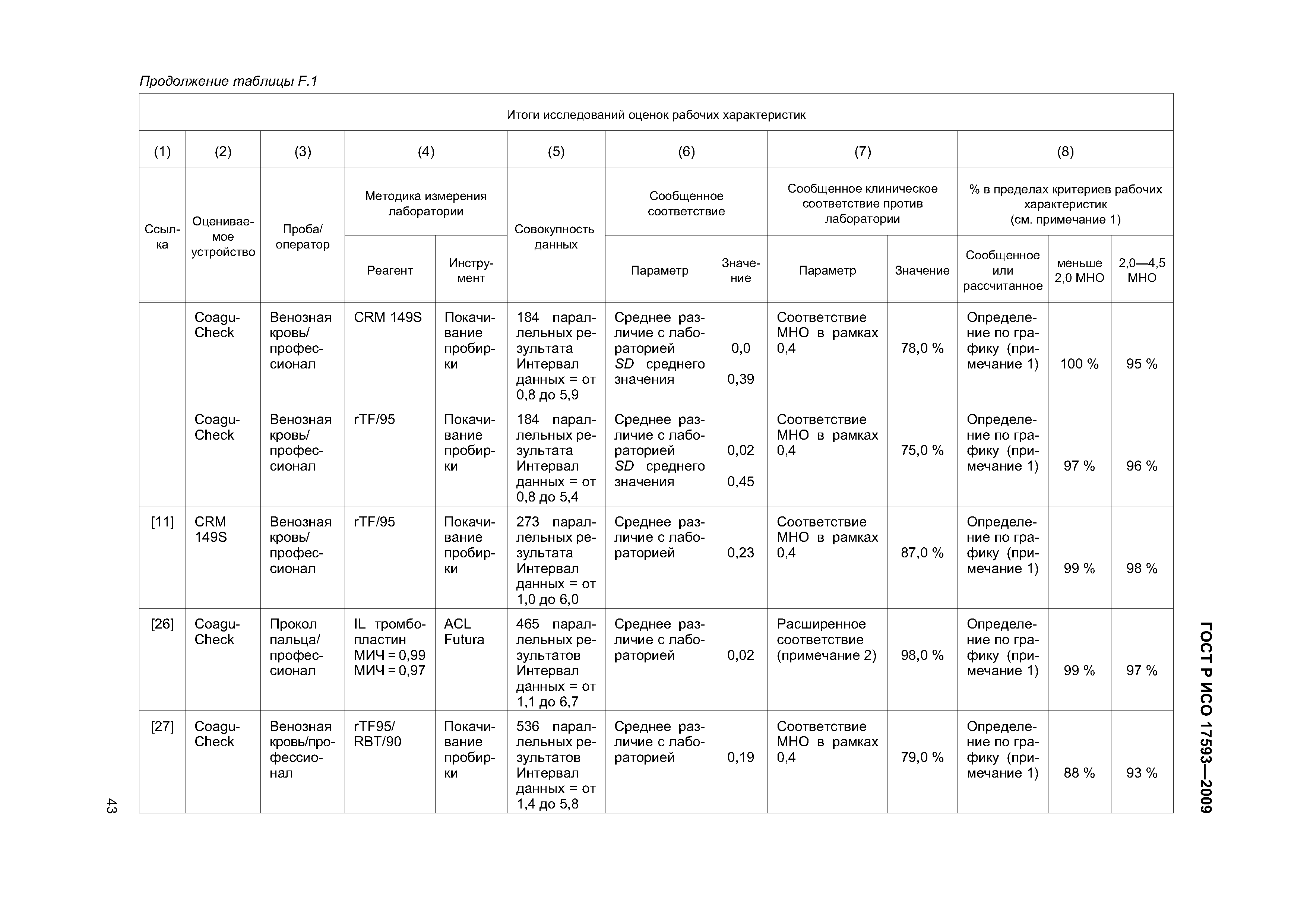
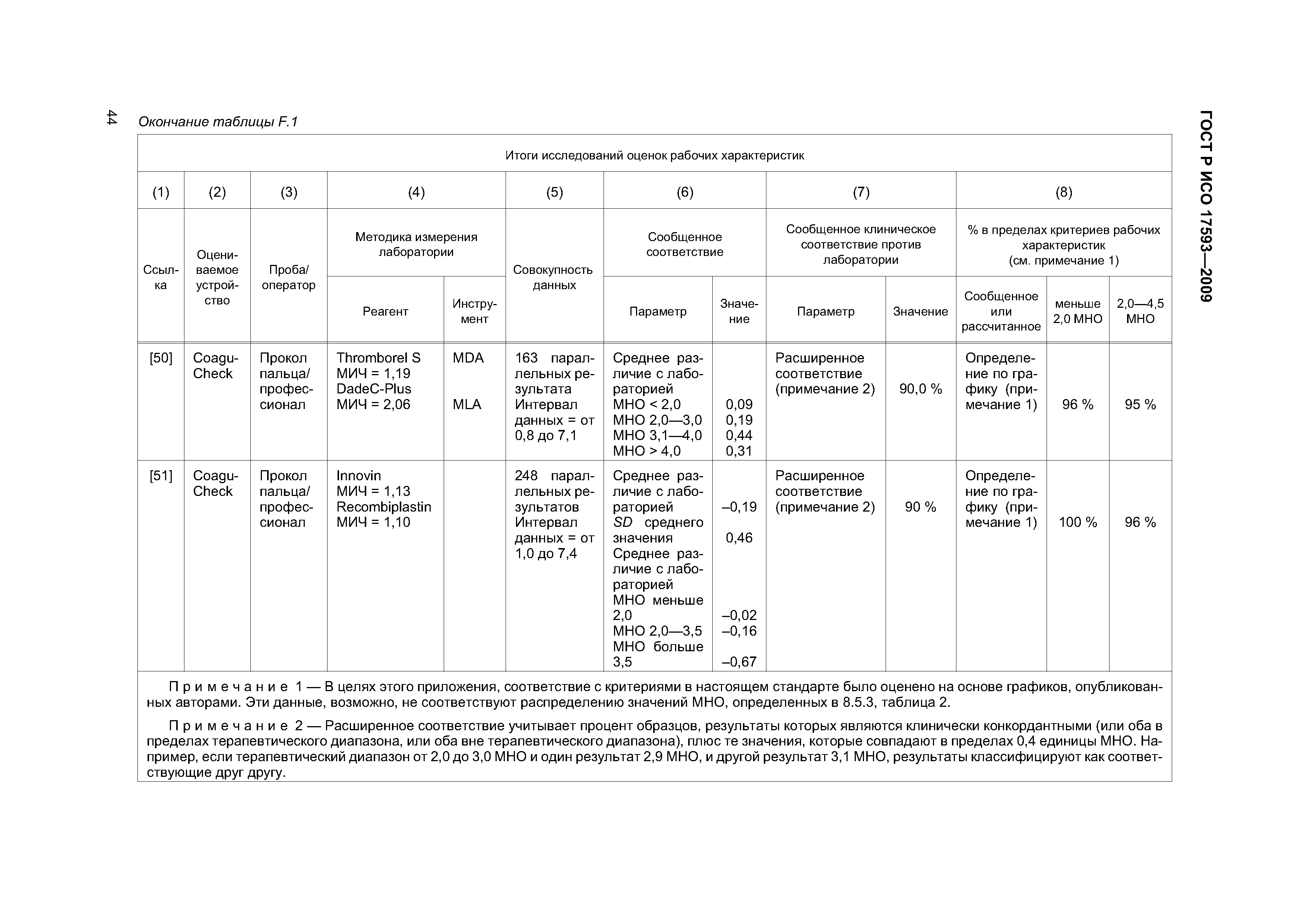
| Оглавление: | 1 Область применения 2 Нормативные ссылки 3 Термины и определения 4 Проектирование и развитие 4.1 Общие требования 4.2 Интервал измерения 4.3 Безопасность 4.4 Менеджмент риска 4.5 Аспекты эргономического и человеческого факторов 4.6 Обеспечение качества и средства контроля риска 4.7 Метрологическая прослеживаемость 5 Информация, поставляемая изготовителем 5.1 Общие требования 5.2 Маркировка инструмента для мониторинга in vitro пероральнои терапии антикоагулянтами 5.3 Инструкции по применению системы для мониторинга in vitro пероральнои терапии антикоагулянтами 5.4 Маркировка реактивов и контрольного материала 5.5 Инструкции по применению реактивов и контрольного материала 6 Испытание безопасности и надежности 6.1 Общие требования 6.2 Защита от удара током 6.3 Защита от механических опасностей 6.4 Электромагнитная совместимость 6.5 Тепловая резистентность 6.6 Сопротивление влажности и жидкостям 6.7 Защита от выделившихся газов, взрыва и имплозии 6.8 Компоненты устройства 6.9 Испытание рабочих характеристик 6.10 Механическая устойчивость против удара, вибрации и сдавления 6.11 Пределы воздействия температуры 6.12 Программа испытания воздействия влажностью 6.13 Испытание хранения и использования реактивов 7 Программы обучения и образования 7.1 Обучение медицинских работников 7.2 Обучение пациентов и других пользователей 8 Проверка рабочих характеристик системы 8.1 Общие положения 8.2 Вклады в неопределенность измерения 8.3 Проверка рабочих характеристик системы 8.4 Проверка прецизионности измерения 8.5 Проверка точности системы 8.6 Минимальная приемлемая точность системы 9 Оценка работы пользователя 9.1 Общие положения 9.2 Места исследования 9.3 Участники исследования 9.4 Инструменты и материалы 9.5 Оценка умений пользователей 9.6 Критерии приемлемости и оценка данных 9.7 Оценка инструкций по применению Приложение А (обязательное) Дополнительные требования для электромагнитной совместимости Приложение В (справочное) Примеры цепи прослеживаемости Приложение С (справочное) Вычисление размера пробы для оценки смещения [28] Приложение D (справочное) Пример вычисления неопределенности для определения MHO протромбина с применением системы мониторинга in vitro пероральной терапии антикоагулянтами Приложение Е (справочное) Элементы обеспечения качества систем мониторинга in vitro пероральной терапии антикоагулянтами Приложение F (справочное) Применение критериев рабочих характеристик к опубликованным оценкам систем мониторинга in vitro пероральной терапии антикоагулянтами Приложение G (справочное) Сведения о соответствии национальных стандартов Российской Федерации ссылочным международным (региональным) стандартам Библиография |
| Разработан: | Лаборатория проблем клинико-лабораторной диагностики ГОУ ВПО Московской медицинской академии им. И.М. Сеченова |
| Утверждён: | 09.12.2009 Федеральное агентство по техническому регулированию и метрологии (612-ст) |
| Издан: | Стандартинформ (2010 г. ) |
| Расположен в: | |
| Нормативные ссылки: |
|







































© 2013 Ёшкин Кот :-) Карта сайта
 ГОСТ Р 51317.4.2-99 «Совместимость технических средств электромагнитная. Устойчивость к электростатическим разрядам. Требования и методы испытаний»
ГОСТ Р 51317.4.2-99 «Совместимость технических средств электромагнитная. Устойчивость к электростатическим разрядам. Требования и методы испытаний»