|
| Обозначение: | ГОСТ Р 54421-2011 |
|
| Статус: | действующий |
|
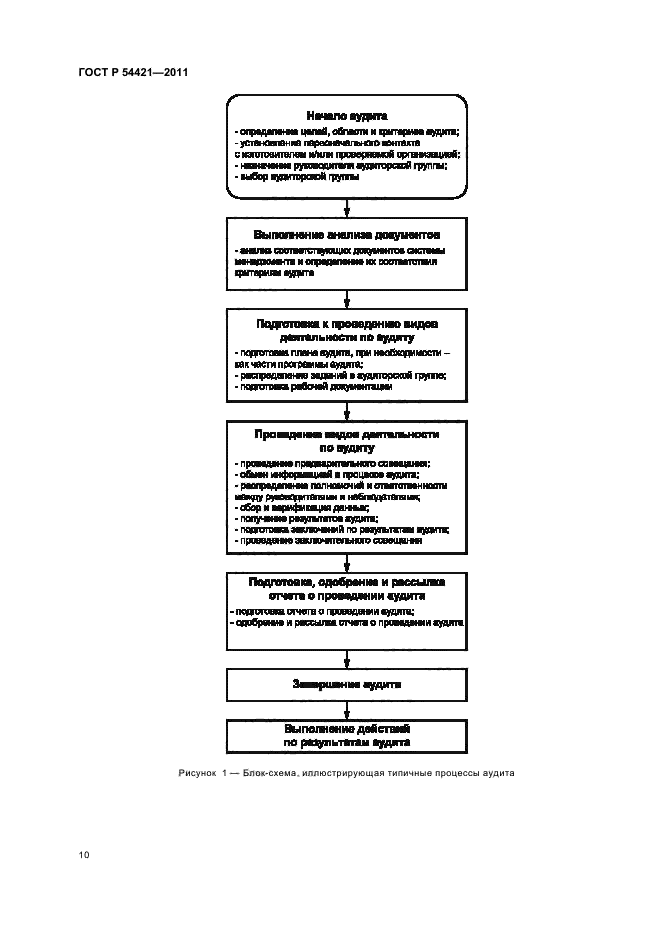
| Название рус.: | Руководство по аудиту систем менеджмента качества изготовителей медицинских изделий на соответствие регулирующим требованиям. Часть 1. Общие требования |
|
| Название англ.: | Guidelines for regulatory auditing of quality management systems of medical device manufacturers. Part 1. General requirements |
|
| Дата актуализации текста: | 01.08.2013 |
|
| Дата актуализации описания: | 01.08.2013 |
|
| Дата издания: | 19.09.2012 |
|
| Дата введения в действие: | 01.01.2013 |
|
| Дата последнего изменения: | 22.05.2013 |
|
| Область и условия применения: | Настоящий стандарт является руководством для организаций, проводящих аудиты и ответственных за разработку, планирование, проведение и документирование аудитов систем менеджмента качества изготовителей медицинских изделий. Настоящий стандарт охватывает также связанные с аудитом требования по проверке выполнения коррекций, корректирующих и предупреждающих действий, деятельности по улучшению, если это применимо. Кроме того, настоящий стандарт устанавливает критерии компетентности, которым должна соответствовать аудиторская группа |
|
| Расположен в: |
|
|