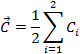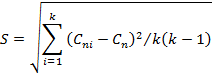| Информационная система |  |
4.1. Методы контроля. Химические факторы
Методические указания МУК 4.1.667-97
«Хромато-масс-спектрометрическое определение концентраций
фенолов и хлорпроизводных в воде»
(утв. Главным государственным санитарным врачом РФ 19 июня 1997 г.)
Дата введения - с момента утверждения
Введены впервые
СОДЕРЖАНИЕ
1. Назначение и область применения
Настоящие методические указания устанавливают хромато-масс-спектрометрическую методику количественного химического анализа проб питьевой и поверхностной (источниках питьевой) воды для определения в них фенола, 2-хлорфенола, 4-хлорфенола в диапазоне концентраций от 0,0005 до 0,1 мг/дм3, 2,4-дихлорфенола, 2,6-дихлорфенола, 2,4,5-трихлорфенола, 2,3,4,5-тетрахлорфенола - от 0,001 до 0,1 мг/дм3, о-крезола, п-крезола, 2,4,6-трихлорфенола - от 0,002 до 0,2 мг/дм3, п-нитрофенола - от 0,01 до 0,2 мг/дм3, пирокатехина, резорцина - от 0,05 до 1,0 мг/дм3, гваякола, 2,6-ксиленола - от 0,1 до 1,0 мг/дм3.
Определению каждого из соединений в указанном диапазоне концентраций не мешает присутствие других замещенных фенолов.
Методические указания могут быть использованы для определения замещенных фенолов в воде в условиях чрезвычайных и послеаварийных ситуаций.
2. Нормы погрешности измерений
Методика обеспечивает выполнение измерений фенола и хлорированных фенолов при доверительной вероятности 0,95 с погрешностью, не превышающей 25 %, гваякола и 2,4,5-трихлорфенола 28 %.
3. Физико-химические свойства и гигиенические
нормативы измеряемых веществ
Сведения о физико-химических свойствах замещенных фенолов и гигиенические нормативы приведены в табл. 1.
4. Метод измерений
4.1. Измеренный объем пробы воды 1,0 дм3 трижды экстрагируют хлористым метиленом при рН ≤ 2, используя делительную воронку. Экстракт хлористого метилена высушивают, концентрируют и анализируют методом хромато-масс-спектрометрии.
Нижний предел обнаружения измеряемых веществ - 0,001 мкг, гваякола, 2,6-ксиленола, пирокатехина, резорцина - 0,025 мкг.
Продолжительность проведения анализа составляет 50 мин.
4.2. Качественную идентификацию соединений осуществляют, основываясь на временах удерживания и относительной интенсивности одного основного и двух подтверждающих ионов (m/z). Количественное определение идентифицированного соединения выполняют методом «внешнего стандарта» по фенолу, относительно которого предварительно определяют градуировочный поправочный коэффициент (F), показывающий, во сколько раз отклик масс-спектрометрического детектора (площадь хроматографического пика, соответствующая выбранным для данного конкретного соединения ионам m/z) на единицу содержания вещества отличается от отклика масс-спектрометрического детектора на единицу содержания фенола.
4.3. Мешающие факторы могут быть связаны с загрязнением растворителей, реагентов, стекла, металлических предметов, что ведет к появлению посторонних пиков и/или возрастанию линии фона на профиле полного ионного тока. Все эти материалы должны быть свободными от данных проявлений в условиях анализа холостых проб.
Свойства веществ и их гигиенические нормативы
|
Вещество |
Формула |
Мол. масса |
Тквп, °C |
Плотность, г/см3 |
Растворимость, (г/см3) |
ПДК, г/см3 |
Класс опасности |
||
|
вода |
этанол |
эфир |
|||||||
|
Фенол |
C6H6O |
94 |
181,8 |
1,0576 |
67 |
х.р. |
х.р. |
0,001 |
4 |
|
2-Хлорфенол |
С6Н5OCl |
128 |
175 |
1,235 |
28,5 |
р. |
р. |
0,001 |
4 |
|
о-Крезол (2-метилфенол) |
C7H8O |
108 |
190,9 |
1,0465 |
30 |
х.р. |
х.р. |
0,05 |
2 |
|
п-Крезол (4-метилфенол) |
C7H8O |
108 |
202,5 |
1,0347 |
24 |
р. |
р. |
0,04 |
2 |
|
Гваякол (2-метоксифенол) |
C7H8O2 |
124 |
205 |
1,1287 |
16 |
р. |
р. |
- |
- |
|
2,6-Ксиленол (2,6-диметилфенол) |
C8H10O |
122 |
212 |
1,076 |
|
р. |
х.р. |
0,25 |
4 |
|
2,4-Дихлорфенол |
С6Н4ОCl2 |
162 |
209 |
|
4,6 |
р. |
р. |
0,002 |
4 |
|
4-Хлорфенол |
С6Н5OCl |
128 |
220 |
1,265 |
27,1 |
х.р. |
х.р. |
0,001 |
4 |
|
2,6-Дихлорфенол |
С6Н4OCl2 |
162 |
218 |
|
|
х.р. |
х.р. |
- |
- |
|
Пирокатехин (1,2-диоксибензол) |
C6H6O2 |
110 |
245,9 |
1,1493 |
450 |
х.р. |
р. |
0,1 |
4 |
|
Резорцин (1,3-диоксибензол) |
C6H6O2 |
110 |
280,8 |
1,285 |
2290 |
2430 |
х.р. |
0,1 |
4 |
|
2,4,6-Трихлорфенол |
C6H3OCl3 |
196 |
246 |
|
0,8 |
р. |
р. |
0,004 |
4 |
|
2,4,5-Трихлорфенол |
C6H3OCl3 |
196 |
248 |
|
|
|
|
- |
- |
|
п-Нитрофенол (4-нитрофенол) |
C6H5NO3 |
139 |
279 |
1,479 |
16 |
1895 |
1190 |
0,02 |
2 |
|
2,3,4,5-Тетрахлорфенол |
C6H2OCl4 |
230 |
|
|
|
|
|
- |
- |
5. Средства измерения, вспомогательные
устройства, материалы, реактивы
При выполнении измерений применяются следующие средства измерений, вспомогательные устройства, материалы и реактивы.
5.1. Средства измерений
|
Хромато-масс-спектрометр МАТ-90 фирмы «Finnigan MAT» (США, ФРГ), состоящий из: |
|
|
- масс-спектрометра высокого разрешения с двойной фокусировкой МАТ-90; |
|
|
- газового хроматографа Varian 3400, оснащенного кварцевой капиллярной хроматографической колонкой DB-5 фирмы J&W Scientific (США) длиной 30 см и внутренним диаметром 0,25 мм с нанесенной жидкой 5 %-ой фенил- и 95 %-ой метилсиликоновой фазой и толщиной пленки неподвижной фазы 0,25 мкм или ей аналогичной; |
|
|
- компьютера Micro VIP 2, соединенного с принтером Printronix MVP. |
|
|
Микрошприцы для хроматографии фирмы «Hamilton» вместимостью 0,001 и 0,01 см3 или аналогичные |
|
|
Весы аналитические лабораторные типа ВЛА-200 или аналогичные |
ГОСТ 24104-80Е |
|
Меры массы |
|
|
Цилиндры мерные типа 2-100, 2-1000 |
|
|
Пипетки стеклянные вместимостью 0,1, 1,0, 2,0 и 10 см3 1-го или 2-го класса точности |
|
|
Колбы мерные 2-10-2, 2-50-2, 2-100-2, 2-1000-2 |
|
|
Стандартные образцы состава замещенных фенолов с погрешностью аттестации ±2 % АОЗТ «ЭКРОС» |
|
|
Стандартные образцы состава хлорированных фенолов в метаноле с концентрацией 0,5 мг/см3 и погрешностью аттестации не более ±1, АОЗТ «ЭКРОС» |
|
|
Стандартные образцы состава хлорированных фенолов в ацетонитриле с концентрацией 0,4 мг/см3 и погрешностью аттестации не более ±2 %, НПО «МС-АНАЛИТИКА» |
|
5.2. Вспомогательные устройства
|
Контейнеры для отбора проб - емкости из темного стекла, объемом 1 дм3, снабженные завинчивающейся крышкой с тефлоновой прокладкой. В случае отсутствия темной посуды образец следует защитить от света. Контейнер должен быть чистым, его нужно прополоскать ацетоном или хлористым метиленом и высушить перед использованием. |
|
|
Воронки делительные ВД 3-1000 или аналогичные |
ГОСТ 9613-75 |
|
Колбы круглодонные К-1-100-29/32 ТХС |
|
|
Колбы выпаривательные КнКШ-100 и КнКШ-10 |
ГОСТ 10394-72 |
|
Баня водяная |
ТУ 61-423-72 |
|
Секундомер СДС пр. 1-2-000 |
ГОСТ 5072-79 |
|
Термометр ТЛ-4 4-Б 2 или ТЛ-2 1-Б 2 |
|
|
Электроплитка |
|
|
Шкаф сушильный электрический 2И-151 |
|
5.3. Материалы и реактивы
|
Кислота серная концентрированная марки ч. |
|
|
Натрий сернокислый безводный марки х.ч. |
|
|
Калий двухромовокислый марки х.ч. |
|
|
Вода дистиллированная |
ГОСТ 2709-72 |
|
Ацетон марки ч.д.а. |
|
|
Ацетонитрил марки х.ч. для хроматографии |
ТУ 6-09-4326-76 |
|
Метанол для хроматографии марки ос.ч. |
ТУ 6-09-2192-85 |
|
Хлористый метилен марки для спектроскопии |
|
|
Гелий газообразный очищенный марки А |
ТУ 51-940-60 |
|
Поверхностно-активное вещество ОП-7 или аналогичное |
|
|
Универсальная индикаторная бумага фирмы «Лахема» (Чехия) или аналогичная |
|
6. Требования безопасности
6.1. При выполнении измерений концентрации хлорированных фенолов с использованием хромато-масс-спектрометра следует соблюдать правила электробезопасности в соответствии с ГОСТом 12.1.019-79 и инструкцией по эксплуатации хромато-масс-спектрометра.
6.2. При работе с реактивами следует соблюдать необходимые меры безопасности, установленные для работы с токсичными, едкими и легковоспламеняющимися веществами по ГОСТу 12.1.005-88 и ГОСТу 12.1.007-76.
6.3. Метанол - сильный, преимущественно нервный и сосудистый яд. В организм человека может поступать через дыхательные пути, неповрежденную кожу. Метанол относится в 3-му классу опасности (ПДКр.з. = 5 мг/м3). При работе с этим растворителем следует соблюдать меры безопасности в соответствии с ГОСТом 12.1.005-88 и ГОСТом 12.1.007-76.
6.4. Хлористый метилен является слабым наркотиком, вызывающим поражение внутренних органов, обладает раздражающим действием. Хлористый метилен относится к 3-му классу опасности (ПДКр.з. = 50 мг/м3) и при работе с этим растворителем следует соблюдать меры безопасности в соответствии с ГОСТом 12.1.007-76.
7. Требования к квалификации операторов
7.1. К обработке проб воды допускают лиц, имеющих квалификацию инженера-химика или техника-химика и опыт работы в химической лаборатории.
7.2. К выполнению измерений и обработке их результатов на хромато-масс-спектрометре допускают лиц, имеющих квалификационную группу по работе на установках с высоким напряжением не ниже четвертой, прошедших соответствующий курс обучения и знающих устройство и правила эксплуатации прибора.
8. Условия отбора проб воды
8.1. Отбор проб воды объемом не менее 1,0 дм3 осуществляют в соответствии с ГОСТом 17.1.505-85 в химически чистые емкости из темного стекла с притертыми крышками, предварительно промытые дистиллированной водой и высушенные в сушильном шкафу при температуре 150 °C. До экстракции пробы воды следует хранить в холодном месте при температуре 4 °C.
8.2. Для получения одного результата измерения отбирают две одинаковые пробы воды.
8.3. Срок хранения отобранных проб воды - не более 7 суток.
9. Условия измерений
9.1. Приготовление растворов и подготовку проб к анализу, согласно ГОСТу 15150-69, осуществляют в следующих условиях:
- температура окружающего воздуха (20 ± 10 °C);
- относительная влажность - не более 80 % при температуре 25 °C;
- атмосферное давление 630 - 800 мм рт. ст.
9.2. Выполнение измерений на хромато-масс-спектрометре проводят в условиях, рекомендуемых технической документацией к прибору и настоящими методическими указаниями.
10. Подготовка к выполнению измерений
и проведение измерений
Перед выполнением измерений проводят следующие работы: подготовку стеклянной посуды, приготовление градуировочных растворов, подготовку хромато-масс-спектрометра к работе, подготовку хроматографической колонки и установление градуировочных характеристик.
10.1. Подготовка посуды
Посуда, используемая для анализа, тщательно моется с поверхностно-активным моющим средством. После этого посуда замачивается на 3 - 4 часа в свежеприготовленном 3 %-ном растворе двухромовокислого калия в серной кислоте (0,5 г двухромовокислого калия на 100 см3 концентрированной серной кислоты) и отмывается в проточной водопроводной воде с последующим ополаскиванием дистиллированной водой. После высушивания в сушильном шкафу при температуре 150 °C отверстия в посуде закрывают притертыми крышками.
10.2. Приготовление 50 %-го (объемная доля)
раствора серной кислоты
В мерный стакан или мензурку объемом не менее 200 см3 помещают 50 см3 дистиллированной воды и медленно порциями при перемешивании добавляют 50 см3 концентрированной серной кислоты. После остывания приготовленный раствор осторожно переливают в мерную колбу объемом 100 см3.
10.3. Приготовление исходных растворов
замещенных фенолов
В качестве исходных растворов фенола и его хлорпроизводных используют стандартные растворы фенолов в метаноле с концентрацией 0,5 мг/см3 и растворы хлорированных фенолов в ацетонитриле с концентрацией 0,4 мг/см3. Срок хранения стандартных растворов - 6 месяцев.
При отсутствии стандартных растворов определяемых в воде компонентов, исходные растворы готовят из чистых веществ с массовой долей основного компонента не менее 98 %.
Для приготовления исходного раствора с концентрацией вещества 0,5 мг/см3 взвешивают на аналитических весах с погрешностью не более 0,2 мг по 50 мг замещенных фенолов и помещают в мерную колбу объемом 100 см3. Растворяют в подходящем растворителе (метаноле, ацетонитриле), доводя объем раствора до метки при температуре 20 °C. Срок хранения исходных растворов - 1 месяц.
10.4. Приготовление градуировочных растворов
Для получения градуировочных растворов исходный раствор фенола в метаноле с концентрацией 0,5 мг/см3 разбавляют метанолом в мерных колбах в 2,5, 5, 10, 50 и 500 раз.
Для получения градуировочного раствора фенола в метаноле № 1 пипеткой объемом 0,1 см3 отбирают 0,1 см3 исходного раствора фенола в метаноле с концентрацией 0,5 мг/см3 и помещают в мерную колбу объемом 50 см3. Добавляют метанол до метки.
Для получения градуировочного раствора фенола в метаноле № 2 пипеткой исходного раствора фенола в метаноле с объемом 1,0 см3 отбирают 1,0 см3 концентрацией 0,5 мг/см3 и помещают в мерную колбу объемом 50 см3. Добавляют метанол до метки.
Для получения градуировочного раствора фенола в метаноле № 3 пипеткой объемом 1,0 см3 отбирают 1,0 см3 исходного раствора фенола в метаноле с концентрацией 0,5 мг/см3 и помещают в мерную колбу объемом 10 см3. Добавляют метанол до метки.
Для получения градуировочного раствора фенола в метаноле № 4 пипеткой исходного раствора фенола в метаноле с объемом 2,0 см3 отбирают 2,0 см3 концентрацией 0,5 мг/см3 и помещают в мерную колбу объемом 10 см3. Добавляют метанол до метки.
Для получения градуировочного раствора фенола в метаноле № 5 пипеткой объемом 2,0 см3 дважды отбирают по 2,0 см3 исходного раствора фенола в метаноле с концентрацией 0,5 мг/см и помещают в мерную колбу объемом 10 см3. Добавляют метанол до метки.
Характеристики градуированных растворов фенола в метаноле № 1 - 5 приведены в табл. 2.
Характеристики градуировочных растворов фенола в метаноле
|
№ раствора |
Концентрация исходного раствора, мг/см3 |
Объем пипетки, см3 |
Объем колбы, см3 |
Концентрация фенола в градуировочном растворе, мг/см3 |
Погрешность приготовления раствора, % |
|
1 |
0,5 |
0,1 |
50 |
0,001 |
1,8 |
|
2 |
0,5 |
1,0 |
50 |
0,01 |
1,8 |
|
3 |
0,5 |
1,0 |
10 |
0,05 |
1,6 |
|
4 |
0,5 |
2,0 |
10 |
0,1 |
1,8 |
|
5 |
0,5 |
2,0 |
10 |
0,2 |
2,1 |
Все колбы с исходным и градуировочными растворами оборачивают в темную бумагу и хранят в холодильнике при температуре 4 °C. Характеристики градуировочных растворов остаются постоянными в течение одного месяца.
10.5. Подготовка прибора к выполнению измерений
Включают хромато-масс-спектрометр МАТ-90 и компьютер Micro VIP 2 в соответствии с техническим описанием и руководством по эксплуатации приборов. Прибор выходит на нормальный режим работы через 24 часа.
Газохроматографическую колонку хроматографа Varian 3400 кондиционируют при температуре 150 °C в течение 12 часов с предварительным медленным нагревом от температуры 50 °C со скоростью 1 °С/мин.
10.6. Условия хроматографирования и записи масс-спектров
Разделение замещенных фенолов на газовом хроматографе проводят в следующем режиме программирования температуры колонки: 50 °C - 1 мин, в интервале 50 - 250 °C со скоростью 10 °С/мин, 250 °C - 10 мин; температура инжектора 200 °C; без деления потока с последующей продувкой растворителя; расход газа-носителя (гелия) - 1 мл/мин.
Масс-спектры электронного удара органических соединений получают при энергии ионизирующих электронов 70 эВ и температуре ионизационной камеры 200 °C. Диапазон сканирования масс 35 - 250 m/z, скорость сканирования 1,0 сек/декада. Идентификацию индивидуальных соединений осуществляют при помощи библиотечного поиска в библиотеке NBS компьютера масс-спектрометра и по временам удерживания.
Хроматографические и масс-спектрометрические характеристики фенола и его производных приведены в табл. 3.
Хроматографические и масс-спектрометрические характеристики
определяемых веществ
|
№ п/п |
Вещество |
Время удерживания, мин:сек |
Характеристические массы, m/z |
|
|
Основной ион |
Подтверждающие ионы |
|||
|
1 |
Фенол |
6:42 ± 0:02 |
94 |
65,66 |
|
2 |
2-Хлорфенол |
6:49 ± 0:02 |
128 |
64,130 |
|
3 |
о-Крезол |
7:53 ± 0:01 |
108 |
77,107 |
|
4 |
п-Крезол |
8:14 ± 0:01 |
108 |
77,107 |
|
5 |
Гваякол |
8:26 ± 0:01 |
124 |
81,109 |
|
6 |
2,6-Ксиленол |
8:44 ± 0:02 |
122 |
107,121 |
|
7 |
2,4-Дихлорфенол |
9:53 ± 0:03 |
162 |
98,164 |
|
8 |
4-Хлорфенол |
10:18 ± 0:02 |
128 |
65,130 |
|
9 |
2,6-Дихлорфенол |
10:23 ± 0:02 |
162 |
98,164 |
|
10 |
Пирокатехин |
10:39 ± 0:03 |
110 |
64,81 |
|
11 |
Резорцин |
12:02 ± 0:03 |
110 |
64,81 |
|
12 |
2,4,6-Трихлорфенол |
12:46 ± 0:01 |
196 |
198,200 |
|
13 |
2,4,5-Трихлорфенол |
12:53 ± 0:01 |
196 |
198,200 |
|
14 |
п-Нитрофенол |
15:35 ± 0:05 |
139 |
65,109 |
|
15 |
2,3,4,5-Тетрахлорфенол |
15:28 ± 0:01 |
232 |
230,234 |
10.7. Установление градуировочной характеристики и
градуировочных
поправочных коэффициентов
Для установления градуировочной характеристики используют не менее 5-ти серий градуировочных растворов фенола в метаноле, один из которых должен иметь концентрацию, близкую к нижней границе диапазона измеряемого содержания.
Каждую серию растворов анализируют не менее 6-ти раз в условиях хромато-масс-спектрометрического определения, как описано в п. 10.6.
На каждой масс-фрагментограмме по основному и двум подтверждающим ионам измеряют площадь пика в условных единицах и полученные значения заносят в табл. 4. По средним значениям из не менее чем 6-ти измерений устанавливают градуировочную характеристику зависимости площади хроматографического пика (усл. ед.) от содержания введенного в хроматограф фенола (мг/см3).
Аналогично получают градуировочные характеристики по стандартным растворам замещенных фенолов в метаноле (ацетонитриле). На масс-фрагментограммах по основному и двум подтверждающим ионам для каждого вещества измеряют площадь пика (в условных единицах), при соотношении сигнал/шум не менее 10:1 и результаты заносят в табл. 4.
Результаты градуировки прибора
|
№ градуировочного раствора |
№ анализа |
Содержание введенного вещества, мг/см3 |
Площадь хроматографического пика Q, усл. ед. |
Градуировочный поправочный коэффициент, F |
|
1 |
1 |
C11 |
Q11 |
F11 |
|
… |
… |
… |
… |
… |
|
… |
k |
C1k |
Q1k |
F1k |
|
… |
1 |
Cn1 |
Qn1 |
Fn1 |
|
… |
… |
… |
… |
… |
|
n |
k |
Cnk |
Qnk |
Fnk |
Для каждого определяемого вещества обрабатывают полученные данные следующим образом:
- рассчитывают значение i-го градуировочного поправочного коэффициента:
|
|
(1) |
Qi - площадь пика характеристических ионов определяемого вещества на i-ой масс-фрагментограмме, усл. ед.;
Qф - площадь пика характеристических ионов фенола на i-ой масс-фрагментограмме, усл. ед.;
Ci - концентрация определяемого вещества, мг/см3;
Сф - концентрация фенола, мг/см3;
- рассчитывают среднее значение градуировочного поправочного коэффициента:
|
|
(2) |
k - число результатов измерения для данного компонента.
- рассчитывают значение относительного среднего квадратического отклонения градуировочного поправочного коэффициента результата измерения SF, % для каждого компонента:
|
|
(3) |
Если выполняются условия:
|
SF ≤ 1/6×θ0, |
(4) |
то случайной погрешностью по сравнению со систематическими пренебрегают и принимают, что границы доверительной вероятности равны θ0. Если данные условия не выполняются, то градуировку проводят снова. Расчеты значений градуировочных коэффициентов Fn, относительных погрешностей результатов измерений θ0 и средних квадратических отклонений результатов измерений SF, представленных в табл. 5, приведены в приложении к методическим указаниям.
Градуировочные поправочные коэффициенты, относительные
погрешности и
средние квадратические отклонения результатов измерений содержания
фенолов и их хлорпроизводных
|
Вещество |
Градуировочный
поправочный коэффициент, |
Относительная погрешность θ0, % (с вероятностью 0,95) |
Среднее квадратическое отклонение SF, % |
|
Фенол |
1,0 |
25 |
2,9 |
|
2-Хлорфенол |
2,5 |
17 |
1,4 |
|
о-Крезол |
5,4 |
19 |
2,3 |
|
п-Крезол |
5,1 |
20 |
2,4 |
|
Гваякол |
11,7 |
28 |
3,1 |
|
2,6-Ксиленол |
12,6 |
17 |
1,9 |
|
2,4-Дихлорфенол |
3,6 |
15 |
1,0 |
|
4-Хлорфенол |
2,1 |
21 |
2,6 |
|
2,6-Дихлорфенол |
3,6 |
17 |
2,0 |
|
Пирокатехин |
5,0 |
20 |
2,4 |
|
Резорцин |
5,4 |
19 |
2,3 |
|
2,4,6-Трихлорфенол |
5,2 |
20 |
2,1 |
|
2,4,5-Трихлорфенол |
4,4 |
26 |
3,2 |
|
п-Нитрофенол |
28,5 |
21 |
2,6 |
|
2,3,4,5-Тетрахлорфенол |
5,3 |
21 |
2,3 |
10.8. Установление коэффициентов экстракции
Степень извлечения и коэффициенты экстракции замещенных фенолов устанавливают на градуировочных растворах веществ в воде.
Градуировочные растворы фенола, 2-хлорфенола, 4-хлорфенола готовят в мерных колбах вместимостью 1 дм3. Для этого в каждую колбу вносят 0,001, 0,01 и 0,1 см3 исходных растворов фенола, 2-хлорфенола, 4-хлорфенола с концентрацией 0,5 мг/см3, доводят объем дистиллированной водой до метки.
Градуировочные растворы 2,4-дихлорфенола, 2,6-дихлорфенола, 2,4,5-трихлорфенола, 2,3,4,5-тетрахлорфенола готовят в мерных колбах вместимостью 1 дм3. Для этого в каждую колбу вносят 0,002, 0,01 и 0,2 см3 исходных растворов 2,4-дихлорфенола, 2,6-дихлорфенола, 2,4,5-трихлорфенола, 2,3,4,5-тетрахлорфенола с концентрацией 0,5 мг/см3, доводят объем дистиллированной водой до метки.
Градуировочные растворы о-крезола, п-крезола, 2,4,6-трихлорфенола готовят в мерных колбах вместимостью 1 дм3. Для этого в каждую колбу вносят 0,004, 0,1 и 0,4 см3 исходных растворов о-крезола, п-крезола, 2,4,6-трихлорфенола с концентрацией 0,5 мг/см3, доводят объем дистиллированной водой до метки.
Градуировочные растворы п-нитрофенола готовят в мерных колбах вместимостью 1 дм3. Для этого в каждую колбу вносят 0,02, 0,1 и 1,0 см3 исходного раствора п-нитрофенола с концентрацией 0,5 мг/см3, доводят объем дистиллированной водой до метки.
Градуировочные растворы пирокатехина, резорцина готовят в мерных колбах вместимостью 1 дм3. Для этого в каждую колбу вносят 0,1, 1,0 и 2,0 см3 исходных растворов пирокатехина, резорцина с концентрацией 0,5 мг/см3, доводят объем дистиллированной водой до метки.
Градуировочные растворы гваякола, 2,6-ксиленола готовят в мерных колбах вместимостью 1 дм3. Для этого в каждую колбу вносят 0,2, 1,0 и 2,0 см3 исходных растворов гваякола, 2,6-ксиленола с концентрацией 0,5 мг/см3, доводят объем дистиллированной водой до метки.
Градуировочные растворы подвергают экстракции и анализу, как описано в п. 10.9, и рассчитывают содержание извлеченных из воды веществ, как описано в п. 11. Рассчитывают степень извлечения веществ из воды по формуле:
|
|
(5) |
и коэффициент экстракции по формуле:
|
Kэi = Ccp./Ci, где |
(6) |
Ci - концентрация вещества в экстракте, мг/дм3;
Сгр. - концентрация вещества в градуировочном растворе, мг/дм3.
Вычисляют среднее значение коэффициента экстракции для каждого вещества по формуле:
|
|
(7) |
Степень извлечения Z и коэффициенты экстракции Kэ веществ из воды приведены в табл. 6.
Степень извлечения и коэффициенты экстракции веществ
|
Вещество |
Степень извлечения, % |
Коэффициент экстракции |
|
Фенол |
80 |
1,25 |
|
2-Хлорфенол |
98 |
1,02 |
|
о-Крезол |
64 |
1,57 |
|
п-Крезол |
59 |
1,70 |
|
Гваякол |
62 |
1,62 |
|
2,6-Ксиленол |
65 |
1,54 |
|
2,4-Дихлорфенол |
83 |
1,21 |
|
4-Хлорфенол |
88 |
1,14 |
|
2,6-Дихлорфенол |
86 |
1,16 |
|
Пирокатехин |
54 |
1,86 |
|
Резорцин |
55 |
1,81 |
|
2,4,6-Трихлорфенол |
68 |
1,48 |
|
2,4,5-Трихлорфенол |
89 |
1,12 |
|
п-Нитрофенол |
59 |
1,73 |
|
2,3,4,5-Тетрахлорфенол |
94 |
1,06 |
10.9. Выполнение измерений
10.9.1. Экстракция проб воды в делительной воронке.
Емкость с пробой воды вскрывают, объем воды (1,0 дм3) замеряют с помощью мерного цилиндра вместимостью 1 дм3 и переливают в делительную воронку вместимостью 1 дм3, снабженную тефлоновым или хорошо притертым и смазанным только водой стеклянным краном. Добавляют пипеткой объемом 1 см3 50 %-ный раствор серной кислоты до значения pH в пробе воды ≤ 2. Значение pH устанавливают с помощью универсальной индикаторной бумаги.
В емкость из-под воды приливают замеренные цилиндром (100 см3) 20 см3 хлористого метилена, герметично закрывают и встряхивают в течение 30 секунд для промывки внутренней поверхности емкости. После этого данную порцию растворителя переносят в делительную воронку, в которой находится анализируемая проба воды. Экстракцию пробы воды проводят, встряхивая делительную воронку в течение 2 минут, периодически сбрасывая избыточное давление. После расслоения органической и водной фаз экстракт отделяют от воды и переносят в круглодонную колбу объемом 100 см3. Пробу воды последовательно экстрагируют еще два раза порциями по 20 см3 хлористого метилена как описано выше. Объединенные экстракты (60 см3) высушивают от воды, пропуская их через сухую пипетку вместимостью 10 см3, заполненную 10 г сернокислого натрия, и собирают в выпаривательной колбе объемом 100 см3. Для количественного переноса круглодонную колбу и пипетку, заполненную сернокислым натрием, промывают 10 см3 хлористого метилена, которые затем добавляют к экстракту в выпаривательной колбе.
В выпаривательную колбу помещают одну или две чистых «кипелки» и экстракт (70 см3) осторожно упаривают на водяной бане при температуре 60 - 65 °C до объема 5 - 8 см3 и переносят в выпаривательную колбу объемом 10 см3. Перенесенный экстракт упаривают дальше досуха. К сухому остатку пипеткой объемом 0,1 см3 добавляют 0,2 см3 (дважды по 0,1 см3) хлористого метилена и этот раствор подвергают хромато-масс-спектрометрическому анализу.
Экстрагирование проб воды и упаривание растворов проводят непосредственно перед хромато-масс-спектрометрическим измерением.
10.9.2. Анализ экстрактов методом хромато-масс-спектрометрии.
Вводят в инжектор хроматографа 0,001 см3 упаренного экстракта и осуществляют разделение смеси в условиях, указанных в п. 10.6.
Записывают хроматограммы в виде файлов данных. Для основного и двух подтверждающих ионов, выбранных из табл. 3, получают масс-фрагментограмму каждого из веществ.
Проводят качественную идентификацию по следующим критериям:
- характеристические ионы для каждого измеряемого компонента должны давать максимальное значение в любом выбранном скане;
- время удерживания не должно отличаться более чем на 20 секунд от времени удерживания стандартного соединения;
- относительная интенсивность пиков трех характеристических ионов в масс-фрагментограмме не должна отличаться более чем на 20 % от относительной интенсивности этих пиков в справочном масс-спектре. Справочный масс-спектр может быть либо библиотечным, либо получен при анализе на хромато-масс-спектрометре градуировочного раствора индивидуального соединения.
На каждой масс-фрагментограмме измеряют площадь пика 3-х характеристических ионов (усл. ед.) для каждого анализируемого вещества. Результаты измерений заносят в табл. 7 и обрабатывают в соответствии с п. 11.
Результаты измерения содержания веществ в пробе воды
|
№ пробы (параллельного определения) |
Площадь характеристических ионов определяемого вещества Qi, усл. ед. |
Градуировочный
поправочный коэффициент, |
Содержание вещества в пробе, мг/дм3 |
|
1 |
Qi1 |
|
Ci1 |
|
2 |
Qi2 |
|
Qi2 |
11. Обработка результатов измерений
11.1. Вычисляют концентрацию определяемого вещества в каждой из 2-х проб по формуле:
|
|
(8) |
![]() - градуировочный поправочный
коэффициент определяемого замещенного фенола;
- градуировочный поправочный
коэффициент определяемого замещенного фенола;
Cф - концентрация фенола, определяемая по градуировочной характеристике, мг/см3;
Vо - объем раствора экстракта, см3;
Vв - объем пробы воды, дм3;
Kэ - коэффициент экстракции вещества, (табл. 6).
11.2. Вычисляют среднее значение концентрации определяемого вещества:
|
|
(9) |
11.3. Рассчитывают разницу между результатами двух параллельных измерений:
|
d = C1 - C2 |
(10) |
Полученное значение не должно превышать значения относительной погрешности Q0 для определяемого вещества (табл. 5).
11.4. Оформление результатов измерения
Оформление результатов измерения содержания замещенных фенолов в воде осуществляют в виде протокола, утверждаемого юридическим лицом, подпись которого заверяется печатью.
|
ПРОТОКОЛ
№ ________ 1. Место проведения анализа _______________________________________________ 2. Юридический адрес лаборатории __________________________________________ 3. Шифр пробы ___________________________________________________________ 4. Место отбора пробы _____________________________________________________ 5. Дата проведения анализа _________________________________________________ Результаты количественного химического анализа
Научный руководитель Ответственный за проведение анализ |
Погрешность измерения может быть выражена либо в процентах, либо в мг/дм3 при доверительной вероятности 0,95.
12. Контроль погрешности измерений
12.1. Перед обработкой любых результатов необходимо проанализировать «холостую пробу» дистиллированной воды по п. 10.8, чтобы убедиться в отсутствии помех и загрязнений от аналитической системы, стеклянного оборудования и реагентов. При выявлении загрязнений обнаруживают их источник, постадийно анализируя все реактивы. Анализ «холостой пробы» проводят также при использовании новой партии реактивов.
12.2. При выполнении каждого анализа проб воды проводят оперативный контроль погрешности измерений по п. 11.3.
12.3. Проводят контроль аттестованных растворов определяемых компонентов. Рассчитывают среднее значение результатов измерений n-го компонента в аттестованном растворе:
|
|
n - результаты измерения концентрации n-го компонента в i-ой пробе аттестованного раствора, мг/дм3.
Полученное значение должно удовлетворять условию:
|
Сн < Сn < Св, где |
Сн и Св - нижнее и верхнее значение концентрации для каждого компонента и каждого аттестованного раствора.
Рассчитывают среднее квадратическое отклонение результатов измерения:
|
|
и относительное отклонение
|
|
Сравнивают полученные значения отклонений результатов измерений с предельно допустимым. Если выполняется условие Sотн ≤ θ0, то воспроизводимость измерения является удовлетворительной. Если для какого-либо компонента данное условие не выполняется, то выясняют причину и повторяют измерения.
Приложение
Расчет погрешности количественных измерений содержания
замещенных
фенолов в водных растворах
1. Расчет погрешности количественных измерений содержания фенола
1.1. Погрешность чистоты реактивов.
Погрешность чистоты реактивов, определяемая квалификацией реактивов, для фенола из набора стандартных образцов АОЗТ «ЭКРОС» θ1 = 1 %, для метанола, квалификации для хроматографии марки «ос. ч.» согласно ТУ 6-09-2192-85 02 θ2 = 1 %.
1.2. Погрешность измерения объемов.
Погрешность измерения объемов растворов определяется погрешностью химической посуды, пипеток, шприцев. Погрешность измерения объема раствора пипеткой вместимостью 0,1 см3 (2-го класса) согласно ГОСТу 29169-91 равна половине цены деления ±0,0005 см3 и для измерения растворов объемом 0,1 см3 равна:
|
|
Погрешность измерения раствора пипеткой вместимостью 1,0 см3 (2-го класса) согласно ГОСТу 29169-91 равна половине цены деления ±0,005 см3 и для измерения растворов объемом 1,0 см3 равна:
|
|
Погрешность измерения раствора пипеткой вместимостью 2,0 см3 (2-го класса) согласно ГОСТу 29169-91 равна половине цены деления ±0,02 см3 и для измерения растворов объемом 2,0 см3 равна:
|
|
Погрешность измерения объема раствора в мерной колбе θ6 вместимостью 10 см3 (2-го класса) погрешностью ±0,06 см3 согласно ГОСТу 1770-74Е равна:
|
|
Погрешность измерения объема раствора в мерной колбе θ7 вместимостью 50 см3 (2-го класса) погрешностью ±0,5 см3 согласно ГОСТу 1770-74Е равна:
|
|
1.3. Погрешность приготовления градуировочных растворов фенола в метаноле.
Погрешность приготовления градуировочных растворов вычисляется по формуле
|
|
n, m, p, q, r - соответствующее число операций.
Погрешность приготовления градуировочных растворов фенола в метаноле с концентрацией 0,001 мг/см3 составляет:
|
|
с концентрацией 0,01 мг/см3:
|
|
с концентрацией 0,05 мг/см3:
|
|
с концентрацией 0,1 мг/см3:
|
|
с концентрацией 0,2 мг/см3:
|
|
1.4. Погрешность измерений концентраций растворов фенола в метаноле с помощью градуировочной характеристики.
Погрешность θшпр измерения объема вводимой в хроматограф пробы шприцем фирмы «Hamilton» вместимостью 0,001 см3 равна половине цены деления ±0,00001 см3 и для измерения объема раствора 0,001 см3 равна:
|
|
Погрешность построения градуировочной характеристики растворов фенола в метаноле θ8:
Таблица
|
№ измерения k |
Аналитический сигнал Ii, усл. ед. |
|
Δmm соответствующая ΔIm, нг |
|
|||
|
Концентрация градуировочного раствора Ci = 0,001 мг/см3 |
|||||||
|
Масса введенной в хроматограф пробы |
|||||||
|
1 |
0,95×106 |
-0,05×106 |
0,13 |
|
|||
|
2 |
1,02×106 |
0,02×106 |
|
|
|||
|
3 |
0,97×106 |
-0,03×106 |
|
|
|||
|
4 |
0,98×106 |
-0,02×106 |
|
|
|||
|
5 |
1,13×106 |
0,13×106 |
|
|
|||
|
6 |
0,94×106 |
-0,06×106 |
|
|
|||
|
|
|
ΔIm = 0,13×106 |
|
|
|||
|
Концентрация градуировочного раствора Ci = 0,01 мг/см3 |
|||||||
|
Масса введенной в хроматограф пробы |
|||||||
|
1 |
4,37×106 |
-0,04×106 |
0,16 |
|
|||
|
2 |
4,42×106 |
0,01×106 |
|
|
|||
|
3 |
4,38×106 |
-0,03×106 |
|
|
|||
|
4 |
4,44×106 |
0,03×106 |
|
|
|||
|
5 |
4,39×106 |
-0,02×106 |
|
|
|||
|
6 |
4,48×106 |
0,07×106 |
|
|
|||
|
|
|
ΔIm = 0,07×106 |
|
|
|||
|
Концентрация градуировочного раствора Ci = 0,05 мг/см3 |
|||||||
|
Масса введенной в хроматограф пробы |
|||||||
|
1 |
24,76×106 |
-0,34×106 |
4,8 |
|
|||
|
2 |
22,68×106 |
-2,42×106 |
|
|
|||
|
3 |
27,03×106 |
1,93×106 |
|
|
|||
|
4 |
25,15×106 |
0,05×106 |
|
|
|||
|
5 |
26,04×106 |
0,94×106 |
|
|
|||
|
6 |
24,98×106 |
-0,12×106 |
|
|
|||
|
|
|
ΔIm = 2,42×106 |
|
|
|||
|
Концентрация градуировочного раствора Ci = 0,1 мг/см3 |
|||||||
|
Масса введенной в хроматограф пробы |
|||||||
|
1 |
50,61×106 |
2,02×106 |
5,8 |
|
|||
|
2 |
45,75×106 |
-2,84×106 |
|
|
|||
|
3 |
47,66×106 |
-0,93×106 |
|
|
|||
|
4 |
48,61×106 |
0,02×106 |
|
|
|||
|
5 |
50,41×106 |
1,82×106 |
|
|
|||
|
6 |
48,47×106 |
-0,12×106 |
|
|
|||
|
|
|
ΔIm = 2,84×106 |
|
|
|||
|
Концентрация градуировочного раствора Ci = 0,2 мг/см3 |
|||||||
|
Масса введенной в хроматограф пробы |
|||||||
|
1 |
242×106 |
- |
6,6 |
|
|||
|
2 |
244×106 |
2×106 |
|
|
|||
|
3 |
250×106 |
8×106 |
|
|
|||
|
4 |
242×106 |
|
|
|
|||
|
5 |
238×106 |
-4×106 |
|
|
|||
|
6 |
248×106 |
6×106 |
|
|
|||
|
7 |
236×106 |
-6×106 |
|
|
|||
|
8 |
245×106 |
3×106 |
|
|
|||
|
|
|
ΔIm = 8×106 |
|
|
|||
Из погрешностей всего интервала концентраций выбираем максимальное значение, которое принимаем за погрешность градуировочной характеристики θ8 = 13 %.
Погрешность измерений концентраций растворов фенола в метаноле с помощью градуировочной характеристики Qгр равна:
|
|
1.5. Погрешность извлечения фенола из водного раствора.
Для вычисления степени извлечения фенола из водного раствора методом экстракции в 1,0 дм3 воды добавляют 0,1, 0,01 и 0,001 см3 раствора фенола в метаноле с концентрацией 500 мкг/см3. Приготовленные водные растворы экстрагируют 3 порциями по 20 см3 хлористого метилена, экстракт отделяют от водной фазы и упаривают до объема 0,2 см3 на водяной бане. Проводят хромато-масс-спектрометрический анализ упаренного раствора фенола в рабочих условиях определения пробы и по градуировочной характеристике рассчитывают количество извлеченного из воды фенола.
Таблица
|
№ измерения k |
Аналитический сигнал Ii, усл. ед. |
|
Δmm соответствующая ΔIm, нг |
|
|
Количество введенного в хроматограф фенола mi = 0,1 мкг = 100 нг |
||||
|
1 |
39,78×106 |
-1,47×106 |
3,8 |
|
|
2 |
43,10×106 |
1,85×106 |
|
|
|
3 |
41,17×106 |
0,08×106 |
|
|
|
4 |
40,95×106 |
-0,30×106 |
|
|
|
|
|
ΔIm = 1,85×106 |
|
|
|
|
|
|
|
|
|
Степень
извлечения: |
||||
|
Количество введенного в хроматограф фенола mi = 0,01 мкг = 10 нг |
||||
|
1 |
3,11×106 |
-0,41×106 |
1,2 |
|
|
2 |
3,33×106 |
-0,19×106 |
|
|
|
3 |
4,05×106 |
0,53×106 |
|
|
|
4 |
3,59×106 |
0,07×106 |
|
|
|
|
|
ΔIm = 0,53×106 |
|
|
|
|
|
|
|
|
|
Степень
извлечения: |
||||
|
Количество введенного в хроматограф фенола mi = 0,001 мкг = 1 нг |
||||
|
1 |
0,95×106 |
-0,15×106 |
0,15 |
|
|
2 |
0,75×106 |
-0,05×106 |
|
|
|
3 |
0,78×106 |
-0,02×106 |
|
|
|
4 |
0,72×106 |
0,08×106 |
|
|
|
|
|
ΔIm = 0,15×106 |
|
|
|
|
|
|
|
|
|
Степень извлечения:
|
||||
Максимальная погрешность при экстракции фенола θэ составляет 19 %.
1.6. Систематическая погрешность измерения концентраций фенола определяется по формуле:
|
|
1.7. Границы суммы неисключенных систематических погрешностей измерения концентраций фенола θ0 рассчитывают по формуле:
|
|
K - коэффициент, определяемый принятой доверительной вероятностью, равный 1,1 при доверительной вероятности 0,95.
|
|
1.8. Среднюю квадратическую погрешность результатов измерений содержания фенола S определяют по формуле:
|
|
Рассчитывают результатов измерений относительную среднюю квадратическую погрешность измерений содержания фенола SF по формуле:
|
|
Таблица
|
№ измерения k |
Масса mi, нг |
Среднее арифметическое m |
mi - m |
(mi - m)2 |
S |
SF, % |
|
1 |
0,95 |
1,00 |
-0,05 |
0,0025 |
0,070 |
2,9 |
|
2 |
1,02 |
|
0,02 |
0,0004 |
|
|
|
3 |
0,97 |
|
-0,03 |
0,0009 |
|
|
|
4 |
0,98 |
|
-0,02 |
0,0004 |
|
|
|
5 |
1,13 |
|
0,13 |
0,0169 |
|
|
|
6 |
0,94 |
|
-0,06 |
0,0036 |
|
|
|
|
|
|
|
|
|
|
|
1 |
9,91 |
10,0 |
-0,09 |
0,0081 |
0,095 |
0,39 |
|
2 |
10,02 |
|
0,02 |
0,0004 |
|
|
|
3 |
9,93 |
|
-0,07 |
0,0049 |
|
|
|
4 |
10,06 |
|
0,06 |
0,0036 |
|
|
|
5 |
9,95 |
|
-0,05 |
0,0025 |
|
|
|
6 |
10,16 |
|
0,16 |
0,0256 |
|
|
|
|
|
|
|
0,0451 |
|
|
|
1 |
49,3 |
50,0 |
-0,7 |
0,49 |
2,88 |
2,4 |
|
2 |
45,2 |
|
-4,8 |
23,0 |
|
|
|
3 |
53,8 |
|
3,8 |
14,4 |
|
|
|
4 |
50,0 |
|
- |
- |
|
|
|
5 |
51,9 |
|
1,9 |
3,61 |
|
|
|
6 |
49,8 |
|
-0,2 |
0,04 |
|
|
|
|
|
|
|
41,54 |
|
|
|
1 |
104 |
100 |
4 |
16 |
3,79 |
1,5 |
|
2 |
94 |
|
-6 |
36 |
|
|
|
3 |
98 |
|
-2 |
4 |
|
|
|
4 |
100 |
|
- |
- |
|
|
|
5 |
104 |
|
4 |
16 |
|
|
|
6 |
100 |
|
- |
- |
|
|
|
|
|
|
|
72 |
|
|
|
1 |
200 |
201 |
-1 |
1 |
4,19 |
0,79 |
|
2 |
202 |
|
2 |
4 |
|
|
|
3 |
207 |
|
7 |
49 |
|
|
|
4 |
200 |
|
-1 |
1 |
|
|
|
5 |
197 |
|
-4 |
16 |
|
|
|
6 |
205 |
|
4 |
16 |
|
|
|
7 |
195 |
|
-6 |
36 |
|
|
|
8 |
202 |
|
1 |
1 |
|
|
|
|
|
|
|
123 |
|
|
Максимальная относительная квадратическая погрешность результатов измерений концентраций фенола составляет 2,9 %.
2. Расчет погрешности количественных измерений содержания замещенных фенолов
2.1. Погрешность чистоты реактивов.
Погрешность чистоты реактивов замещенных фенолов θ1 определяется квалификацией реактивов из набора стандартных образцов АОЗТ «ЭКРОС» и НПО «МС-АНАЛИТИКА».
2.2. Погрешность измерений концентраций с помощью градуировочной характеристики.
Погрешность измерений концентраций замещенных фенолов с помощью градуировочной характеристики, установленной для фенола θ2 = 13 %.
2.3. Погрешность измерения объемов.
Погрешность измерения объема вводимой в хроматограф пробы с помощью шприца фирмы «Hamilton» θ3 составляет 1 %.
2.4. Погрешность определения поправочного градуировочного коэффициента.
Погрешность определения поправочного градуировочного коэффициента θ4 рассчитывают по формуле:
|
|
Fi - значение i-го поправочного градуировочного коэффициента, определяемого по формуле:
|
|
Qi - площадь пиков характеристических ионов определяемого соединения на i-й масс-фрагментограмме, усл. ед.;
Qф - площадь пиков характеристических ионов фенола на масс-фрагментограмме, равная 2,42 10 усл. ед.;
mi и mф - масса определяемого соединения и фенола, вводимые в хроматограф, равные 200 нг;
Fn - среднее значение поправочного коэффициента, которое рассчитывают по формуле:
|
|
2.5. Погрешность измерений концентраций замещенных фенолов.
Погрешность измерений концентраций замещенных фенолов θизм определяют по формуле:
|
|
2.6. Границы суммы неисключенных систематических погрешностей измерений концентраций θ0 рассчитывают по формуле:
|
|
K - коэффициент, определяемый принятой доверительной вероятностью, равный 1,1 при доверительной вероятности 0,95.
2.7. Среднюю квадратичную погрешность результатов измерений S определяют по формуле:
|
|
2.8. Относительную среднюю квадратическую погрешность результатов измерений S рассчитывают по формуле:
|
|
Результаты расчетов погрешностей приведены в таблице.
Таблица
|
№ измерения, k |
Площадь пика Qi, усл. ед. |
Попр. коэфф. Fi |
ΔF |
θ4 |
θизм |
θ0 |
S |
SF |
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
|
2-Хлорфенол (θ1 = 1 %) |
||||||||
|
1 |
106×106 |
2,3 |
-0,2 |
|
|
|
|
|
|
2 |
100×106 |
2,4 |
-0,1 |
|
|
|
|
|
|
3 |
95×106 |
2,5 |
- |
|
|
|
|
|
|
4 |
91×106 |
2,6 |
0,1 |
8 % |
15 % |
17 % |
0,1 |
1,4 % |
|
5 |
98×106 |
2,5 |
- |
|
|
|
|
|
|
6 |
95×106 |
2,5 |
- |
|
|
|
|
|
|
7 |
94×106 |
2,6 |
0,1 |
|
|
|
|
|
|
8 |
93×106 |
2,6 |
0,1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
о-Крезол (θ2 = 2 %) |
||||||||
|
1 |
41×106 |
6,0 |
0,6 |
|
|
|
|
|
|
2 |
46×106 |
5,4 |
- |
|
|
|
|
|
|
3 |
45×106 |
5,4 |
- |
11 % |
17 % |
19 % |
0,1 |
2,3 % |
|
4 |
50×106 |
4,8 |
-0,6 |
|
|
|
|
|
|
5 |
45×106 |
5,4 |
- |
|
|
|
|
|
|
6 |
45×106 |
5,4 |
- |
|
|
|
|
|
|
|
||||||||
|
п-Крезол (θ1 = 2 %) |
||||||||
|
1 |
49×106 |
5,1 |
- |
|
|
|
|
|
|
2 |
45×106 |
5,4 |
0,3 |
|
|
|
|
|
|
3 |
51×106 |
4,8 |
-0,3 |
12 % |
18 % |
20 % |
0,1 |
2,4 % |
|
4 |
51×106 |
4,8 |
-0,3 |
|
|
|
|
|
|
5 |
48×106 |
5,1 |
- |
|
|
|
|
|
|
6 |
53×106 |
4,5 |
-0,6 |
|
|
|
|
|
|
|
||||||||
|
Гваякол (θ1 = 2 %) |
||||||||
|
1 |
22×106 |
11,1 |
-0,6 |
|
|
|
|
|
|
2 |
21×106 |
11,7 |
- |
|
|
|
|
|
|
3 |
22×106 |
10,8 |
-0,9 |
23 % |
26 % |
28 % |
0,3 |
3,1 % |
|
4 |
20×106 |
12,3 |
0,6 |
|
|
|
|
|
|
5 |
21×106 |
11,4 |
-0,3 |
|
|
|
|
|
|
6 |
18×106 |
13,2 |
1,5 |
|
|
|
|
|
|
|
||||||||
|
2,6-Ксиленол (θ1 = 2 %) |
||||||||
|
1 |
20×106 |
12,3 |
-0,3 |
|
|
|
|
|
|
2 |
19×106 |
12,9 |
0,3 |
|
|
|
|
|
|
3 |
18×106 |
13,2 |
0,6 |
7,1 % |
15 % |
17 % |
0,2 |
1,9 % |
|
4 |
21×106 |
11,7 |
-0,9 |
|
|
|
|
|
|
5 |
18×106 |
13,2 |
0,6 |
|
|
|
|
|
|
6 |
21×106 |
11,7 |
-0,9 |
|
|
|
|
|
|
|
||||||||
|
2,4-Дихлорфенол (θ1 = 1 %) |
||||||||
|
1 |
64×106 |
3,8 |
0,2 |
|
|
|
|
|
|
2 |
69×106 |
3,5 |
-0,1 |
|
|
|
|
|
|
3 |
65×106 |
3,7 |
0,1 |
|
|
|
|
|
|
4 |
68×106 |
3,6 |
- |
5,6 % |
14 % |
15 % |
0,1 |
1,0 % |
|
5 |
67×106 |
3,6 |
- |
|
|
|
|
|
|
6 |
66×106 |
3,7 |
0,1 |
|
|
|
|
|
|
7 |
70×106 |
3,5 |
-0,1 |
|
|
|
|
|
|
8 |
68×106 |
3,6 |
- |
|
|
|
|
|
|
|
||||||||
|
4-Хлорфенол (θ1 = 2 %) |
||||||||
|
1 |
134×106 |
1,8 |
-0,3 |
|
|
|
|
|
|
2 |
121×106 |
2,0 |
0,1 |
|
|
|
|
|
|
3 |
142×106 |
1,7 |
-0,4 |
|
|
|
|
|
|
4 |
105×106 |
2,3 |
0,2 |
13 % |
19 % |
21 % |
0,2 |
2,6 % |
|
5 |
110×106 |
2,2 |
0,1 |
|
|
|
|
|
|
6 |
105×106 |
2,3 |
0,2 |
|
|
|
|
|
|
7 |
107×106 |
2,2 |
0,1 |
|
|
|
|
|
|
8 |
121×106 |
2,0 |
-0,1 |
|
|
|
|
|
|
|
||||||||
|
2,6-Дихлорфенол (θ1 = 1 %) |
||||||||
|
1 |
65×106 |
3,7 |
0,1 |
|
|
|
|
|
|
2 |
64×106 |
3,8 |
0,2 |
|
|
|
|
|
|
3 |
68×106 |
3,6 |
- |
|
|
|
|
|
|
4 |
70×106 |
3,5 |
-0,1 |
8,3% |
15% |
17% |
0,2 |
2,0% |
|
5 |
63×106 |
3,8 |
0,2 |
|
|
|
|
|
|
6 |
72×106 |
3,4 |
0,2 |
|
|
|
|
|
|
7 |
64×106 |
3,8 |
-0,2 |
|
|
|
|
|
|
8 |
74×106 |
3,3 |
-0,3 |
|
|
|
|
|
|
|
||||||||
|
Пирокатехин (θ1 = 2 %) |
||||||||
|
|
|
|
|
|
|
|
|
|
|
1 |
53×106 |
4,6 |
-0,4 |
|
|
|
|
|
|
2 |
51×106 |
4,7 |
-0,3 |
|
|
|
|
|
|
3 |
48×106 |
5,0 |
- |
12 % |
18 % |
20 % |
0,3 |
2,4 % |
|
4 |
48×106 |
5,0 |
- |
|
|
|
|
|
|
5 |
48×106 |
5,0 |
- |
|
|
|
|
|
|
6 |
43×106 |
5,6 |
0,6 |
|
|
|
|
|
|
|
||||||||
|
Резорцин (θ1 = 2 %) |
||||||||
|
|
|
|
|
|
|
|
|
|
|
1 |
47×106 |
5,2 |
-0,2 |
|
|
|
|
|
|
2 |
45×106 |
5,4 |
- |
|
|
|
|
|
|
3 |
44×106 |
5,5 |
0,1 |
11 % |
17 % |
19 % |
0,3 |
2,3 % |
|
4 |
41×106 |
5,9 |
0,5 |
|
|
|
|
|
|
5 |
47×106 |
5,2 |
-0,2 |
|
|
|
|
|
|
6 |
48×106 |
5,0 |
-0,4 |
|
|
|
|
|
|
|
||||||||
|
2,4,6-Трихлорфенол (θ1 = 1 %) |
||||||||
|
1 |
50×106 |
4,8 |
-0,4 |
|
|
|
|
|
|
2 |
48×106 |
5,0 |
-0,2 |
|
|
|
|
|
|
3 |
45×106 |
5,4 |
0,2 |
|
|
|
|
|
|
4 |
42×106 |
5,8 |
0,6 |
12 % |
18 % |
20 % |
0,3 |
2,1 % |
|
5 |
46×106 |
5,3 |
0,1 |
|
|
|
|
|
|
6 |
45×106 |
5,4 |
0,2 |
|
|
|
|
|
|
7 |
47×106 |
5,1 |
-0,1 |
|
|
|
|
|
|
8 |
48×106 |
5,0 |
-0,2 |
|
|
|
|
|
|
|
||||||||
|
2,4,5-Трихлорфенол (θ1 = 1 %) |
||||||||
|
1 |
46×106 |
5,3 |
0,9 |
|
|
|
|
|
|
2 |
57×106 |
4,2 |
-0,2 |
|
|
|
|
|
|
3 |
57×106 |
4,2 |
-0,2 |
|
|
|
|
|
|
4 |
53×106 |
4,6 |
0,2 |
20 % |
24 % |
26 % |
0,4 |
3,2 % |
|
5 |
62×106 |
3,9 |
-0,5 |
|
|
|
|
|
|
6 |
59×106 |
4,1 |
-0,3 |
|
|
|
|
|
|
7 |
57×106 |
4,2 |
-0,2 |
|
|
|
|
|
|
8 |
54×106 |
4,5 |
0,1 |
|
|
|
|
|
|
|
||||||||
|
п-Нитрофенол (θ1 = 2 %) |
||||||||
|
1 |
8,3×106 |
29,1 |
0,6 |
|
|
|
|
|
|
2 |
7,7×106 |
31,5 |
3,0 |
|
|
|
|
|
|
3 |
9,0×106 |
27,0 |
-1,5 |
13 % |
19 % |
21 % |
0,6 |
2,6 % |
|
4 |
9,3×106 |
26,7 |
-1,8 |
|
|
|
|
|
|
5 |
8,9×106 |
27,3 |
-1,2 |
|
|
|
|
|
|
6 |
8,3×106 |
29,1 |
0,6 |
|
|
|
|
|
|
|
||||||||
|
2,3,4,5-Тетрахлорфенол (θ1 = 2 %) |
||||||||
|
1 |
43×106 |
5,6 |
0,3 |
|
|
|
|
|
|
2 |
45×106 |
5,4 |
0,1 |
|
|
|
|
|
|
3 |
49×106 |
4,9 |
-0,5 |
13 % |
19 % |
21 % |
0,3 |
2,3 % |
|
4 |
46×106 |
5,3 |
- |
|
|
|
|
|
|
5 |
45×106 |
5,4 |
0,1 |
|
|
|
|
|
|
6 |
44×106 |
5,2 |
-0,1 |
|
|
|
|
|
|
|
||||||||
|
Главный государственный санитарный врач Российской Федерации |
Г.Г. Онищенко |