 | Информационная система |  |
Государственное санитарно-эпидемиологическое
нормирование
Российской Федерации
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение остаточных количеств
флуфенацета и суммы всех метаболитов,
содержащих N-фторфенил-N-изопропил
радикалы в воде, почве, зерне и соломе
зерновых колосовых, в клубнях картофеля
методом капиллярной газожидкостной
хроматографии
Методические указания
МУК 4.1.3203-14
Москва 2015
1. Разработаны Российским государственным аграрным университетом - МСХА им. К.А. Тимирязева, Учебно-научным консультационным центром «Агроэкология пестицидов и агрохимикатов» Минсельхоза России (В.А. Калинин, А.В. Довгилевич, О.И. Рыбакова).
2. Рекомендованы к утверждению Комиссией по государственному санитарно-эпидемиологическому нормированию Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (протокол от 26 июня 2014 г. № 1).
3. Утверждены руководителем Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, Главным государственным санитарным врачом Российской Федерации А.Ю. Поповой 30 июля 2014 г.
4. Введены впервые.
СОДЕРЖАНИЕ
|
УТВЕРЖДАЮ Руководитель
Федеральной службы ______________________ А.Ю. Попова 30 июля 2014 г. |
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение остаточных количеств флуфенацета и
суммы всех метаболитов, содержащих
N-фторфенил-N-изопропил
радикалы в воде, почве,
зерне и соломе зерновых колосовых,
в клубнях картофеля методом капиллярной
газожидкостной хроматографии
Методические указания
МУК 4.1.3203-14
Свидетельство о метрологической аттестации № 01.00282-2008/0190.19.12.13 от 19.12.2013.
Настоящие методические указания устанавливают порядок применения метода капиллярной газожидкостной хроматографии для определения массовых концентраций флуфенацета и суммы всех метаболитов, содержащих N-фторфенил-N-изопропил радикалы (оксалат, сернистая кислота и тригликолат сульфоксид) с пересчетом на флуфенацет в воде в диапазоне 0,0005 - 0,005 мг/дм3 и в почве в диапазоне 0,05 - 0,5 мг/кг, а также уровня их остаточных количеств в зерне пшеницы, клубнях картофеля в диапазоне 0,05 - 0,5 мг/кг и в соломе пшеницы в диапазоне 0,1 - 1,0 мг/кг. Методические указания носят рекомендательный характер.
Флуфенацет (I)
N-(4-фторфенил)-N-(метилэтил)-2-[[5-(трифторметил)-1,3,4-тиадиазол-2-ил]окси]ацетамид.
Структурная формула:
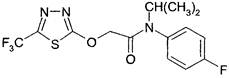
Эмпирическая формула: C14H13F4N3O2S.
Молекулярная масса: 363,3.
Агрегатное состояние: бесцветный кристаллический порошок со слабым неспецифическим запахом.
Температура плавления: частичное плавление происходит при температуре 76 °С, вновь образовавшиеся из расплавленной массы кристаллы плавятся при температуре 79 °С.
Давление паров (при 20 °С): 9×10-7 гПа.
Коэффициент распределения октанол/вода: Kow log Р = 3,2 при 24 °С.
Растворимость в воде (мг/дм3, при 25 °С): при pH 4 и 7 - 56, при pH 9 - 54.
Растворимость (г/дм3, при 20 °С): гексан - 8,7; изопропанол - 170; октанол - 88; полиэтиленгликоль - 74; дихлорометан, ацетонитрил, ацетон > 200.
Стабилен к гидролизу в водных растворах в диапазоне pH от 5 до 9, стабилен к фотолизу при pH 5.
Краткая токсикологическая характеристика. Флуфенацет относится к умеренно опасным веществам по острой пероральной (ЛД50 для крыс - от 589 до 1617 мг/кг) и ингаляционной дермальной (ЛК50 для крыс (4 часа) более 3740 мг/м3) токсичностям, но к мало опасным веществам по дермальной токсичности (ЛД50 крыс более 2000 мг/кг).
Область применения. Флуфенацет - гербицид из группы тиадиазолов, ингибитор процесса деления клеток и роста растений. Применяется для борьбы с широким кругом злаковых и некоторых широколиственных сорняков в предвсходовый и ранний послевсходовый период на кукурузе, зерновых, хлопчатнике, картофеле, рисе, сое, подсолнечнике, томатах и других культурах с нормой расхода 50 - 900 г/га.
Проходит регистрационные испытания в России в качестве гербицида в составе смесевых препаратов в посевах зерновых культур с нормой расхода 120 г/га по д.в.
Метаболиты флуфенацета
Оксалат (II)
N-(4-фторфенил)-М-(метилэтил)-аминощавелевая кислота.
Структурная формула:
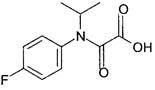
Сернистая кислота (III)
N-(4-фторфенил)-N-(метилэтил)-ацетамид-2-сернистая кислота.
Структурная формула:
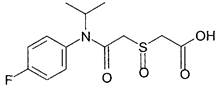
Тригликолат сульфоксид (IV)
N-(4-фторфенил)-N-(метилэтил)-ацетамид-2-сульфинил уксусная кислота.
Структурная формула:

Дериват флуфенацета (V)
4-фтор-N-метилэтил бензенамин трифторацетамид.
Структурная формула:
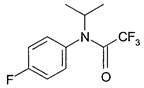
ВМДУ в импортируемой продукции: зерно зерновых культур, клубни картофеля - 0,05 мг/кг.
1. Погрешность измерений
При соблюдении всех регламентированных условий проведения анализа в точном соответствии с данной методикой погрешность (и ее составляющие) результатов измерений при доверительной вероятности Р = 0,95 не превышает значений, приведенных в табл. 1 для соответствующих диапазонов концентраций.
Полнота извлечения вещества, стандартное отклонение, доверительные интервалы среднего результата для полного диапазона концентраций (n = 20) приведены в табл. 2.
Метрологические параметры для флуфенацета
|
Анализируемый объект |
Диапазон определяемых концентраций, мг/кг (мг/дм3) |
Показатель точности (граница относительной погрешности), ±δ, % Р = 0,95 |
Стандартное отклонение повторяемости, σr, % |
Предел повторяемости, r, % |
Предел воспроизводимости, R, % |
|
Вода |
0,0005 - 0,005 |
50 |
2,32 |
6,45 |
8,38 |
|
Почва |
0,05 - 0,1 вкл. |
50 |
1,70 |
4,73 |
6,14 |
|
0,2 - 0,5 вкл. |
25 |
1,77 |
4,92 |
6,40 |
|
|
Зерно пшеницы |
0,05 - 0,1 вкл. |
50 |
1,69 |
4,70 |
6,11 |
|
Солома пшеницы |
0,2 - 0,5 вкл. |
25 |
2,53 |
7,03 |
9,14 |
|
0,1 - 1,0 вкл. |
25 |
2,55 |
7,09 |
9,22 |
|
|
Клубни картофеля |
0,05 - 0,1 вкл. |
50 |
2,36 |
6,56 |
8,53 |
|
0,2 - 0,5 вкл. |
25 |
1,90 |
5,28 |
6,87 |
Полнота извлечения вещества, стандартное отклонение,
доверительный интервал среднего результата для флуфенацета
|
Анализируемый объект |
Метрологические параметры, Р = 0,95, n = 20 |
||||
|
предел обнаружения, мг/кг (мг/дм3) |
диапазон определяемых концентраций, мг/кг (мг/дм3) |
среднее значение определения, % |
стандартное отклонение, S, % |
доверительный интервал среднего результата, ±, % |
|
|
Вода |
0,0005 |
0,0005 - 0,005 |
71,68 |
1,80 |
0,61 |
|
Почва |
0,05 |
0,05 - 0,5 |
72,87 |
1,62 |
0,55 |
|
Зерно пшеницы |
0,05 |
0,05 - 0,5 |
75,01 |
2,74 |
0,96 |
|
Солома пшеницы |
0,1 |
0,1 - 1,0 |
73,97 |
2,50 |
0,87 |
|
Клубни картофеля |
0,05 |
0,05 - 0,5 |
73,97 |
2,08 |
0,72 |
2. Метод измерения
Метод основан на определении флуфенацета и суммы всех метаболитов, содержащих N-фторфенил-N-изопропил радикалы методом капиллярной газожидкостной хроматографии с использованием масс-селективного детектора после их окисления перманганатом калия в течение 5 минут и дальнейшего гидролиза до 4-фтор-N-метилэтил бензоламина (далее по тексту фторанилин) путем кипячения матрицы с 47 %-м раствором серной кислоты в течение 24 часов. Фторанилин отделяют от матрицы методом перегонки с водяным паром и экстрагируют из дистиллята органическим растворителем. Фторанилин дериватизируют трифторуксусным ангидридом с последующей очисткой полученного деривата флуфенацета 4-фтор-N-метилэтил бензенамин трифторацетамид (V) на концентрирующих патронах № 1.
Идентификация вещества проводится по времени удерживания пика целевого иона деривата. Для повышения уровня достоверности идентификации используют два подтверждающих иона, принадлежащих веществу. Количественное определение проводится путем определения соотношения интенсивности (площади) пиков, отвечающих характеристичным ионам идентифицируемого компонента и аналитического стандарта на регистрируемых ионных масс-хроматограммах.
В предлагаемых условиях анализа метод специфичен. Избирательность метода достигается за счет использования масс-селективного детектора по ионам, характеризующим вещество.
3. Средства измерений, реактивы,
вспомогательные устройства и материалы
3.1. Средства измерений
|
Весы аналитические класса точности специальный (I) с наибольшим пределом взвешивания до 110 г и дискретностью 0,0001 г |
|
|
Весы лабораторные общего назначения класса точности средний (III) с наибольшим пределом взвешивания до 600 г и пределом допустимой погрешности ±0,038 г |
|
|
Колбы мерные на 10, 25, 50, 100, 500 и 1000 см3 |
|
|
Пипетки мерные на 1,0; 2,0; 5,0 см3 |
|
|
Пробирки мерные на 10 см3 |
|
|
Хроматографическая система, включающая: - хроматограф газовый с электронным регулированием всех газовых потоков и возможностью управления параметрами газа-носителя в колонке, снабженный стандартным автосамплером с дозирующим объемом от 0,1 до 100 мм3 для автоматического ввода пробы в хроматографическую систему и масс-селективным детектором с высокопроизводительным турбомолекулярным насосом - компьютерное программное обеспечение, обслуживающее управление работой всего прибора, настройку и управление работой вакуумной системы, обеспечивающее сбор и хранение всех данных, поступающих с системы «газовый хроматограф - масс-селективный детектор», выполнение библиотечного поиска и количественный анализ |
|
|
Цилиндры мерные на 10, 25 и 50 см3 |
|
|
Шприц объемом 1 см3 для дозирования газов и агрессивных жидкостей (при давлении до 0,6 мПа) с погрешностью менее 1 % от номинального объема |
|
Примечание. Допускается использование средств измерений с аналогичными или лучшими характеристиками.
3.2. Реактивы
|
Флуфенацет, аналитический стандарт с содержанием действующего вещества не менее 97,8 % |
CAS 142459-58-3 |
|
4-фтор-N-метилэтил бензенамин трифторацетамид, аналитический стандарт с содержанием действующего вещества не менее 99,8 % |
CAS 201668-34-0 |
|
4-фтор-N-метилэтил бензоламин, аналитический стандарт с содержанием действующего вещества не менее 97,3 % |
СAS 70441-63-3 |
|
N, N-диметилформамид, плотность 0,944 г/см3, чистота не менее 99,0 % |
CAS 68-12-2 |
|
4-(диметиламино)пиридин, чистота не менее 99,0 % |
CAS 1122-58-3 |
|
Азот, осч |
|
|
Ацетон, осч |
ТУ 6-09-3513-86 |
|
Бисульфит натрия, чистота не менее 97,0 %, содержание нерастворимых примесей менее 0,005 % |
СAS 7681-57-4 |
|
Вода дистиллированная и (или) бидистиллированная (вода дистиллированная, перегнанная повторно в стеклянной емкости) |
|
|
Гелий, очищенный |
ТУ 51-940-80 |
|
Калий марганцово-кислый, чда |
|
|
Кальций хлористый, ч |
ТУ 6-09-4711-81 |
|
Кислота серная концентрированная, ч |
|
|
Кислота соляная, хч |
|
|
Концентрирующие патроны для твердофазной экстракции с гидрофобным сорбентом с размером частиц 63 - 200 мкм с привитыми гексадецильными (С16) группами (объем - 1 см3, масса сорбента - 0,6 г) (патрон № 1) |
ТУ 4215-002-05451931-94 |
|
Метилен хлористый, хч |
ТУ 2631-019-44493179-98 |
|
Натрий серно-кислый, безводный, хч |
|
|
Натрия гидроокись, хч |
|
|
Пиридин, безводный, плотность 0,978 г/см3, чистота не менее 99,8 %, воды менее 0,003 |
СAS 110-86-1 |
|
Спирт метиловый (метанол), хч |
|
|
Трифторуксусный ангидрид, плотность 1,511 г/см3, чистота не менее 99,0 % Примечание. Трифторуксусный ангидрид является токсичным и очень гигроскопичным. Лучше иметь реагент в небольшой таре и использовать в течение 2 недель после вскрытия бутылки. Обращаться с особой осторожностью в вытяжном шкафу, строго соблюдая технику безопасности. |
CAS 407-25-0 |
Примечание. Допускается использование реактивов с аналогичными или лучшими характеристиками.
3.3. Вспомогательные устройства, материалы
|
Алонж прямой с отводом для вакуума для работы с концентрирующими патронами |
|
|
Аппарат для встряхивания проб с возвратно-поступательным направлением колебаний, с максимальной загрузкой 10 кг, с амплитудой колебаний 30 мм и скоростью от 10 до 300 колебаний в минуту |
|
|
Виалы (пузырьки) с тефлоновыми прокладками емкостью 40 см3 |
|
|
Воронки делительные на 500 см3 |
|
|
Воронки лабораторные, стеклянные |
|
|
Испаритель ротационный вакуумный с ручным подъемником, с диагональным конденсором и объемом испарительной колбы от 50 до 3000 см3, с изменяемой скоростью вращения штока испарителя от 5 до 240 об ./мин, с водяной баней с антикоррозионным покрытием объемом 5 дм3 и с диапазоном температур от 20 до 100 °С |
|
|
Колбы круглодонные со шлифом (концентраторы) на 500, 1000 см3 и 4000 см3 |
ТС ТУ 92-891.029-91 |
|
Колбы круглодонные со шлифом двугорлые на 2000 см3 |
ТС ТУ 92-891.029-91 |
|
Колонка хроматографическая капиллярная из кварцевого стекла с внутренний диаметром 0,25 мм, длиной 30 м, с неподвижной фазой, содержащей 5 % фенила и 95 % метилполисилоксана и толщиной пленки 0,25 мкм |
|
|
Насос диафрагменный, химически стойкий на 100 % с мощностью электропривода 245 Вт, предельным вакуумом 100 мбар/абс., с избыточным давлением 1 бар и скоростью откачки 34 дм3/мин |
|
|
Сито лабораторное с полотном из латуни или нержавеющей стали с размером ячеек 1 мм |
|
|
Стаканы стеклянные, термостойкие объемом 100 - 2000 см3 |
|
|
Установка для перегонки растворителей с круглодонной колбой объемом 4000 см3 и приемной конической колбой объемом 1000 см3 |
|
|
Установка для перегонки с водяным паром с круглодонной двугорлой колбой объемом 2000 см3 и приемной круглодонной колбой объемом 500 см3 |
|
|
Центрифуга лабораторная, настольная с максимальным рабочим числом оборотов 4000 об./мин, с рабочим объемом ротора 200 см3×4 ячейки, выбираемый временной диапазон работы от 0 до 100 мин и с набором полипропиленовых банок емкостью 200 см3 |
|
Примечание. Допускается применение оборудования с аналогичными или лучшими техническими характеристиками.
4. Требования безопасности
4.1. При выполнении измерений необходимо соблюдать требования техники безопасности при работе с химическими реактивами по ГОСТ 12.1.007-76, требования электробезопасности при работе с электроустановками по ГОСТ Р 12.1.019-09, а также требования, изложенные в технической документации на газовый хроматограф.
4.2. Помещение должно соответствовать требованиям пожаробезопасности по ГОСТ 12.1.004-91 и иметь средства пожаротушения по ГОСТ 12.4.009-83. Содержание вредных веществ в воздухе не должно превышать норм, установленных ГН 2.2.5.1313-03 «Предельно допустимые концентрации (ПДК) вредных веществ в воздухе рабочей зоны». Организация обучения работников безопасности труда - по ГОСТ 12.0.004-91.
5. Требования к квалификации операторов
К выполнению измерений и обработке их результатов допускаются специалисты, имеющие опыт работы в химической лаборатории, прошедшие обучение и владеющие техникой проведения анализа, освоившие метод анализа в процессе тренировки и уложившиеся в нормативы контроля при проведении процедуры контроля погрешности анализа.
6. Условия измерений
При выполнении измерений соблюдают следующие условия:
- процессы приготовления растворов и подготовки проб к анализу проводят при температуре воздуха (20 ± 5) °С, относительной влажности не более 80 % и нормальном атмосферном давлении;
- выполнение измерений на жидкостном хроматографе проводят в условиях, рекомендованных технической документацией к прибору.
7. Подготовка к определению
Выполнению измерений предшествуют следующие операции: очистка растворителей (при необходимости), приготовление растворов, кондиционирование хроматографической колонки, подготовка концентрирующих патронов № 1 для очистки экстракта, проверка хроматографического поведения веществ на концентрирующих патронах № 1, установление градуировочной характеристики.
7.1. Подготовка органических растворителей
7.1.1. Очистка ацетона
Ацетон, содержащий воду, предварительно осушают, добавляя в него гранулированный безводный хлористый кальций из расчета не менее 100 г/дм3. Выдерживают его над осушителем в течение 5 - 6 часов. Затем ацетон сливают с осушителя в круглодонную колбу со шлифом объемом 4000 см3 аппарата для перегонки растворителей, прибавляют туда марганцово-кислый калий из расчета 100 мг/дм3. Ацетон перегоняют при температуре 56,2 °С, а фракции, отогнанные при температуре ниже и выше 56,2 °С, отбрасывают.
7.1.2. Очистка метанола
Метанол, содержащий воду, предварительно осушают, добавляя в него гранулированный безводный углекислый калий из расчета не менее 100 г/дм3. Выдерживают его над осушителем в течение 5 - 6 часов. Затем метанол фильтруют через фильтр низкой плотности в круглодонную колбу со шлифом объемом 4000 см3 аппарата для перегонки растворителей.
Метанол перегоняют при температуре 64,7 °С, а фракции, отогнанные при температуре ниже и выше 64,7 °С отбрасывают.
7.1.3. Приготовление бидистиллированной воды
Дистиллированную воду помещают в круглодонную колбу со шлифом объемом 4000 см3 от аппарата для перегонки растворителей, добавляют к ней марганцово-кислый калий из расчета 1 г/дм3 и кипятят в течение 6 часов.
Собирают фракции, отогнанные при температуре 100,0 °С, а фракции, отогнанные при температуре ниже и выше 100,0 °С отбрасывают.
7.2. Приготовление растворов для проведения анализа
7.2.1. Приготовление рабочих растворов
7.2.1.1. Приготовление 50 %-го раствора гидроокиси натрия.
В мерную колбу на 100 см3 переносят 50 г гидроокиси натрия, добавляют 50 - 60 см3 дистиллированной воды. Затем раствор перемешивают и после охлаждения доводят водой объем в колбе до метки (при приготовлении раствора соблюдать осторожность и работать под тягой).
7.2.1.2. Приготовление 0,2 %-го раствора 4-(диметиламино)пиридина в пиридине.
В мерную колбу объемом 25 см3 помещают 0,05 г 4-(диметиламино)пиридина, прибавляют 15 см3 пиридина, перемешивают и доводят пиридином объем в колбе до метки (при приготовлении раствора соблюдать осторожность и работать под тягой).
7.2.1.3. Приготовление 1 и раствора серной кислоты.
Мерным цилиндром отбирают 28 см3 концентрированной серной кислоты и осторожно переносят в мерную колбу на 1000 см3, куда предварительно наливают около 500 см3 дистиллированной воды. Затем раствор перемешивают и после охлаждения доводят водой объем в колбе до метки (при приготовлении раствора соблюдать осторожность и работать под тягой).
7.2.2. Приготовление градуировочных растворов
7.2.2.1. Стандартный раствор № 1 с концентрацией деривата флуфенацета (V) 250 мкг/см3 (в пересчете на эквивалент флуфенацета I).
В мерную колбу вместимостью 100 см3 помещают 17,15 мг 4-фтор-N-метилэтил бензенамин трифторацетамид (V, дериват флуфенацета), растворяют в 40 - 50 см3 ацетона, доводят объем до метки ацетоном, тщательно перемешивают. Стандартный раствор № 1 хранят в холодильнике в течение 3 месяцев.
7.2.2.2. Стандартный раствор № 2 с концентрацией деривата флуфенацета (V) 10, 0 мкг/см3 (в пересчете на эквивалент флуфенацета I).
Из стандартного раствора № 1 отбирают пипеткой 1 см3, помещают в мерную колбу объемом 25 см3, доводят объем до метки ацетоном. Стандартный раствор № 2 используется для приготовления стандартных растворов для хроматографического исследования и хранится в холодильнике в течение 3 месяцев.
7.2.2.3. Стандартный раствор № 3 с концентрацией деривата флуфенацета (V) 1,0 мкг/см3 (в пересчете на эквивалент флуфенацета I).
Из стандартного раствора № 2 отбирают пипеткой 1 см3, помещают в мерную колбу объемом 10 см3, доводят объем до метки ацетоном. Стандартный раствор № 3 используется для приготовления стандартных растворов для хроматографического исследования и хранится в холодильнике в течение 14 суток.
7.2.2.4. Стандартный раствор № 4 с концентрацией деривата флуфенацета (V) 0,5 мкг/см3 (в пересчете на эквивалент флуфенацета I).
Из стандартного раствора № 3 отбирают пипеткой 5 см3, помещают в мерную колбу объемом 10 см3, доводят объем до метки ацетоном. Стандартный раствор № 4 используется для приготовления стандартных растворов для хроматографического исследования и хранится в холодильнике в течение 14 суток.
7.2.2.5. Стандартный раствор № 5 с концентрацией деривата флуфенацета (V) 0,2 мкг/см3 (в пересчете на эквивалент флуфенацета I).
Из стандартного раствора № 3 отбирают пипеткой 2 см3, помещают в мерную колбу объемом 10 см3, доводят объем до метки ацетоном. Стандартный раствор № 5 используется для установления градуировочной характеристики и хранится в холодильнике в течение 14 суток.
7.2.2.6. Стандартный раствор № 6 с концентрацией деривата флуфенацета (V) 0,1 мкг/см3 (в пересчете на эквивалент флуфенацета I).
Из стандартного раствора № 3 отбирают пипеткой 1 см3, помещают в мерную колбу объемом 10 см3, доводят объем до метки ацетоном. Стандартный раствор № 5 используется для установления градуировочной характеристики и хранится в холодильнике в течение 14 суток.
7.2.2.7. Стандартный раствор № 7 с концентрацией деривата флуфенацета (V) 0,05 мкг/см3 (в пересчете на эквивалент флуфенацета I).
Из стандартного раствора № 4 отбирают пипеткой 1 см3, помещают в мерную колбу объемом 10 см3, доводят объем до метки ацетоном. Стандартный раствор № 7 используется для установления градуировочной характеристики и хранится в холодильнике в течение 14 суток.
7.2.3. Приготовление растворов для внесения в контрольные образцы
7.2.3.1. Стандартный раствор А с концентрацией флуфенацета (I) 250 мкг/см3.
В мерную колбу вместимостью 100 см3 помещают 25,0 мг флуфенацета (I), добавляют 40 - 50 см3 метанола, перемешивают до полного растворения вещества и доводят объем до метки этим же растворителем. Раствор А хранится в холодильнике не более 3 месяцев.
7.2.3.2. Стандартный раствор В с концентрацией флуфенацета 5,0 мкг/см3.
Из стандартного раствора А отбирают пипеткой 1 см3, помещают в мерную колбу объемом 50 см3 и доводят объем до метки метанолом. Стандартный раствор В используется для внесения в контрольные образцы и хранится в холодильнике не более одного месяца.
7.2.3.3. Стандартный раствор С с концентрацией флуфенацета 0,5 мкг/см3.
Из стандартного раствора В отбирают пипеткой 1 см3, помещают в мерную колбу объемом 10 см3 и доводят объем до метки метанолом. Стандартный раствор С используется для внесения в контрольные образцы и хранится в холодильнике не более одного месяца.
7.3. Установление градуировочной характеристики
Градуировочную характеристику, выражающую отклик целевого иона (Response) от концентрации деривата флуфенацета (V) в растворе (мкг/см3), устанавливают путем определения соотношения интенсивности (площади) пиков, отвечающих характеристичным ионам идентифицируемого компонента и аналитического стандарта на регистрируемых ионных масс-хроматограммах по 4 растворам для градуировки с концентрацией 0,05; 0,1; 0,2; 0,5 мкг/см3. Для подтверждения обнаружения именно деривата флуфенацета используются еще два подтверждающих иона, относительная интенсивность которых должна попадать в правильный диапазон.
В испаритель хроматографа вводят по 1 мм3 каждого градуировочного раствора и анализируют в условиях хроматографирования по п. 9.4. Осуществляют не менее 5 параллельных измерений.
7.4. Подготовка концентрирующих патронов № 1 для
очистки
экстрактов и для концентрирования проб воды
Вся процедура подготовки происходит с использованием вакуума, скорость потока растворов через патрон не должна превышать 5 см3/мин (1 - 2 кап./с). Растворители должны быть элюированы в вакууме около - 2 кПа.
Патрон № 1 устанавливают на алонж с отводом для вакуума, сверху в патрон вставляют шприц с разъемом типа Люер объемом не менее 10 см3 (используют как емкость для элюентов).
7.4.1. Подготовка концентрирующих патронов № 1 для очистки экстракта
Концентрирующий патрон промывают сначала 5 см3 ацетона, затем 5 см3 воды. Элюировать каждый растворитель пока уровень жидкости не достигнет верхней границы сорбента. Элюаты отбрасывают. Нельзя допускать высыхания поверхности патрона.
7.4.2. Подготовка концентрирующих патронов № 1
для концентрирования проб воды
Концентрирующий патрон промывают сначала 5 см3 метанола, затем 15 см3 воды. Элюировать каждый растворитель пока уровень жидкости не достигнет верхней границы сорбента. Элюаты отбрасывают. Нельзя допускать высыхания поверхности патрона.
8. Отбор проб и хранение
Отбор проб производится в соответствии с «Унифицированными правилами отбора проб сельскохозяйственной продукции, продуктов питания и объектов окружающей среды для определения микроколичеств пестицидов» № 2051-79 от 21.08.79, а также в соответствии с ГОСТ Р 51592-2000 «Вода. Общие требования к отбору проб», ГОСТ 17.4.3.01-83 «Почвы. Общие требования к отбору проб», ГОСТ 28168-89 «Почвы. Отбор проб», ГОСТ 13586.3-83 «Зерно. Правила приемки и методы отбора проб», ГОСТ Р ИСО 6497-11 «Корма растительного происхождения. Методы отбора проб», ГОСТ 27853-88, ГОСТ 13341-77 «Свежие и свежемороженые овощи, картофель, бахчевые, фрукты, ягоды, грибы. Правила приемки и методы отбора проб», ГОСТ 7176-85 «Картофель свежий продовольственный, заготовляемый и поставляемый. ТУ».
Пробы воды хранят в стеклянной герметично закрытой таре в холодильнике при температуре 4 °С не более 10 суток.
Для длительного хранения проб почвы, почву подсушивают при комнатной температуре в отсутствие прямого солнечного света. Сухие почвенные образцы могут храниться в темной таре в течение года. Перед анализом сухую почву просеивают через сито с отверстиями диаметром 1 мм.
Отобранные пробы зерна и соломы подсушивают до стандартной влажности и хранят в бумажных или тканевых мешочках в сухом, хорошо проветриваемом шкафу, недоступном для грызунов.
Пробы клубней картофеля хранят в полиэтиленовой таре в морозильнике при температуре -18 °С.
9. Выполнение определения
9.1. Вода
9.1.1. Концентрирование пробы на концентрирующих патронах № 1
К пробе воды массой 1000 г добавляют 14 мл концентрированной соляной кислоты и тщательно перемешивают.
Пробу воды наносят на подготовленный по п. 7.4.2 концентрирующий патрон № 1. Флуфенацет элюируют с патрона 25 см3 метанола. Вся процедура происходит с использованием вакуума, скорость потока растворов через патрон не должна превышать 5 см3/мин (1 - 2 кап./с). Растворители должны быть элюированы в вакууме около - 2 кПа.
Элюат собирают в концентратор объемом 100 см3 и выпаривают досуха при температуре водяной бани не выше 25 - 30 °С.
К сухому остатку в концентраторе, полученному по п. 9.1.1, добавляют 75 см3 дистиллированной воды, обмывают стенки концентратора и помещают на 5 мин на аппарат для встряхивания проб. Затем в колбу добавляют 10 см3 1 н раствора серной кислоты, перемешивают смесь в течение 1 - 2 мин, прибавляют 0,3 г марганцово-кислого калия, перемешивают смесь в течение 5 мин, смесь приобретет фиолетовый цвет, 2,0 г бисульфита натрия, встряхнуть, смесь потеряет фиолетовый цвет. Затем в колбу аккуратно добавляют 50 см3 концентрированной серной кислоты. Реакционную смесь кипятят с обратным холодильником в течение 24 часов.
Примечание. Так как при добавлении кислоты образуется газ, эта процедура должна проводиться строго под тягой.
Необходимо обеспечить достаточный и постоянный приток воды к конденсатору для обеспечения полной конденсации паров при кипячении с обратным холодильником. Также необходимо обеспечить надежное подключение шлангов к водопроводной воде для предотвращения протечек.
Поскольку никакие горючие растворители не используются при кислотном гидролизе, кипячение ночью не представляет опасности.
9.1.3. Перегонка с водяным паром
Смесь, полученную по п. 9.1.2, остудить в течение 15 - 20 мин, затем осторожно добавить в колбу 350 см3 дистиллированной воды. Охладить колбу в емкости с дробленым льдом в течение 15 мин. Затем постепенно (порциями по 10 см3) в колбу добавить 100 см3 50 %-го раствора гидроксида натрия. Смесь необходимо постоянно перемешивать и охлаждать.
Проверить pH смеси, pH должно быть больше 12. При необходимости довести pH до значения больше 12 с помощью небольших порций (по 5 см3) 50 %-го раствора гидроксида натрия. Убрать колбу из ледяной бани. Перенести содержимое из этой колбы в двугорлую круглодонную колбу для перегонки с водяным паром.
В круглодонную колбу объемом 500 см3 (приемник для дистилляции) добавить 2 см3 концентрированной соляной кислоты и присоединить эту колбу к перегонку с водяным паром.
Дистиллировать смесь со скоростью отгонки дистиллята от 1,5 до 2,5 см3/мин. Когда будет собрано 150 - 200 см3 дистиллята позволить перегонке остыть в течение 10 - 15 мин и отсоединить приемник для дистилляции. При необходимости дистиллят можно хранить в холодильнике (0 - 5 °С) в течение 10 часов.
9.1.4. Экстракция фторанилина из дистиллята
Дистиллят, полученный по п. 9.1.3, переносят в делительную воронку объемом 500 см3. Исходную колбу обмывают 10 см3 дистиллированной воды и переносят в ту же делительную воронку.
Проверить pH, значение pH должно быть меньше 2. Если pH больше 2, необходимо добавить дополнительно концентрированной соляной кислоты до достижения pH < 2.
Подкисленную водную фракцию промывают 2 раза по 10 см3 хлористого метилена, каждый раз интенсивно встряхивая делительную воронку в течение 30 секунд. После полного разделения слоев выделившийся нижний (хлористого метилена) слой отбрасывают.
Водную фазу в делительной воронке подщелачивают с помощью 50 %-го раствора гидроксида натрия (~2,5 мл) до значения pH больше 10.
Фторанилин экстрагируют двумя порциями хлористого метилена объемом по 5 см3, каждый раз встряхивая делительную воронку в течение 30 секунд. После полного разделения фаз в делительной воронке нижний слой (хлористый метилен) собирают в мерную пробирку объемом 10 см3 через слой безводного сульфата натрия. Довести общий объем экстракта до 10 см3.
Примечание. Первые 5 см3 экстракта содержат основное количество фторанилина. Потеря даже небольшой части экстракта значительно сократит выход производного (деривата флуфенацета). Будьте осторожны в обращении с экстрактом.
При необходимости экстракт можно хранить в течение 10 часов в холодильнике(< 5 °С).
Примечание. Весь процесс должен быть проведен только в работающей тяге и завершен без промедления после его начала.
Аликвоту (1/2 раствора) хлористого метилена (5 см3), полученного по п. 9.1.4, переносят в чистую сухую мерную пробирку объемом 10 см3, добавить 10 мм3 концентрированной серной кислоты и 250 мм3 N, N-диметилформамида. Хорошо перемешать содержимое пробирки. Упарить хлористый метилен слабым потоком азота до объема менее 200 мм3. С помощью N, N-диметилформамида довести общий объем в пробирке до 300 мм3. Поместить пробирку в стакан с холодной водой, температура которой меньше 10 °С.
Примечание. Необходимо хлористый метилен упарить полностью. Остаточные количества хлористого метилена могут привести к образованию солей, и возможен неполный выход производного.
При помощи газонепроницаемого шприца в пробирку добавить 100 мм3 0,2 %-го раствора 4-(диметиламино)пиридина в пиридине, затем полученную смесь хорошо перемешать в ультразвуковой ванне.
Добавить в пробирку 300 мм3 трифторуксусного ангидрида по каплям с помощью газонепроницаемого шприца. Дать смеси постоять около 15 мин.
Примечание. Использовать трифторуксусный ангидрид только в работающей тяге.
Затем в пробирку осторожно, по каплям, добавить 3,0 см3 очищенной воды, слегка помешивая. Общий объем раствора довести очищенной водой до 8 см3. Вытащить пробирку из стакана с холодной водой, хорошо перемешать содержимое (при необходимости использовать ультразвуковую ванну).
9.1.6. Очистка экстракта на концентрирующих патронах № 1
Раствор, полученный в п. 9.1.5, наносят на подготовленный по п. 7.4.1 концентрирующий патрон № 1 с небольшой скоростью нанесения (давление - 2 кПа), элюат отбрасывают. Пробирку обмывают 2 см3 очищенной воды, наносят на патрон, элюат отбрасывают. Патрон промывают 5 см3 воды, элюат также отбрасывают. Высушить патрон под вакуумом в течение 15 мин (давление около - 4 кПа).
Дериват флуфенацета элюируют с патрона 4 см3 ацетона при скорости потока от 15 до 20 капель/мин. Собирают элюат в чистую мерную пробирку объемом 10 см3.
Примечание. Ацетон через патрон должен быть пропущен с нежным положительным давлением из шприца. Не использовать вакуум для элюирования ацетона через патрон.
Доводят общий объем в пробирке до 5 см3 ацетоном и 1 мм3 пробы вводят в хроматограф.
9.2. Почва, зерно пшеницы, клубни картофеля
9.2.1. Окисление и гидролиз
Образец почвы, измельченного зерна пшеницы или клубней картофеля массой 10 г помещают в круглодонную колбу со шлифом объемом 1000 см3, приливают 75 см3 дистиллированной воды и помещают на 60 минут на аппарат для встряхивания проб. Затем в колбу добавляют 10 см3 1 н раствора серной кислоты, перемешивают смесь в течение 1 - 2 мин, прибавляют 0,3 г марганцово-кислого калия, перемешивают смесь в течение 5 минут, смесь приобретет фиолетовый цвет, 2,0 г бисульфита натрия, встряхнуть, смесь потеряет фиолетовый цвет. Затем в колбу аккуратно добавляют 50 см3 концентрированной серной кислоты. Реакционную смесь кипятят с обратным холодильником в течение 24 часов.
Примечание. Так как при добавлении кислоты образуется газ, эта процедура должна проводиться строго под тягой.
Необходимо обеспечить достаточный и постоянный приток воды к конденсатору для обеспечения полной конденсации паров при кипячении с обратным холодильником. Также необходимо обеспечить надежное подключение шлангов к водопроводной воде для предотвращения протечек.
Поскольку никакие горючие растворители не используются при кислотном гидролизе, кипячение ночью не представляет опасности.
Далее проводят перегонку с водяным паром, экстракцию фторанилина из дистиллята, дериватизацию и очистку экстракта на концентрирующих патронах № 1, как указано в пунктах 9.1.3, 9.1.4, 9.1.5 и 9.1.6 соответственно.
9.3. Солома пшеницы
Образец измельченной соломы массой 5 г помещают в круглодонную колбу со шлифом объемом 1000 см3, приливают 150 см3 дистиллированной воды и помещают на 60 минут на аппарат для встряхивания проб. Затем в колбу добавляют 10 см3 1 н раствора серной кислоты, перемешивают смесь в течение 1 - 2 мин, прибавляют 0,3 г марганцовокислого калия, перемешивают смесь в течение 5 минут, смесь приобретет фиолетовый цвет, 2,0 г бисульфита натрия, встряхнуть, смесь потеряет фиолетовый цвет. Затем в колбу аккуратно добавляют 50 см3 концентрированной серной кислоты. Реакционную смесь кипятят с обратным холодильником в течение 24 часов.
Примечание. Так как при добавлении кислоты образуется газ, эта процедура должна проводиться строго под тягой.
Необходимо обеспечить достаточный и постоянный приток воды к конденсатору для обеспечения полной конденсации паров при кипячении с обратным холодильником. Также необходимо обеспечить надежное подключение шлангов к водопроводной воде для предотвращения протечек.
Поскольку никакие горючие растворители не используются при кислотном гидролизе, кипячение ночью не представляет опасности.
9.3.2. Перегонка с водяным паром
Смесь, полученную по п. 9.3.1, остудить в течение 15 - 20 минут, затем осторожно добавить в колбу 300 см3 дистиллированной воды. Охладить колбу в емкости с дробленым льдом в течение 15 минут. Затем постепенно (порциями по 10 см3) в колбу добавить 200 см3 50 %-го раствора гидроксида натрия. Смесь необходимо постоянно перемешивать и охлаждать.
Проверить pH смеси, pH должно быть больше 12. При необходимости довести pH до значения больше 12 с помощью небольших порций (по 10 см3) 50 %-го раствора гидроксида натрия. Убрать колбу из ледяной бани. Перенести содержимое из этой колбы в двугорлую круглодонную колбу для перегонки с водяным паром.
В круглодонную колбу объемом 500 см3 (приемник для дистилляции) добавить 2 см3 концентрированной соляной кислоты и присоединить эту колбу к перегонку с водяным паром.
Дистиллировать смесь со скоростью отгонки дистиллята от 1,5 до 2,5 см3/мин. Когда будет собрано 150 - 200 см3 дистиллята позволить перегонке остыть в течение 10 - 15 мин и отсоединить приемник для дистилляции. При необходимости дистиллят можно хранить в холодильнике (0 - 5 °С) в течение 10 часов.
Далее проводят экстракцию фторанилина из дистиллята, дериватизацию и очистку экстракта на концентрирующих патронах № 1, как указано в пп. 9.1.4, 9.1.5 и 9.1.6 соответственно.
9.4. Условия хроматографирования
Хроматографическая система, включающая:
- хроматограф газовый с электронным регулированием всех газовых потоков и возможностью управления параметрами газа-носителя в колонке, снабженный стандартным автосамплером с дозирующим объемом от 0,1 до 100 мм3 для автоматического ввода пробы в хроматографическую систему и масс-селективным детектором с высокопроизводительным турбомолекулярным насосом;
- компьютерное программное обеспечение, обслуживающее управление работой всего прибора, настройку и управление работой вакуумной системы, обеспечивающее сбор и хранение всех данных, поступающих с системы «газовый хроматограф - масс-селективный детектор», выполнение библиотечного поиска и количественный анализ.
Колонка хроматографическая капиллярная из кварцевого стекла с внутренний диаметром 0,25 мм, длиной 30 м, с неподвижной фазой, содержащей 5 % фенила и 95 % метилполисилоксана и толщиной пленки 0,25 мкм.
Температура испарителя - 200 °С, тип газа гелий, режим сплитлесс, давление 17,64 psi, суммарный поток 8,6 см3/мин, начало сброса 0,75 мин.
Температура термостата колонки программированная: начальная температура - 60 °С, выдержка 2 минуты, нагрев колонки по 15 °С в минуту до 250 °С, выдержка 1 мин, режим постоянный поток, поток через колонку 1,3 см3/мин, средняя скорость 29 см/с.
Температура устройства сопряжения масс-селективного детектора с хроматографом - 280 °С. Температура источника ионов 230 °С, температура квадруполя 150 °С. Относительное напряжение на электронном умножители 1518 В. Режим ионизации электронным ударом. Режим сбора данных SIM, целевой ион m/z 207, подтверждающие ионы m/z 138 и 249.
Объем вводимой пробы: 1 мм3.
Линейность детектирования сохраняется в пределах 0,05 - 0,5 нг.
Примечание. Для получения полной картины процесса гидролиза флуфенацета и его метаболитов до фторанилина рекомендуется провести холостой эксперимент с извлечением аналитического стандарта фторанилина по п. 9.1.3 «Перегонка с водяным паром» и хроматографировать по условиям хроматографирования п. 9.4. На основе полученных данных определяют полноту извлечения фторанилина из матрицы.
10. Обработка результатов анализа
Содержание деривата флуфенацета (V) в пересчете на эквивалент флуфенацета (I) в пробах воды, почвы, зерна и соломы зерновых колосовых культур, клубнях картофеля по пику деривата рассчитывают отдельно по формуле:
|
|
X - содержание флуфенацета, мг/кг;
Scm - высота (площадь) пика стандарта деривата флуфенацета (V);
Snp - высота (площадь) пика деривата флуфенацета (V) в образце, мВ;
А - концентрация стандартного раствора деривата флуфенацета (V), мкг/см3;
V - объем экстракта, подготовленного для хроматографирования, см3;
m - масса анализируемого образца, г (см3);
Р - содержание деривата флуфенацета (V) в аналитическом стандарте, %;
D - коэффициент пересчета с учетом отобранной аликвоты (равен 2,0).
11.
Проверка приемлемости результатов
параллельных определений
За результат анализа принимают среднее арифметическое результатов двух параллельных определений, расхождение между которыми не превышает предела повторяемости:
X1, Х2 - результаты параллельных определений, мг/кг или мг/дм3;
r - значение предела повторяемости (табл. 1), при этом r = 2,8×σr.
При невыполнении условия (1) выясняют причины превышения предела повторяемости, устраняют их и вновь выполняют анализ.
12. Оформление результатов
Результат анализа представляют в виде:
|
|
![]() - среднее арифметическое результатов
определений, признанных приемлемыми, мг/кг;
- среднее арифметическое результатов
определений, признанных приемлемыми, мг/кг;
Δ - граница абсолютной погрешности, мг/кг:
|
|
δ - граница относительной погрешности методики (показатель точности в соответствии с диапазоном концентраций, табл. 1), %.
В случае если содержание компонента менее нижней границы диапазона определяемых концентраций, результат анализа представляют в виде:
«содержание вещества в пробе менее 0,0005 мг/кг».*
________
* - 0,0005 мг/кг - предел обнаружения.
13. Контроль качества результатов измерений
Оперативный контроль погрешности и воспроизводимости измерений, а также контроль стабильности градуировочной характеристики осуществляется в соответствии с ГОСТ Р ИСО 5725-1-6-02 «Точность (правильность и прецизионность) методов и результатов измерений».
13.1. Контроль стабильности градуировочной характеристики.
Стабильность результатов измерений контролируют перед проведением измерений, анализируя один из градуировочных растворов.
Контроль стабильности градуировочной характеристики для деривата флуфенацета (V) проводят при смене основных градуировочных растворов № 1 и 2 каждые 3 месяца, при смене основных градуировочных растворов № 3, 4, 5, 6 и 7 - каждые 14 суток, а также в начале и окончании каждой серии анализов.
При контроле стабильности градуировочной характеристики проводят измерения не менее трех образцов концентраций для градуировки, содержание деривата флуфенацета (V) в которых должно охватывать весь диапазон концентраций от 0,05 до 0,5 мкг/см3.
Градуировочная характеристика считается стабильной, если для каждого из используемого для контроля градуировочного раствора сохраняется соотношение:
|
|
X - концентрация флуфенацета (по деривату) контрольного измерения, мкг/см3;
С - известная концентрация градуировочных растворов деривата флуфенацета (V) в ацетоне, взятая для контроля стабильности градуировочной характеристики, мкг/см3;
3,53 - погрешность градуировочной характеристики, %.
Если величина расхождения (А) превышает 3,53 %, делают вывод о невозможности применения градуировочной характеристики для дальнейших измерений. В этом случае выясняют и устраняют причины нестабильности градуировочной характеристики и повторяют контроль ее стабильности с использованием других градуировочных растворов деривата флуфенацета (V), предусмотренных МВИ. При повторном обнаружении нестабильности градуировочной характеристики определяют ее заново согласно п. 7.3.
13.2. Плановый внутрилабораторный оперативный контроль процедуры выполнения анализа проводится методом добавок.
Величина добавки Сд должна удовлетворять условию:
|
|
![]() - характеристика погрешности
(абсолютная погрешность) результатов анализа, соответствующая содержанию
компонента в испытуемом образце (расчетному значению содержания компонента в
образце с добавкой соответственно) мг/кг, при этом:
- характеристика погрешности
(абсолютная погрешность) результатов анализа, соответствующая содержанию
компонента в испытуемом образце (расчетному значению содержания компонента в
образце с добавкой соответственно) мг/кг, при этом:
|
Δл = ±0,84Δ, где |
Δ - граница абсолютной погрешности, мг/кг:
|
|
δ - граница относительной погрешности методики (показатель точности в соответствии с диапазоном концентраций, табл. 1), %.
Результат контроля процедуры Кк рассчитывают по формуле:
|
|
![]() - среднее арифметическое результатов
параллельных определений (признанных приемлемыми по п. 11), содержания
компонента в образце с добавкой, испытуемом образце и концентрация добавки
соответственно, мг/кг.
- среднее арифметическое результатов
параллельных определений (признанных приемлемыми по п. 11), содержания
компонента в образце с добавкой, испытуемом образце и концентрация добавки
соответственно, мг/кг.
Норматив контроля К рассчитывают по формуле:
|
|
Проводят сопоставление результата контроля процедуры (Кк) с нормативом контроля (К).
Если результат контроля процедуры удовлетворяет условию:
|
|Кк| ≤ К, |
(2) |
процедуру анализа признают удовлетворительной.
При невыполнении условия (2) процедуру контроля повторяют. При повторном невыполнении условия (2) выясняют причины, приводящие к неудовлетворительным результатам, и принимают меры по их устранению.
13.3. Проверка приемлемости результатов измерений, полученных в условиях воспроизводимости.
Расхождение между результатами измерений, выполненных в условиях воспроизводимости (разное время, разные операторы, разные лаборатории), не должно превышать предела воспроизводимости (R):
|
|
(3) |
X1, Х2 - результаты измерений в двух разных лабораториях, мг/кг;
R - предел воспроизводимости (в соответствии с диапазоном концентраций, табл. 1), %.
Приложение 1
|
Среда |
Внесено, мг/кг |
Обнаружено, мг/кг |
Полнота определения, % |
|
Вода |
0,0005 |
0,00036 ± 0,00001 |
72,0 |
|
0,001 |
0,00071 ± 0,00001 |
71,0 |
|
|
0,002 |
0,00143 ± 0,00001 |
71,6 |
|
|
0,005 |
0,00360 ± 0,0001 |
72,1 |
|
|
Почва |
0,05 |
0,0369 ± 0,0006 |
73,8 |
|
0,10 |
0,0720 ± 0,0015 |
72,0 |
|
|
0,20 |
0,1460 ± 0,0032 |
73,0 |
|
|
0,50 |
0,3633 ± 0,0042 |
72,7 |
|
|
Зерно пшеницы |
0,05 |
0,0364 ± 0,0008 |
72,8 |
|
0,10 |
0,0767 ± 0,0013 |
76,7 |
|
|
0,20 |
0,1490 ±0,0047 |
74,5 |
|
|
0,50 |
0,3805 ± 0,0098 |
76,1 |
|
|
Солома пшеницы |
0,1 |
0,0728 ± 0,0023 |
72,8 |
|
0,2 |
0,1483 ± 0,0045 |
74,1 |
|
|
0,5 |
0,2929 ± 0,0079 |
73,2 |
|
|
1,0 |
0,7572 ± 0,0108 |
75,7 |
|
|
Клубни картофеля |
0,05 |
0,0374 ± 0,0011 |
74,9 |
|
0,10 |
0,0742 ± 0,0011 |
74,2 |
|
|
0,20 |
0,1488 ± 0,0035 |
74,4 |
|
|
0,50 |
0,3621 ± 0,0064 |
72,4 |