 | Информационная система |  |
Государственное санитарно-эпидемиологическое нормирование
Российской Федерации
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
ОПРЕДЕЛЕНИЕ
ОСТАТОЧНЫХ
КОЛИЧЕСТВ ПЕСТИЦИДОВ
В ПИЩЕВЫХ ПРОДУКТАХ,
СЕЛЬСКОХОЗЯЙСТВЕННОМ СЫРЬЕ
И ОБЪЕКТАХ ОКРУЖАЮЩЕЙ СРЕДЫ
Сборник
методических указаний
МУК
4.1.2062 - 4.1.2074-06
Москва, 2009
1. Сборник подготовлен Федеральным научным центром гигиены им. Ф.Ф. Эрисмана (академик РАМН, проф. В.Н. Ракитский, проф. Т.В. Юдина); при участии специалистов Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека. Разработчики методов указаны в каждом из них.
2. Рекомендованы к утверждению Комиссией по государственному санитарно-эпидемическому нормированию при Федеральной службе по надзору в сфере защиты прав потребителей и благополучия человека.
3. Утверждены Главным государственным санитарным врачом Российской Федерации, Первым заместителем Министра здравоохранения Российской Федерации, академиком РАМН Г.Г. Онищенко.
4. Введены впервые.
Содержание
|
УТВЕРЖДАЮ |
|
Руководитель Федеральной службы |
|
по надзору в сфере защиты |
|
прав потребителей и благополучия |
|
населения, Главный государственный |
|
санитарный врач Российской Федерации |
|
Г.Г. Онищенко |
|
5 мая 2006 г. |
|
МУК 4.1.2064-06 |
|
Дата введения: 1.07.2006 |
МЕТОДИЧЕСКИЕ УКАЗАНИЯ
ПО ОПРЕДЕЛЕНИЮ ОСТАТОЧНЫХ КОЛИЧЕСТВ ХИЗАЛОФОП-П-ЭТИЛА
В ЗЕРНЕ ГОРОХА, СЕМЕНАХ И МАСЛЕ ПОДСОЛНЕЧНИКА
ПО ОСНОВНОМУ МЕТАБОЛИТУ ХИЗАЛОФОП-П КИСЛОТЕ
МЕТОДОМ КАПИЛЛЯРНОЙ ГАЗОЖИДКОСТНОЙ ХРОМАТОГРАФИИ
1. Вводная часть
1.1. Краткая характеристика препарата.
Фирма производитель: ЗАО «Фирма Август».
Торговое название: Миура, КЭ.
Действующее вещество (д.в.): хизалофоп-П-этил.
Название д.в. по номенклатуре ИЮПАК: (R)-2-[4-[(6-хлорхиноксалин-2-илокси)-фенокси] пропионовой кислоты этиловый эфир.
Структурная формула д.в.:

Эмпирическая формула д.в.: C19H17ClN2O4.
Молекулярная масса д.в.: 372,8.
Химически чистое вещество: светло-коричневые кристаллы.
Температура плавления д.в.: 76 - 77 °С.
Давление пара д.в. при 20 °С: 0,011 мПа.
Растворимость д.в. (г/л) при 20 °С: в воде - 0,0004, в гексане - 5,0 , этаноле - 22, ксилоле - 360, ацетоне - 650.
Стабильность д.в.: устойчив к действию света, разлагается до хизалофоп-П кислоты под действием разбавленных кислот и щелочей.
Острая пероральная токсичность препаратов (LD50) для крыс - 1180 - 1210 мг/кг, для мышей - 1750 - 1800 мг/кг. Не оказывает раздражающего действия на кожу.
Гигиенические нормативы: ВМДУ в горохе и масле подсолнечника - 0,05 мг/кг, семенах подсолнечника - 0,02 мг/кг.
1.2. Краткая характеристика хизалофоп-П кислоты
Название по номенклатуре ИЮПАК: (R)-2-[4-[(6-хлорхиноксалин-2-илокси)фенокси] пропионовая кислота.
Структурная формула:
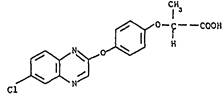
Эмпирическая формула д.в.: C17H13ClN2O4.
Молекулярная масса д.в.: 344,8.
2. Метод определения хизалофоп-П-этила в зерне гороха, семенах и масле подсолнечника по основному метаболиту хизалофоп-П кислоте с применением капиллярной газожидкостной хроматографии
2.1. Основные положения
2.1.1. Принцип метода.
Метод основан на количественном определении хизалофоп-П кислоты, основного метаболита хизалофоп-П-этила, и включает извлечение остаточных количеств хизалофоп-П кислоты из анализируемого объекта органическими растворителями, очистку экстракта перераспределением в системе несмешивающихся растворителей и метилирование хизалофоп-П кислоты диазометаном. Количественное определение проводят методом внешнего стандарта с применением капиллярной газожидкостной хроматографии и использованием термоионного детектора (ТИД).
2.1.2. Избирательность метода.
Метод специфичен в присутствии других применяемых в сельском хозяйстве пестицидов. Способы очистки экстрактов, а также применение селективного детектора и капиллярной колонки позволяет устранять влияние коэкстрактивных веществ на результаты анализа.
2.1.3. Метрологическая характеристика метода.
Диапазоны измеряемых концентраций, пределы обнаружения и другие метрологические параметры метода представлены в таблицах 1 и 2.
Метрологические параметры метода.
|
Метрологические параметры |
Анализируемые объекты: |
||
|
Зерно гороха |
Семена подсолнечника |
Масло подсолнечника |
|
|
Предел обнаружения, мг/кг |
0,01 |
0,01 |
0,025 |
|
Диапазон определяемых концентраций, мг/кг |
0,01 - 0,08 |
0,01 - 0,08 |
0,025 - 0,2 |
|
Среднее значение определения, % |
82,3 |
77,0 |
80,0 |
|
Стандартное отклонение, % |
4,5 |
5,9 |
6,2 |
|
Относительное стандартное отклонение, % |
2,7 |
3,3 |
3,7 |
Полнота определения хизалофоп-П кислоты в модельных пробах (n = 6)
|
Анализируемые объекты |
Внесено, мг/кг |
Извлечено, % |
Доверительный интервал среднего результата, % |
|
Зерно гороха |
0,01 |
77,3 |
±5,3 |
|
0,02 |
81,4 |
±4,6 |
|
|
0,04 |
83,7 |
±4,3 |
|
|
0,08 |
86,9 |
±3,7 |
|
|
Семена подсолнечника |
0,01 |
69,8 |
±6,7 |
|
0,02 |
75,3 |
±6,1 |
|
|
0,04 |
79,2 |
±5,8 |
|
|
0,08 |
83,5 |
±5,3 |
|
|
Масло подсолнечника |
0,025 |
75,5 |
±7,1 |
|
0,05 |
78,3 |
±6,5 |
|
|
0,1 |
82,2 |
±5,8 |
|
|
0,2 |
83,8 |
±5,4 |
2.2. Реактивы, растворы, материалы
Аналитический стандарт хизалофоп-П кислоты.
Азот газообразный высокой чистоты, ТУ 301-07-25-89.
Ацетон, осч, ТУ 2633-004-11291058-94.
Ацетонитрил для хроматографии, хч, ТУ 6-09-4326-76.
Вата медицинская, ТУ 9393-001-00302238-97.
Вода дистиллированная и перегнанная над KМnО4 и щелочью.
н-Гексан, хч, ТУ 6-09-3375-78.
Дихлорметан, хч, ТУ 6-09-2662-77.
Изооктан эталонный, ГОСТ 12433-83.
Калия гидроокись, чда, ГОСТ 24363-80.
Натрий сернокислый б/в (сульфат), чда, ГОСТ 4166-76.
Натрий хлористый, чда, ГОСТ 4233-77.
N-Нитрозометилмочевина, хч, ТУ 6-09-11-1643-82.
Серная кислота, осч, ГОСТ 14262-78.
Спирт этиловый ректификат (этанол), ГОСТ 17299-78.
Фильтры бумажные, красная лента, ТУ 2642-001-42624157-98.
Фильтры бумажные, белая лента, ТУ 2642-001-42624157-98.
Фильтры бумажные, синяя лента, ТУ 2642-001-42624157-98.
Эфир этиловый (серный), ОСТ 84-2006-88.
2.3. Приборы, аппаратура, посуда
Газовый хроматограф с ТИД.
Колонка хроматографическая капиллярная кварцевая длиной 15 м, внутренним диаметром 0,32 мм с неподвижной фазой SE-52, толщина слоя - 0,45 мкм.
Аппарат для встряхивания, ТУ 64-1-1081-73 или аналогичный.
Весы аналитические типа ВЛА-200, ГОСТ 34104-80.
Весы лабораторные типа ВЛКТ-500, ГОСТ 24104-80.
Воронки делительные емкостью 250 и 500 мл, ГОСТ 25336-82.
Воронки химические конусные, ГОСТ 25336-82.
Индикаторная бумага универсальная, ТУ 6-09-1181-76.
Колбы-концентраторы емкостью 100 и 250 мл, ГОСТ 25336-82.
Колбы плоскодонные емкостью 100 и 300 мл, ГОСТ 25336-82.
Колбы мерные со шлифом емкостью 25, 50, 100 мл, ГОСТ 1770-74.
Колпачки алюминиевые для герметизации флаконов, ГОСТ Р 51314-99.
Мельница электрическая лабораторная, ТУ 46-22-236-79 или аналогичная.
Микрошприц МШ-10, ТУ 2-833-106.
Насос водоструйный, ГОСТ 10696-75.
Ротационный вакуумный испаритель типа ИР-1 или аналогичный.
Пипетки мерные емкостью 1, 2, 5 и 10 мл, ГОСТ 20292-74.
Приспособление для обжима колпачков на флаконах, ТУ 42-2-2442-73.
Пробирки мерные со шлифом емкостью 5,0 мл, ГОСТ 1770-74.
Стаканы химические на 100, 200 и 500 мл, ГОСТ 25336-82.
Установка для перегонки растворителей при атмосферном давлении.
Установка для упаривания растворителей в токе азота.
Установка ультразвуковая «Серьга» УЗМ002 или аналогичная.
Флаконы стеклянные (типа пенициллиновых) емкостью 5,0 мл, ТУ 64-2-10-87.
Электроплитка, ГОСТ 14919-83.
2.4. Подготовка к определению
2.4.1. Подготовка и очистка растворителей.
Перед началом работы рекомендуется проверить чистоту применяемых органических растворителей. Для этого 100 мл растворителя упаривают в ротационном вакуумном испарителе при температуре +40 °С до объема 1,0 мл и хроматографируют. При обнаружении мешающих определению примесей очистку растворителей производят в соответствии с общепринятыми методиками.
2.4.2. Приготовление стандартных растворов.
Основной раствор хизалофоп-П кислоты с содержанием 100 мкг/мл готовят растворением в смеси ацетон:этанол (80:20) 0,01 г аналитического стандарта в мерной колбе емкостью 100 мл. Раствор хранят в холодильнике при температуре +4 - 6 °С не более трех месяцев.
Рабочие стандартные растворы с концентрациями 4,0, 2,0, 1,0 и 0,5 мкг/мл готовят из основного стандартного раствора хизалофоп-П кислоты соответствующим последовательным разбавлением ацетоном.
Для приготовления калибровочных растворов в мерные пробирки со шлифом емкостью 5,0 мл вносят по 1,0 мл рабочих растворов хизалофоп-П кислоты с концентрациями 0,5 , 1,0, 2,0 и 4,0 мкг/мл. Растворители в пробирках упаривают в токе азота досуха и проводят метилирование хизалофоп-П кислоты.
В пробирки добавляют по 2,0 мл свежеприготовленного эфирного раствора диазометана (п. 2.4.4), закрывают притертыми пробками и ставят на 12 - 14 часов (на ночь) в холодильник с температурой +4 - 6 °С. После этого этиловый эфир в пробирках упаривают досуха в токе азота при комнатной температуре. Сухой остаток растворяют в 1,0 мл изооктана и хроматографируют по п. 2.6.3.
2.4.3. Построение калибровочного графика.
Для построения калибровочного графика в инжектор хроматографа вводят по 2 мкл приготовленных по п. 2.4.2 растворов, содержащих хизалофоп-П кислоту (в виде хизалофоп-П-метила) в концентрациях 0,5, 1,0, 2,0 и 4,0 мкг/мл. Осуществляют не менее трех параллельных измерений и находят среднее значение высоты (площади) хроматографического пика для каждой концентрации. Строят калибровочный график зависимости высоты (площади) хроматографического пика в мм (мм2) от концентрации хизалофоп-П кислоты в рабочем растворе в мкг/мл.
2.4.4. Приготовление эфирного раствора диазометана (из расчета метилирования хизалофоп-П кислоты в экстрактах 2-х проб).
N-Нитрозометилмочевину массой 0,5 г помещают во флакон емкостью 2,0 - 3,0 мл и герметизируют резиновой пробкой и колпачком с помощью приспособления для обжима колпачков на флаконах. Этиловый эфир объемом 4,0 мл вносят в другой флакон емкостью 5,0 мл, герметизируют резиновой пробкой и колпачком и охлаждают в морозильной камере холодильника в течение 30 минут.
После этого флаконы через предварительно проколотые пробки соединяют гибкой тефлоновой трубкой (внутр. диам. ~ 1,5 - 2,0 мм), одним концом погружая ее в этиловый эфир на всю глубину (флакон с охлажденным этиловым эфиром обязательно должен еще иметь свободный выход в атмосферу). Во флакон с нитрозометилмочевиной, используя шприц с тонкой иглой и прокалывая пробку, добавляют по каплям по стенке 50 % водный раствор гидроокиси калия (~ 0,3 мл) до прекращения реакции. Этиловый эфир при насыщении диазометаном окрашивается в ярко желтый цвет.
Внимание! Приготовление эфирного раствора диазометана и процедуру метилирования необходимо обязательно проводить в работающем вытяжном шкафу.
2.5. Отбор, первичная обработка и хранение проб
Отбор проб зерна гороха проводят в соответствии с ГОСТ 28674-90 «Горох. Требования по заготовке и поставке», семян и масла подсолнечника - ГОСТ 10852-86 «Семена масличные. Правила приемки и методы отбора проб».
Среднюю пробу зерна гороха измельчают, перемешивают и выделяют аналитические пробы. Для длительного хранения аналитические пробы зерна гороха помещают в морозильную камеру с температурой -18 °С и хранят в закрытой стеклянной или полиэтиленовой таре.
Пробы семян подсолнечника просушивают до стандартной влажности и хранят в закрытой стеклянной или полиэтиленовой таре. Перед анализом семена подсолнечника вылущивают, измельчают на лабораторной мельнице и после перемешивания измельченной массы отбирают усредненную аналитическую пробу.
Пробы масла подсолнечника хранят в холодильнике при 0 - 4 °С в закрытой стеклянной таре не более 2-х месяцев.
2.6. Проведение определения
2.6.1. Зерно гороха и семена подсолнечника.
2.6.1.1. Экстрагирование и очистка экстракта.
Аналитическую пробу массой 25,0 ± 0,1 г помещают в плоскодонную колбу емкостью 300 мл и добавляют к пробе зерна гороха 150 мл смеси ацетон:этанол (80:20), а к пробе семян подсолнечника 150 мл смеси ацетон:этанол:бидистилированная вода (70:20:10). Содержимое колбы слегка встряхивают и подвергают обработке ультразвуком в УЗ-бане в течение 10 минут. После этого экстракт фильтруют через бумажный фильтр белая лента в колбу-концентратор емкостью 250 мл. Содержимое колбы с пробой промывают 50 мл ацетона, который также фильтруют в колбу-концентратор.
При использовании аппарата для встряхивания в колбу с аналитической пробой зерна гороха вносят 150 мл смеси ацетон:этанол (80:20), а к пробе семян подсолнечника добавляют 150 мл смеси ацетон:этанол:бидистилированная вода (70:20:10). Содержимое колбы встряхивают в течение 60 минут. Экстракт фильтруют через бумажный фильтр белая лента в колбу-концентратор емкостью 250 мл. Содержимое колбы с пробой промывают 50 мл ацетона, который также фильтруют в колбу-концентратор.
Колбу-концентратор с объединенным экстрактом подсоединяют к ротационному вакуумному испарителю и упаривают растворители до объема 10 - 20 мл при температуре +40 °С. В колбу-концентратор добавляют 200 мл бидистиллированной воды, 5,0 мл 10 % водного раствора гидроокиси калия, перемешивают встряхиванием и помещают в холодильник с температурой +4 - 6 °С на 2 часа. После этого содержимое колбы фильтруют через бумажный фильтр красная лента в делительную воронку емкостью 500 мл. К содержимому воронки добавляют 10 мл насыщенного водного раствора хлористого натрия, 75 мл дихлорметана и воронку встряхивают в течение 2-х минут. После 5-ти минутного отстаивания нижний дихлорметановый слой сливают и отбрасывают. Эту процедуру очистки экстракта повторяют с использованием 50 мл дихлорметана. Далее в воронку добавляют 40 мл насыщенного водного раствора хлористого натрия, приливают 75 мл н-гексана и встряхивают содержимое воронки в течение 2-х минут. После 5-ти минутного отстаивания нижний водный слой собирают в химический стакан емкостью 300 мл, а верхний гексановый слой сливают и отбрасывают.
Водный раствор пробы, находящийся в химическом стакане, подкисляют концентрированной серной кислотой до pH 2,0 и переносят в чистую делительную воронку емкостью 500 мл. В воронку добавляют 75 мл смеси гексан:этиловый эфир (80:20) и встряхивают в течение 2-х минут. После полного разделения слоев нижний водный слой сливают в химический стакан, а верхний гексано-эфирный слой фильтруют через фильтр синяя лента со слоем безводного сульфата натрия (толщина слоя ~ 1,0 - 1,5 см) в колбу-концентратор емкостью 150 мл. Экстрагирование и фильтрование повторяют с использованием 50 мл смеси гексан:этиловый эфир (80:20). Нижний водный слой отбрасывают.
Колбу-концентратор с объединенным экстрактом подсоединяют к ротационному вакуумному испарителю и упаривают растворители до объема 3 - 5 мл при температуре +40 °С. Остаток экстракта количественно переносят из колбы-концентратора в мерную пробирку со шлифом емкостью 5,0 мл и упаривают растворители досуха в токе азота при температуре +50 °С.
2.6.1.2. Метилирование.
После охлаждения до комнатной температуры в пробирку с сухим остатком добавляют 2,0 мл свежеприготовленного эфирного раствора диазометана (по п. 2.4.4). Пробирку закрывают притертой пробкой и ставят на 12 - 14 часов (на ночь) в холодильник с температурой +4 - 6 °С. После этого этиловый эфир в пробирке упаривают досуха в токе азота при комнатной температуре. Сухой остаток растворяют в 0,5 мл изооктана и проводят количественное определение хизалофоп-П кислоты по п. 2.6.3.
2.6.2. Масло подсолнечника.
2.6.2.1. Экстрагирование и очистка экстракта.
Аналитическую пробу масла массой 10,0 ± 0,1 г растворяют в 50 мл гексана (насыщенного ацетонитрилом) в плоскодонной колбе емкостью 100 мл и после этого гексановый раствор масла переносят в делительную воронку емкостью 250 мл. Колбу промывают 50 мл ацетонитрила (насыщенного гексаном) и также переносят его в воронку. Содержимое воронки встряхивают в течение 2-х минут. После 5-ти минутного отстаивания нижний ацетонитрильный слой сливают в колбу-концентратор емкостью 250 мл. В делительную воронку добавляют еще 50 мл ацетонитрила (насыщенного гексаном). Содержимое воронки встряхивают в течение 2-х минут, отстаивают и нижний ацетонитрильный слой объединяют в колбе-концентраторе с предыдущим. Верхний гексановый слой отбрасывают.
Колбу-концентратор с объединенным ацетонитрильным экстрактом подсоединяют к ротационному вакуумному испарителю и упаривают растворитель до объема 10 - 20 мл при температуре +50 °С. В колбу-концентратор добавляют 200 мл дистиллированной воды, 5,0 мл 10 % водного раствора гидроокиси калия, раствор перемешивают встряхиванием и выдерживают 2 часа в холодильнике с температурой +4 - 6 °С. После этого содержимое колбы фильтруют через бумажный фильтр белая лента в делительную воронку емкостью 500 мл. К содержимому воронки добавляют 10 мл насыщенного водного раствора хлористого натрия, 75 мл дихлорметана и воронку встряхивают в течение 2-х минут. После 5-ти минутного отстаивания нижний дихлорметановый слой сливают и отбрасывают. Эту процедуру очистки экстракта повторяют два раза с использованием каждый раз по 50 мл дихлорметана. Далее в воронку добавляют 40 мл насыщенного водного раствора хлористого натрия, приливают 75 мл н-гексана и встряхивают содержимое воронки в течение 2-х минут. После 5-ти минутного отстаивания нижний водный слой собирают в химический стакан емкостью 300 мл, а верхний гексановый слой сливают и отбрасывают.
Водный раствор пробы, находящийся в химическом стакане, подкисляют концентрированной серной кислотой до pH 2,0 и переносят в чистую делительную воронку емкостью 500 мл. В воронку добавляют 75 мл смеси гексан:этиловый эфир (80:20) и встряхивают в течение 2-х минут. После полного разделения слоев нижний водный слой сливают в химический стакан, а верхний гексано-эфирный слой фильтруют через фильтр синяя лента со слоем безводного сульфата натрия (толщина слоя ~ 1,0 - 1,5 см) в колбу-концентратор емкостью 150 мл. Экстрагирование и фильтрование повторяют с использованием 50 мл смеси гексан:этиловый эфир (80:20). Нижний водный слой отбрасывают.
Колбу-концентратор с объединенным экстрактом подсоединяют к ротационному вакуумному испарителю и упаривают растворители до объема 3 - 5 мл при температуре +40 °С. Остаток экстракта количественно переносят из колбы-концентратора в мерную пробирку со шлифом емкостью 5,0 мл и упаривают растворители досуха в токе азота при температуре +50 °С.
2.6.2.2. Метилирование.
После охлаждения до комнатной температуры в пробирку с сухим остатком добавляют 2,0 мл свежеприготовленного эфирного раствора диазометана (по п. 2.4.4). Пробирку закрывают притертой пробкой и ставят на 12 - 14 часов (на ночь) в холодильник с температурой +4 - 6 °С. После этого этиловый эфир в пробирке упаривают досуха в токе азота при комнатной температуре. Сухой остаток растворяют в 0,5 мл изооктана и проводят количественное определение хизалофоп-П кислоты по п. 2.6.3.
2.6.3. Условия хроматографирования.
Газовый хроматограф с ТИД.
Колонка хроматографическая капиллярная кварцевая длиной 15 м, внутренним диаметром 0,32 мм с неподвижной фазой SE-52, толщина слоя - 0,45 мкм.
Температура колонки: программирование от 180 °С (1 мин) до 280 °С (15 мин) со скоростью 10 °С/мин.
Температура испарителя: 250 °С.
Температура детектора: 290 °С.
Расход газов: газа-носителя (гелий марки «А») - 2,5 см3/мин, водорода и воздуха к ТИД - 30 и 250 см3/мин соответственно, дополнительного газа (гелий марки «А») к ТИД - 30 см3/мин.
Объем вводимой пробы: 2 мкл.
Время удерживания хизалофоп-П кислоты (в виде производного): 13,2 ± 0,1 мин.
Предел детектирования: 0,25 нг.
Линейный диапазон детектирования: 0,5 - 4,0 нг.
2.6.4. Обработка результатов анализа.
Содержание хизалофоп-П кислоты рассчитывают методом внешнего стандарта по формуле:
![]()
X - содержание хизалофоп-П кислоты в пробе, мг/кг,
H - высота (площадь) пика анализируемого вещества, мм (мм2),
Hст - высота (площадь) пика стандартного вещества, мм (мм2),
А - концентрация стандартного рабочего раствора хизалофоп-П кислоты, мкг/мл,
V - количество экстракта, подготовленного для хроматографирования, мл,
m - масса (г) аналитической пробы.
Пересчет на содержание хизалофоп-П-этила (X1) проводят по формуле: X1 = 1,08 × X.
3. Требования техники безопасности
Необходимо соблюдать общепринятые правила техники безопасности при работе с органическими растворителями, токсичными веществами, электронагревательными приборами и сжатыми газами, а также требования, изложенные в документации к приборам.
4. Контроль погрешности измерений
Оперативный контроль погрешности и воспроизводимости результатов измерений осуществляется в соответствии с ГОСТ ИСО 5725-1 - 6-2002 «Точность (правильность и прецизионность) методов и результатов измерений».
5. Разработчики.
П.А. Тарарин, Т.А. Маханькова, Л.В. Григорьева, Е.И. Кожемякова (ВНИИ защиты растений).