Информационная система |
| Карта сайта |
Скачать ГОСТ ISO 10993-6-2011 Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 6. Исследования местного действия после имплантации
Дата актуализации: 10.08.2017

 ГОСТ ISO 10993-6-2011
ГОСТ ISO 10993-6-2011
Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 6. Исследования местного действия после имплантации
| Обозначение: |  ГОСТ ISO 10993-6-2011 ГОСТ ISO 10993-6-2011 |
| Обозначение англ: |  10993-6-2011 10993-6-2011 |
| Статус: | действует |
| Название рус.: | Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 6. Исследования местного действия после имплантации |
| Название англ.: | Medical devices. Biological evaluation of medical devices. Part 6. Tests for local effects after implantation |
| Дата добавления в базу: | 01.10.2014 |
| Дата актуализации: | 05.05.2017 |
| Дата введения: | 01.01.2013 |
| Область применения: | Стандарт устанавливает методы исследования местного действия после имплантации материалов, предназначенных для использования в медицинских изделиях. Стандарт применим к следующим материалам: - твердые монолитные и биостабильные; - деградируемые и (или) резорбируемые (рассасывающиеся); - пористые материалы, жидкости, пасты и порошкообразные. Исследуемые образцы имплантируют в участки тела и ткани животного, которые пригодны для оценки биологической безопасности материала. Предлагаемые имплантационные методы не предназначены для оценки механических или функциональных свойств материалов. Стандарт применим к медицинским изделиям, используемым местно по клиническим показаниям, для оценки реакции окружающих тканей при возможном нарушении целостности изделия. |
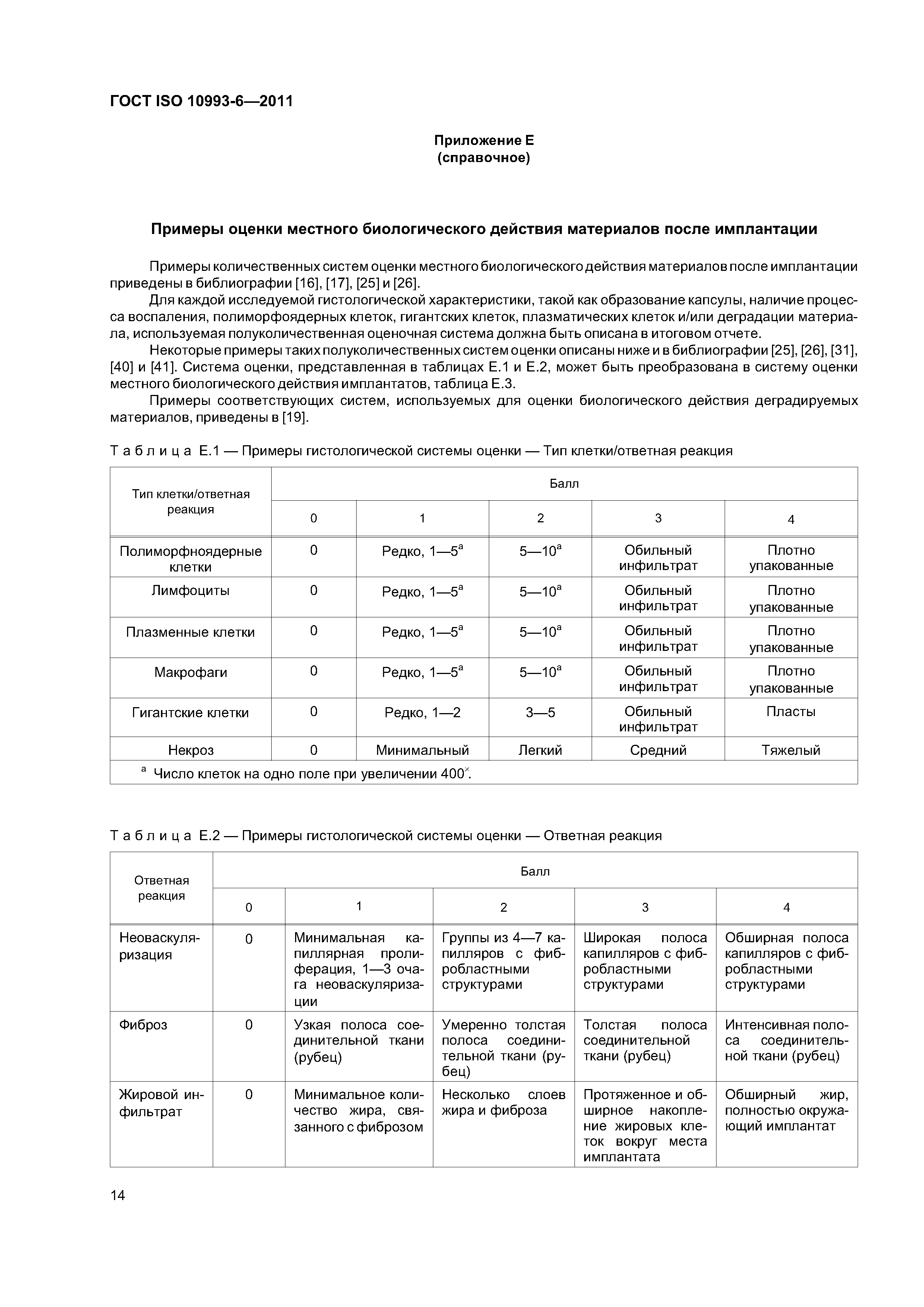
| Оглавление: | 1 Область применения 2 Нормативные ссылки 3 Термины и определения 4 Основные положения об имплантационных методах исследования 4.1 Общие сведения 4.2 Подготовка объектов исследования для имплантации 5 Методы исследования, основные аспекты 5.1 Природа тканей в области имплантации образцов 5.2 Вид экспериментального животного 5.3 Продолжительность эксперимента 5.4 Условия хирургического вмешательства и эксперимента 5.5 Оценка результатов 6 Отчет об исследовании Приложение А (справочное) Общие положения о влиянии сроков имплантации и тканевой реакции на процессы деградации и резорбции материалов Приложение В (обязательное) Методы имплантации в подкожную ткань Приложение С (обязательное) Метод имплантации в мышечную ткань Приложение D (обязательное) Метод имплантации в костную ткань Приложение Е (справочное) Примеры оценки местного биологического действия материалов после имплантации Библиография Приложение ДА (справочное) Сведения о соответствии межгосударственных стандартов ссылочным международным стандартам |
| Разработан: | ФГУП ВНИИНМАШ |
| Утверждён: | 29.11.2011 Межгосударственный Совет по стандартизации, метрологии и сертификации (Inter-Governmental Council on Standardization, Metrology, and Certification 40) 13.12.2011 Федеральное агентство по техническому регулированию и метрологии (1309-ст) |
| Издан: | Стандартинформ (2013 г. ) |
| Расположен в: | |
| Нормативные ссылки: |
|























© 2013 Ёшкин Кот :-) Карта сайта
 ГОСТ ISO 10993-12-2011 «Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 12. Приготовление проб и контрольные образцы»
ГОСТ ISO 10993-12-2011 «Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 12. Приготовление проб и контрольные образцы»