Информационная система |
| Карта сайта |
Скачать ГОСТ Р 54329-2011 Сводный комплект технической документации для демонстрации соответствия существенным принципам обеспечения безопасности и основных функциональных характеристик медицинских изделий
Дата актуализации: 10.08.2017

 ГОСТ Р 54329-2011
ГОСТ Р 54329-2011
Сводный комплект технической документации для демонстрации соответствия существенным принципам обеспечения безопасности и основных функциональных характеристик медицинских изделий
| Обозначение: |  ГОСТ Р 54329-2011 ГОСТ Р 54329-2011 |
| Обозначение англ: |  GOST R 54329-2011 GOST R 54329-2011 |
| Статус: | действует |
| Название рус.: | Сводный комплект технической документации для демонстрации соответствия существенным принципам обеспечения безопасности и основных функциональных характеристик медицинских изделий |
| Название англ.: | Summary technical documentation for demonstrating conformity to the essential principles of safety and performance of medical devices |
| Дата добавления в базу: | 01.09.2013 |
| Дата актуализации: | 05.05.2017 |
| Дата введения: | 01.03.2012 |
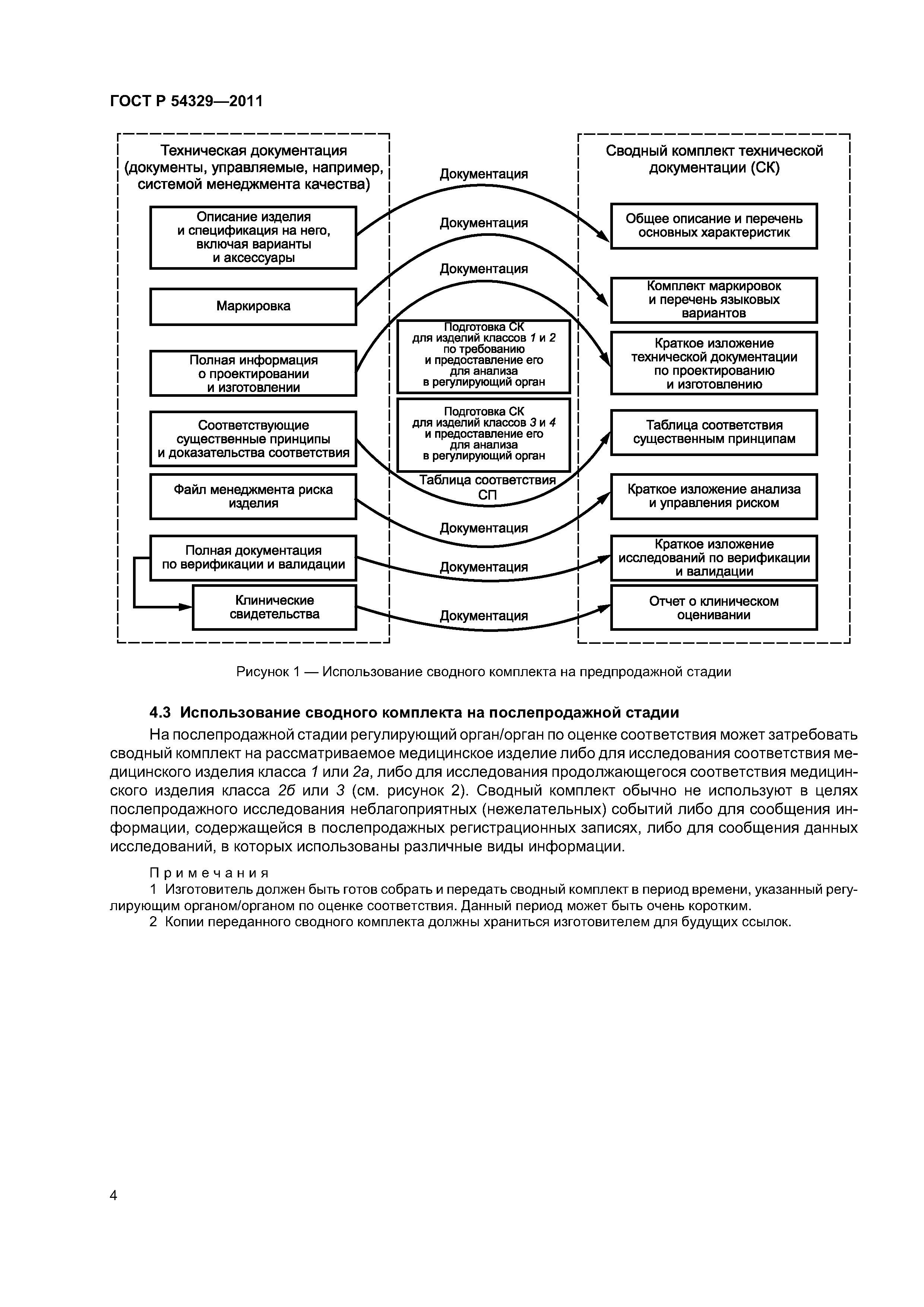
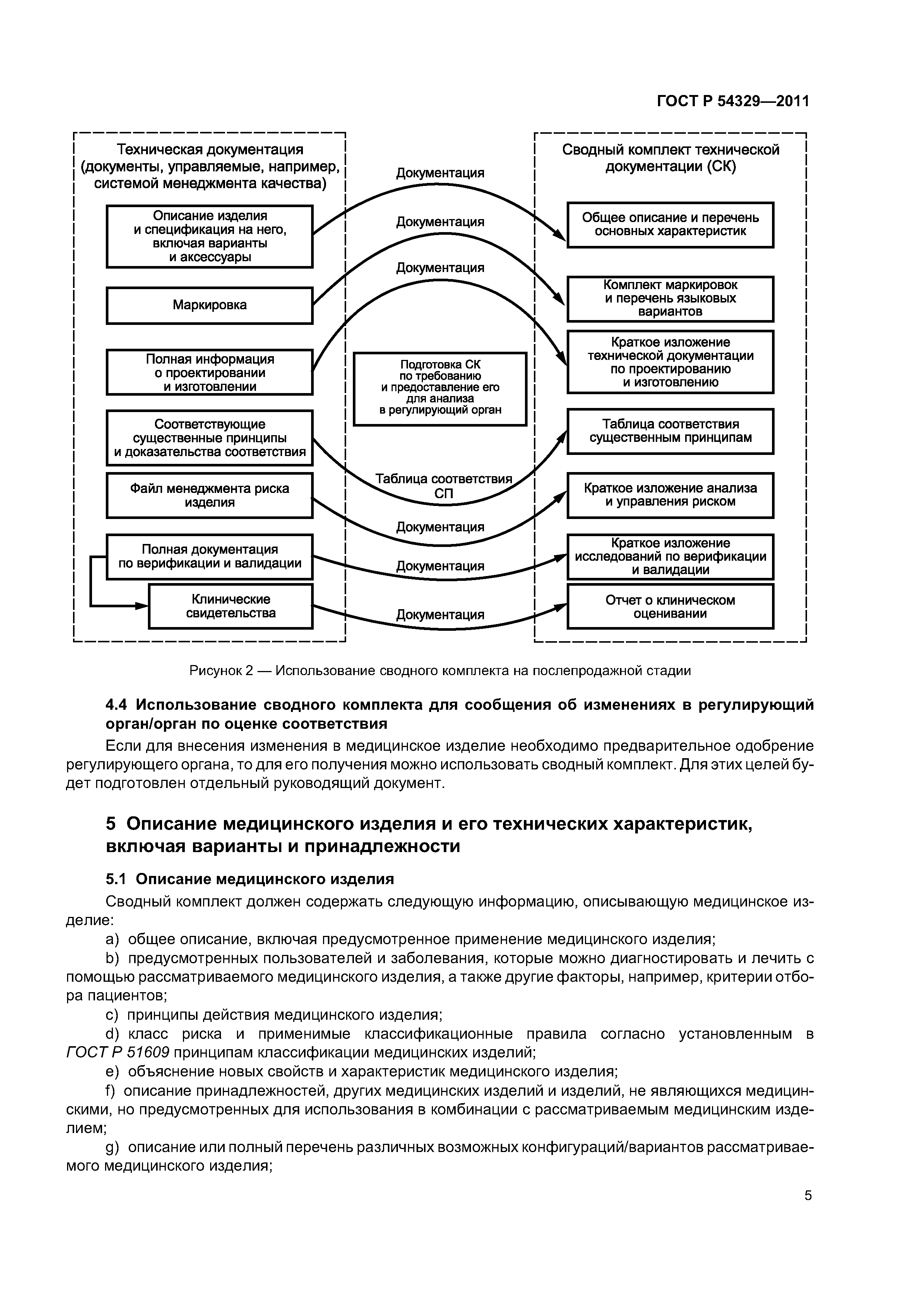
| Область применения: | Изготовитель медицинских изделий должен подготовить техническую документацию на свои изделия и поддерживать ее в рабочем состоянии, а также обеспечивать своевременный доступ к данной технической документации, демонстрирующей, как было разработано, спроектировано и изготовлено медицинское изделие. Данная техническая документация, обычно управляемая системой менеджмента качества изготовителя, часто является обширной и делится на части, которые могут находиться, например, в разных структурных подразделениях или на разных производственных площадках. Следует отметить, что как для регулирующего органа или органа по оценке соответствия, так и для и регулируемых отраслей промышленности удобно, если для выполнения установленных действий по оценке соответствия вместо полной технической документации используется сводный комплект технической документации на рассматриваемое изделие. Сводный комплект должен быть подготовлен в установленной регулирующими требованиями суммарной или сокращенной форме, со степенью детализации, достаточной для регулирующего органа или органа по оценке соответствия. Документы, содержащиеся в данном комплекте должны быть частью полной технической документации, хранящейся у изготовителя и позволяющей ему демонстрировать, что медицинское изделие, к которому относится данная техническая документация, соответствует существенным принципам обеспечения безопасности и основных функциональных характеристик медицинских изделий (ГОСТ Р ИСО/ТО 16142). Наличие сводного комплекта помогает уменьшить различия в требованиях к документации, имеющиеся в разных юрисдикциях, сокращая таким образом финансовые затраты на достижение соответствия регулирующим требованиям и помогая пациентам получить доступ к новым технологиям и методикам лечения. |
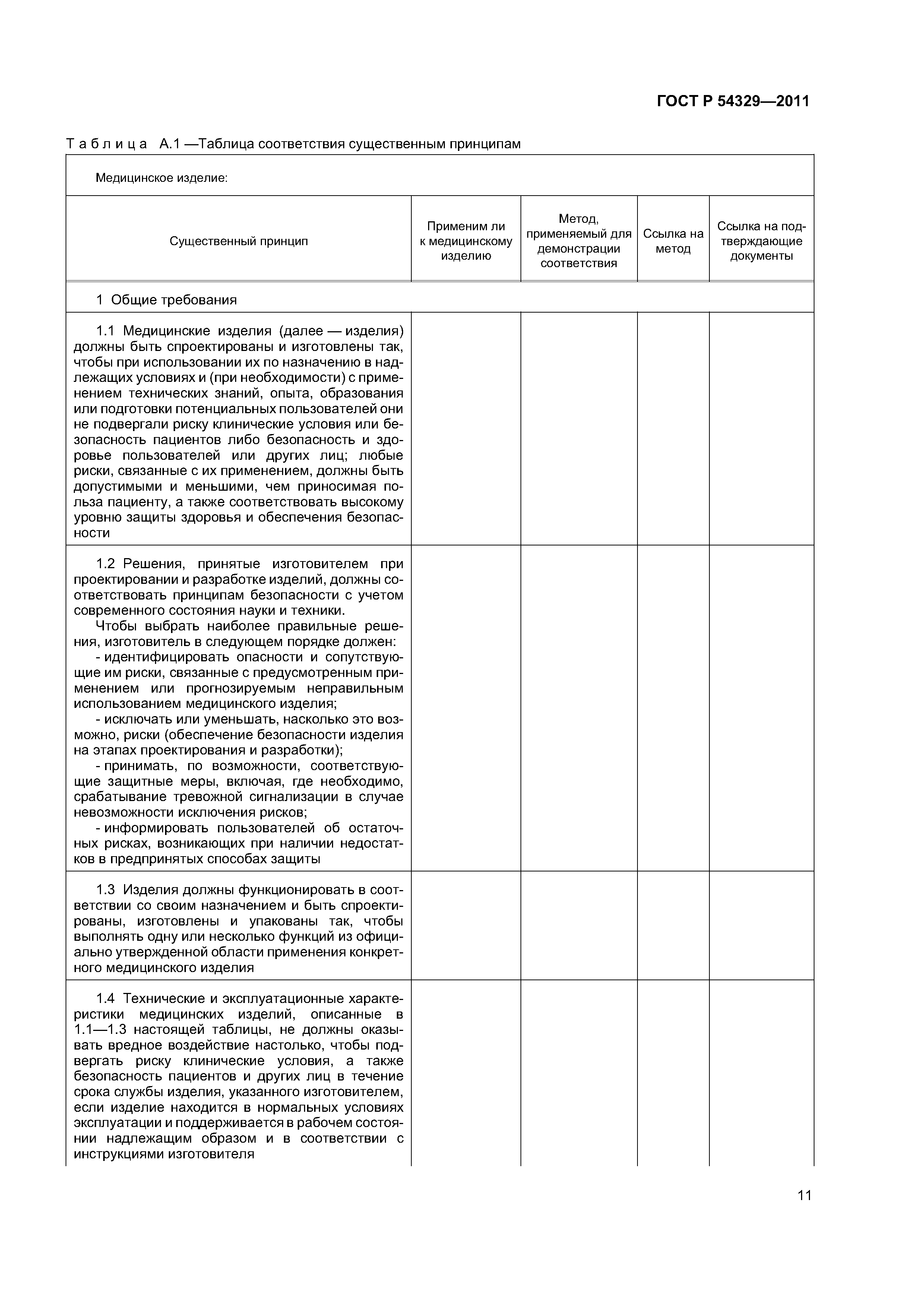
| Оглавление: | 1 Область применения 1.1 Обоснование 1.2 Цель 1.3 Область применения 2 Нормативные ссылки 3 Термины и определения 4 Подготовка и использование сводного комплекта 4.1 Подготовка 4.2 Использование сводного комплекта на предпродажной стадии 4.3 Использование сводного комплекта на послепродажной стадии 4.4 Использование сводного комплекта для сообщения об изменениях в регулирующий орган/орган по оценке соответствия 5 Описание медицинского изделия и его технических характеристик, включая варианты и принадлежности 5.1 Описание медицинского изделия 5.2 Техническое описание медицинского изделия 5.3 Ссылка на подобные и предыдущие варианты медицинского изделия 6 Маркировка 7 Информация по проектированию и производству 7.1 Проектирование медицинского изделия 7.2 Производственные процессы 7.3 Производственные площадки 8 Таблица соответствия существенным принципам 9 Основные результаты анализа и управления риском 10 деятельность по верификации и валидации 10.1 Общие положения 10.2 Биологическая совместимость 10.3 Лекарственные средства 10.4 Биологическая безопасность 10.5 Стерилизация 10.6 Верификация и валидация программного обеспечения 10.7 Исследования на животных 10.8 Клиническое свидетельство 11 Формат сводного комплекта 12 Декларация соответствия. Приложение А (справочное) Таблица соответствия существенным принципам Приложение ДА (справочное) Сведения о соответствии ссылочных национальных стандартов международным стандартам, использованным в качестве ссылочных в примененном международном документе |
| Разработан: | ЗАО МЕДИ-ТЕСТ |
| Утверждён: | 15.06.2011 Федеральное агентство по техническому регулированию и метрологии (127-ст) |
| Издан: | Стандартинформ (2011 г. ) |
| Расположен в: | |
| Нормативные ссылки: |
|
















© 2013 Ёшкин Кот :-) Карта сайта
 ГОСТ Р ИСО 15223-2002 «Медицинские изделия. Символы, применяемые при маркировании на медицинских изделиях, этикетках и в сопроводительной документации»
ГОСТ Р ИСО 15223-2002 «Медицинские изделия. Символы, применяемые при маркировании на медицинских изделиях, этикетках и в сопроводительной документации»