 | Информационная система |  |
Государственное санитарно-эпидемиологическое
нормирование
Российской Федерации
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение остаточных количеств
галаксифоп-Р-метила в зерне гороха,
гречихе, капусте белокочанной и
корнеплодах моркови методом
капиллярной газожидкостной
хроматографии
Методические указания
МУК 4.1.3326-15
Москва 2016
1. Разработаны сотрудниками ФГБНУ «Всероссийский НИИ защиты растений» Федерального агентства научных организаций (В.И. Долженко, С.Е. Маслаков) и ООО «Инновационный центр защиты растений» (И.А. Цибульская, В.Ф. Павлова).
2. Рекомендованы к утверждению Комиссией по государственному санитарно-эпидемиологическому нормированию Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (протокол от 17 декабря 2015 г. № 2).
3. Утверждены руководителем Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, Главным государственным санитарным врачом Российской Федерации А.Ю. Поповой 28 декабря 2015 г.
4. Введены впервые.
СОДЕРЖАНИЕ
|
УТВЕРЖДАЮ Руководитель
Федеральной службы А.Ю. Попова 28 декабря 2015 г. |
4.1. МЕТОДЫ КОНТРОЛЯ. ХИМИЧЕСКИЕ ФАКТОРЫ
Определение остаточных количеств
галаксифоп-Р-метила в зерне гороха, гречихе, капусте
белокочанной и корнеплодах моркови методом
капиллярной газожидкостной хроматографии
Методические указания
МУК 4.1.3326-15
Свидетельство о метрологической аттестации № 01.5.04.201/01.00043/2015. Настоящие методические указания устанавливают порядок применения метода капиллярной газожидкостной хроматографии для определения остаточных количеств галаксифоп-Р-метила в зерне гречихи, капусте белокочанной, корнеплодах моркови в диапазоне концентраций 0,01 - 0,10 мг/кг, в зерне гороха - 0,025 - 0,25 мг/кг.
Методические указания носят рекомендательный характер.
Галаксифоп-Р-метил
((R)-2-[4-(3-хлоро-5-трифторометил-2-пиридилокси)фенокси]пропионовой кислоты метиловый эфир (ИЮПАК)
Структурная формула:
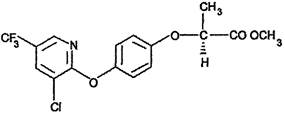
Эмпирическая формула: C16H13ClF3NO4.
Молекулярная масса: 375,7.
Химически чистый метиловый эфир галоксифоп-Р кислоты представляет собой светло-коричневую жидкость или почти бесцветную жидкость.
Давление пара при 25 °С: 0,328 мПа.
Температура кипения: свыше 280 °С.
Коэффициент перераспределения н-октанол-вода: Kow logP = 4,0.
Растворимость: в воде - 9,08 мг/дм3 (при 20 °С); в ацетоне, циклогексане, хлороформе, метиловом спирте, этаноле, толуоле, ксилоле - свыше 1000 г/дм3.
Стабильность: стабилен к воздействию света, воздуха, нагревания до 300 °С. Гидролизуется до галаксифоп-Р кислоты в воде, кислых и щелочных средах. В биологических средах гидролизуется до галоксифоп-Р кислоты в течение 4 - 8 дней в зависимости от вида растений.
Галоксифоп-Р кислота
(R)-2-[4-(3-хлоро-5-трифторометил-2-пиридилокси)фенокси]пропионовая кислота.
Структурная формула:
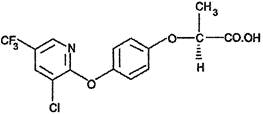
Эмпирическая формула: C15H11ClF3NO4.
Молекулярная масса: 361,7.
Химически чистое вещество: белый кристаллический порошок.
Температура плавления: 107 - 108 °С.
Давление пара при 25 °С: 0,0035 мПа.
Растворимость при 25 °С: в воде - 375 мг/дм3, хорошо растворяется в большинстве органических растворителей.
Краткая токсикологическая характеристика. Острая пероральная токсичность LD50 для крыс 300 - 623 мг/кг, острая дермальная токсичность LD50 для крыс - 2000 мг/кг. Оказывает незначительное раздражающее действие на слизистую глаз кролика. Побочные отрицательные эффекты не обнаружены.
Область применения препарата. Послевсходовый гербицид для применения на широколистных культурах (свекле, картофеле, масличных, бобовых и других культурах) для борьбы с одно- и многолетними травами.
Гигиенические нормативы для галаксифоп-Р-метила в России: МДУ для свеклы сахарной, подсолнечника (семена), сои (бобы), масла растительного - 0,05 мг/кг; рапса - 0,2 мг/кг; картофеля - 0,01 мг/кг; для гороха, капусты белокочанной, корнеплодов моркови и гречихи - не установлен.
1. Погрешность измерений
При соблюдении всех регламентированных условий проведения анализа в точном соответствии с данной методикой погрешность (и ее составляющие) результатов измерений при доверительной вероятности Р = 0,95 не превышает значений, приведенных в табл. 1, для соответствующих диапазонов концентраций.
Таблица 1
Метрологические параметры
|
Анализируемый объект |
Диапазон определяемых концентраций, мг/кг |
Показатель точности* (границы относительной погрешности) (Р = 0,95), ±δ, % |
Показатель повторяемости (среднеквадратическое отклонение повторяемости), σr, % |
Показатель воспроизводимости (среднеквадратическое отклонение воспроизводимости), σR, % |
Предел повторяемости (значение допустимого расхождения. между двумя результатами параллельных определений), r, % |
Предел воспроизводимости (значение допустимого расхождения между двумя результатами измерений, полученными в разных лабораториях), R, % (Р = 0,95) |
|
Зерно гороха |
0,025 - 0,25 |
23 |
8 |
12 |
22 |
34 |
|
Корнеплоды моркови |
0,01 - 0,1 |
22 |
7 |
11 |
20 |
31 |
|
Капуста белокочанная |
0,01 - 0,1 |
22 |
7 |
И |
20 |
31 |
|
Гречиха |
0,01 - 0,1 |
23 |
8 |
12 |
22 |
34 |
|
* Соответствует расширенной неопределенности Uотн. при коэффициенте охвата k = 2 |
||||||
Таблица 2
Полнота извлечения галаксифоп-Р-метила, стандартное
отклонение,
доверительный интервал среднего результата
|
Анализируемый объект |
Метрологические параметры, Р = 0,95, n = 20 |
||||
|
предел количественного определения, мг/кг |
диапазон определяемых концентраций, мг/кг |
полнота извлечения вещества, % |
стандартное отклонение, % |
доверительный интервал среднего результата, % |
|
|
Зерно гороха |
0,025 |
0,025 - 0,25 |
73,3 |
5,2 |
2,27 |
|
Корнеплоды моркови |
0,01 |
0,01 - 0,1 |
75,0 |
4,8 |
2,10 |
|
Капуста белокочанная |
0,01 |
0,01 - 0,1 |
81,2 |
4,3 |
1,88 |
|
Гречиха |
0,01 |
0,01 - 0,1 |
79,5 |
5,1 |
2,23 |
2. Метод измерений
Методика основана на определении галаксифоп-Р-метила методом капиллярной газожидкостной хроматографии с использованием электронозахватного детектора (ЭЗД) после его омыления и экстракции галоксифоп-Р кислоты из проб водно-метанольным раствором, очистке в системе несмешивающихся растворителей и на патронах для твердофазной экстракции.
Идентификация галаксифоп-Р-метила проводится по времени удерживания, количественное определение - методом абсолютной калибровки.
Избирательность метода обеспечивается сочетанием условий подготовки проб и хроматографирования.
3. Средства измерений, реактивы,
вспомогательные устройства и материалы
3.1. Средства измерений
|
Газовый хроматограф с электронозахватным (ЭЗД) детектором, снабженный автоматическим пробоотборником |
|
|
Весы аналитические с пределом взвешивания до 210 г и пределом допускаемой погрешности 0,1 мг |
ГОСТ Р 53228-08 |
|
Весы технические с пределом взвешивания до 150 г и пределом допускаемой погрешности 0,1 г |
ГОСТ Р 53228-08 |
|
Колбы мерные на 10, 100 см3 |
|
|
Микродозаторы одноканальные переменного объема от 100 до 1000 мм3 и от 1 до 5 см3 |
|
|
Газовый хроматограф с электронозахватным (ЭЗД) детектором, снабженный автоматическим пробоотборником |
|
|
Микрошприц вместимостью 10 мм3 |
|
|
Колбы мерные на 10, 50, 100 и 1000 см3 |
|
|
Цилиндры мерные на 50, 100 и 250 см3 |
Примечание. Допускается использование средств измерения с аналогичными или лучшими характеристиками.
3.2. Реактивы
|
Галаксифоп-Р-метил, аналитический стандарт с содержанием основного компонента 99,0 % |
ТУ 6-09-3534-87 |
|
Ацетонитрил, хч |
ТУ 6-21-39-96 |
|
Азот газообразный, осч, в баллонах |
|
|
Вода бидистиллированная, деионизированная |
ТУ 6-09-3375-78 |
|
Гексан, хч |
|
|
Гидроксид калия, чда |
|
|
Кислота соляная, хч |
ТУ 6-09-2662-77 |
|
Метилен хлористый, хч |
|
|
Метиловый спирт, хч |
|
|
Гидроксид натрия, хч |
|
|
Натрий сернокислый безводный, хч |
|
|
Натрий хлористый, хч |
ТУ 6-09-11-1643-82 |
|
N-нитрозометилмочевина |
ТУ 6-09-3534-87 |
|
Раствор № 1 (гексан-этилацетат в соотношении 9:1) |
|
|
Хлороформ, чда |
|
|
Этилацетат, чда |
|
|
Эфир диэтиловый, хч |
Примечание. Допускается использование реактивов с более высокой квалификацией, не требующих дополнительной очистки растворителей.
3.3. Вспомогательные устройства и материалы
|
Воронки делительные емкостью 100 и 250 см3 |
|
|
Воронки химические конусные |
|
|
Колбы круглодонные на шлифе объемом 10, 50, 100 и 250 см3 |
|
|
Колбы плоскодонные конические вместимостью 100 см3 |
|
|
Патроны, заполненные гидрофильным слабокислотным сорбентом на основе силикагеля |
ТУ 4215-002-0545-931-94 |
|
Стаканы полипропиленовые центрифужные с крышками объемом 100 см3 |
|
|
Ротационный вакуумный испаритель с мембранным насосом, с пределом вакуума до 10 мбар |
|
|
Центрифуга с максимальной рабочей частотой вращения 4000 об./мин. |
|
|
Устройство перемешивающее (50 - 200 колебаний в минуту) |
|
|
Ультразвуковая ванна с рабочей частотой 35 кГц |
|
|
Установка для перегонки растворителей |
|
|
Установка для синтеза диазометана |
|
|
Установка для твердофазной экстракции |
|
|
Фильтры бумажные обезжиренные средней плотности |
ТУ 6.091678-86 |
|
Хроматографическая капиллярная кварцевая колонка длиной 30 м, внутренним диаметром 0,32 мм, с неподвижной жидкой фазой из диметилполисилоксана (толщина пленки 0,25 мкм) |
|
Примечание. Допускается применение оборудования с аналогичными или лучшими техническими характеристиками.
4. Требования безопасности
4.1. При выполнении измерений необходимо соблюдать требования техники безопасности при работе с химическими реактивами по ГОСТ 12.1.007-76, требования по электробезопасности при работе с электроустановками по ГОСТ 12.1.019-09, а также требования, изложенные в технической документации на газовый хроматограф.
4.2. Помещение лаборатории должно быть оборудовано приточно-вытяжной вентиляцией, соответствовать требованиям пожарной безопасности по ГОСТ 12.1.004-91 и иметь средства пожаротушения по ГОСТ 12.4.009-83. Содержание вредных веществ в воздухе не должно превышать ПДК (ОБУВ), установленных ГН 2.2.5.1313-03 и ГН 2.2.5.2308-07.
Организация обучения работников безопасности труда - по ГОСТ 12.0.004-90.
5. Требования к квалификации операторов
Измерения в соответствии с настоящей методикой может выполнять специалист-химик, имеющий опыт работы на газовом хроматографе, ознакомленный с руководством по эксплуатации хроматографа, освоивший данную методику и подтвердивший экспериментально соответствие получаемых результатов нормативам контроля погрешности измерений по п. 13.
6. Условия измерений
При выполнении измерений выполняют следующие условия:
- процессы приготовления растворов и подготовки проб к анализу проводят при температуре воздуха (20 ± 5) °С и относительной влажности не более 80 %;
- выполнение измерений на газовом хроматографе проводят в условиях, рекомендованных технической документацией к прибору.
7. Подготовка к определению
Измерениям предшествуют следующие операции: очистка органических растворителей (при необходимости), приготовление градуировочных растворов и раствора внесения, установление градуировочной характеристики, приготовление смесей растворителей, растворов для экстракции и очистка экстрактов, подготовка патрона для ТФЭ и проверка поведения галаксифоп-Р-метила на патроне.
7.1. Кондиционирование колонки
Перед началом анализа кварцевую капиллярную колонку кондиционируют в токе азота при температуре термостата колонки 280 °С не менее 30 мин.
7.2. Кондиционирование патрона для твердофазной экстракции
Патрон промывают 3 см3 раствора № 1, затем 3 см3 гексана.
7.3. Подготовка растворителей и приготовление растворов
7.3.1. Подготовка растворителей. Растворители, используемые для анализа, специальной подготовки не требуют. Рекомендуется проверить чистоту применяемых растворителей. При обнаружении примесей, которые могут мешать определению, растворители очищают общепринятыми методами.
7.3.2. 20 %-й раствор гидроксида натрия: 100 г гидроксида натрия помещают в колбу на 500 см3 и растворяют в 400 см3 бидистиллированной воды. Раствор можно хранить в течение недели в темной герметично закрытой посуде.
7.3.3. Раствор № 1 (гексан-этилацетат в соотношении 9:1). 450 см3 гексана помещают в мерную колбу на 500 см3 и добавляют 50 см3 этилацетата, перемешивают. Раствор хранят при комнатной температуре в течение 3 месяцев.
7.3.4. Насыщенный раствор хлористого натрия в воде. 320 г хлористого натрия растворяют в 1 дм3 дистиллированной воды. Раствор можно хранить при комнатной температуре в течение недели.
7.3.5. 6 N раствор соляной кислоты. В мерную колбу на 500 см3 помещают 250 см3 концентрированной соляной кислоты и доводят до метки водой, перемешивают. Раствор можно хранить при комнатной температуре в течение месяца

Рис. 1. Прибор для получения диазометана:
1 - реакционный сосуд;
2 - переходник с капельницей;
3 - холодильник;
4 - переходник;
5 - насадка с отводом;
6 - приемная колба
7.3.6. 50 %-й раствор гидроксида калия готовят растворением 50 г гидроксида калия в 50 см3 воды. Раствор следует использовать в день приготовления.
7.3.7. Приготовление раствора диазометана в эфире. В круглодонную колбу на 100 см3 помещают 15 см3 50 %-го водного раствора гидроксида калия и 15 см3 диэтилового эфира. Смесь охлаждают до 5 °С, затем при взбалтывании прибавляют 5 г N-нитрозометилмочевины. Колбу присоединяют к холодильнику, нижний конец которого снабжен аллонжем с отводом, проходящим через резиновую пробку и погруженным в слой диэтилового эфира (40 мл) на дне приемника. Приемник охлаждают смесью льда и соли.
Реакционную колбу погружают в водяную баню, нагревают до 30 °С. Отгонку прекращают, как только перестают идти пузырьки газа через слой диэтилового эфира в приемнике.
7.4. Приготовление основного и градуировочных растворов
7.4.1. Основной раствор с концентрацией 0,1 мг/см3: точную навеску галаксифоп-Р-метила (10 ± 0,2)мг помещают в мерную колбу вместимостью 100 см3, растворяют в 50 - 60 см3 гексана и доводят объем до метки гексаном, тщательно перемешивают.
7.4.2. Раствор галаксифоп-Р-метила № 1 с концентрацией 1,0 мкг/см3 для градуировки: в мерную колбу вместимостью 100 см3 вносят 1,0 см3 основного раствора и доводят до метки гексаном, тщательно перемешивают.
7.4.3. Рабочие растворы галаксифоп-Р-метила № 2 - 5 с концентрацией 0,01 - 0,1 мкг/см3 для градуировки: в 4 мерные колбы вместимостью 100 см3 помещают 1,0; 2,0; 5,0 и 10,0 см3 раствора № 1 и доводят до метки гексаном, тщательно перемешивают. Получают рабочие растворы с концентрациями гапаксифоп-Р-метила 0,01; 0,02; 0,05 и 0,1 мкг/см3.
Основной и градуировочные растворы можно хранить в холодильнике при температуре 0 - 4 °С в течение месяца.
При изучении полноты извлечения галаксифоп-Р-метила используют смеси, приготовленные из основного раствора методом последовательного разбавления по объему ацетонитрилом.
7.5. Построение градуировочного графика
Для установления градуировочной характеристики (площадь пика - концентрация галаксифоп-Р-метила в растворе) в хроматограф вводят по 1 мм3 градуировочных растворов (не менее 3 параллельных измерений для каждой концентрации, не менее 4 точек по диапазону измеряемых концентраций). Затем измеряют площади пиков и строят график зависимости среднего значения площади пика от концентрации галаксифоп-Р-метила в градуировочном растворе.
Методом наименьших квадратов рассчитывают градуировочный коэффициент (K) в уравнении линейной регрессии:
|
C = KS, где |
S - площадь пика градуировочного раствора.
Градуировку признают удовлетворительной, если значение коэффициента линейной корреляции оказывается не ниже 0,99.
Градуировочную характеристику необходимо проверять при замене реактивов, хроматографической колонки или элементов хроматографической системы, а также при отрицательном результате контроля градуировочного коэффициента.
Градуировочную зависимость признают стабильной при выполнении следующего условия:
|
|
С - аттестованное значение массовой концентрации галаксифоп-Р-метила в градуировочном растворе,
СK - результат контрольного измерения массовой концентрации галаксифоп-Р-метила в градуировочном растворе,
λконтр. - норматив контроля градуировочного коэффициента, % (λконтр. = 10 % При Р = 0,95).
7.6. Проверка хроматографического поведения
галаксифоп-Р-метила
на патроне для твердофазной экстракции
На подготовленный патрон вносят 1 см3 стандартного раствора галаксифоп-Р-метила с концентрацией 0,1 мкг/см3 (п. 7.2). Промывают патрон 3 см3 гексана, элюат отбрасывают. Затем элюируют галаксифоп-Р-метил раствором № 1 со скоростью 1 - 2 капли в секунду. Отбирают фракции по 2 см3, упаривают досуха, растворяют в 1 см3 гексана и анализируют по п. 9.5.
Фракции, содержащие галаксифоп-Р-метил, объединяют и вновь анализируют.
Устанавливают концентрацию вещества в элюате, определяют полноту смывания с патрона и необходимый для очистки объем элюента.
Примечание. Проверку хроматографического поведения галаксифоп-Р-метила следует проводить обязательно, поскольку профиль вымывания может изменяться при использовании новой партии патронов и растворителей.
8. Отбор проб и хранение
Отбор проб производится в соответствии с «Унифицированными правилами отбора проб сельскохозяйственной продукции, пищевых продуктов и объектов окружающей среды для определения микроколичеств пестицидов» (№ 2051-79 от 21.08.79) а также в соответствии с ГОСТ Р 51809-01 «Капуста белокочанная, свежая, реализуемая в розничной торговой сети. Технические условия»; ГОСТ 1721-85 «Морковь столовая свежая, заготовляемая и поставляемая»; ГОСТ 28674-90 «Горох. Требования при заготовках и поставках»; ГОСТ 19092-92 «Гречиха. Требования при заготовках и поставках».
Пробы моркови и капусты хранят в морозильной камере при температуре -18 °С. Для длительного хранения зерна гороха и гречихи подсушивают при комнатной температуре в отсутствие прямого солнечного света. Сухие образцы могут храниться в течение года. Перед анализом пробы гороха и гречихи доводят до стандартной влажности и измельчают. Пробы моркови и капусты перед анализом, не размораживая, измельчают на терке или в гомогенизаторе.
9. Проведение определения
9.1. Омыление и экстракция галаксифоп-Р кислоты из проб
Навеску измельченной пробы (20 г) помещают в центрифужный стакан на 100 см3, добавляют 10 см3 20 %-го раствора гидроксида натрия в 50 см3 метилового спирта, плотно закрывают крышкой, встряхивают на механическом встряхивателе в течение 30 мин и центрифугируют 10 мин (n = 4000 об./мин). Содержимое колбы фильтруют в коническую колбу емкостью 250 см3 методом декантации через бумажный фильтр средней плотности. Экстракцию повторяют 10 см3 20 %-го раствора гидроксида натрия в 50 см3 метилового спирта. Объединенный экстракт подвергают очистке по п. 9.2.
9.2.
Очистка экстракта в системе
несмешивающихся растворителей
9.2.1. Экстракты моркови и капусты.
К полученному раствору добавляют 50 см3 насыщенного раствора хлористого натрия, подкисляют 6 N раствором соляной кислоты до pH 1 - 2 (примерно 15 см3) и переносят в делительную воронку на 250 см3. В делительную воронку добавляют 50 см3 хлористого метилена, воронку встряхивают. После разделения фаз нижний слой фильтруют, пропуская через фильтр средней плотности со слоем безводного сернокислого натрия в круглодонную колбу на 250 см3. Экстракцию повторяют еще два раза. Экстракты объединяют и упаривают досуха на ротационном вакуумном испарителе при температуре бани не выше 40 °С.
9.2.2. Экстракты зерна гороха.
Из экстракта отбирают аликвоту 20 - 25 см3, добавляют 10 см3 насыщенного раствора хлористого натрия, 25 см3 дистиллированной воды, подкисляют 6 N раствором соляной кислоты до pH 1 - 2 (примерно 4 см3) и переносят в делительную воронку на 100 см3. В делительную воронку добавляют 25 см3 хлороформа, воронку встряхивают. После разделения фаз нижний слой фильтруют, пропуская через фильтр средней плотности со слоем безводного сернокислого натрия в круглодонную колбу на 250 см3. Экстракцию повторяют еще два раза. Экстракты объединяют и упаривают досуха на ротационном вакуумном испарителе при температуре бани не выше 40 °С.
9.2.3. Экстракты гречихи.
К полученному раствору добавляют 50 см3 насыщенного раствора хлористого натрия, подкисляют 6 N раствором соляной кислоты до pH 1 - 2 (примерно 15 см3) и переносят в делительную воронку на 250 см3. В делительную воронку добавляют 50 см3 хлористого метилена, воронку встряхивают. После разделения фаз нижний слой фильтруют, пропуская через фильтр средней плотности со слоем безводного сернокислого натрия в круглодонную колбу на 250 см3. Экстракцию повторяют еще два раза. Экстракты объединяют и упаривают досуха на ротационном вакуумном испарителе при температуре бани не выше 40 °С.
9.3. Метилирование галаксифоп-Р кислоты
Сухой остаток, полученный по пп. 9.1 - 9.2, растворяют в 3 см3 свежеприготовленного раствора диазометана в диэтиловом эфире и оставляют на 30 мин. Затем испаряют остатки диазометана и диэтилового эфира в токе теплого воздуха.
9.4. Очистка на патроне для твердофазной экстракции
Сухой остаток, полученный по пп. 9.1 - 9.3, растворяют в 1 см3 гексана и вносят на предварительно кондиционированный патрон (п. 7.2), колбу ополаскивают 1 см3 гексана и также наносят на патрон. Патрон промывают 3 см3 гексана, элюат отбрасывают. Галаксифоп-Р-метал элюируют 5 см3 раствора № 1, элюат собирают, упаривают досуха на ротационном вакуумном испарителе при температуре бани не выше 40 °С, остаток растворяют в 1 - 2 см3 гексана и 1 мм3 вводят в хроматограф.
9.5. Условия хроматографирования
Газовый хроматограф с детектором электронного захвата. Капиллярная кварцевая колонка длиной 30 м, внутренним диаметром 0,32 мм с толщиной слоя неподвижной фазы диметилполисилоксана 0,25 мкм. Температура колонки: программирование от 150 °С (1 мин) до 300 °С со скоростью 20 °С/мин. Температура испарителя: 300 °С. Температура детектора: 320 °С. Расход газа носителя (азот) - 20 см3/мин (0,75 мин - 1 см3/мин без разделения потока, деление потока 20:1). Объем вводимой пробы: 1 мкл. Время удерживания галаксифоп-Р-метила составляет (7,5 ± 0,1) мин.
10. Обработка результатов анализа
Количественное определение проводят методом абсолютной калибровки. Содержание галаксифоп-Р-метила в пробе (X, мг/кг) вычисляют по формуле:
|
|
Sx - площадь пика галаксифоп-Р-метила на хроматограмме испытуемого образца, мм2 (AU);
K - градуировочный коэффициент, найденный на стадии построения соответствующей градуировочной зависимости;
V - объем пробы, подготовленной для хроматографического анализа, см3;
Р - навеска анализируемого образца, г.
Содержание остаточных количеств галаксифоп-Р-метила в образце вычисляют как среднее из двух параллельных определений.
Образцы, дающие пики большие, чем стандартный раствор галаксифоп-Р-метила с концентрацией 1,0 мкг/см3, разбавляют гексаном.
11.
Проверка приемлемости результатов
параллельных определений
За результат анализа принимают среднее арифметическое результатов двух параллельных определений, расхождение между которыми не превышает предела повторяемости (1):
|
|
(1) |
Х1, Х2 - результаты параллельных определений, мг/кг;
r - значение предела повторяемости (r = 2,8σr).
При невыполнении условия (1) выясняют причины превышения предела повторяемости, устраняют их и вновь выполняют анализ.
12. Оформление результатов
Результат анализа представляют в виде:
|
( |
![]() - среднее арифметическое результатов
определений, признанных приемлемыми, мг/кг;
- среднее арифметическое результатов
определений, признанных приемлемыми, мг/кг;
Δ - граница абсолютной погрешности, мг/кг;
|
|
δ - граница относительной погрешности методики (показатель точности в соответствии с диапазоном концентраций), %.
В случае если содержание компонента меньше нижней границы диапазона определяемых концентраций, результат анализа представляют в виде:
«содержание вещества в пробе менее нижней границы определения» (например: менее 0,01 мг/кг*, где *- 0,01 мг/кг - предел обнаружения галаксифоп-Р-метила в корнеплодах моркови).
13. Контроль качества результатов измерений
Оперативный контроль погрешности и воспроизводимости измерений осуществляется в соответствии с ГОСТ Р ИСО 5725-1 - 6-02 «Точность (правильность и прецизионность) методов и результатов измерений».
13.1. Стабильность результатов измерений контролируют перед проведением измерений, анализируя один из градуировочных растворов.
13.2. Плановый внутрилабораторный оперативный контроль процедуры выполнения анализа проводится с применением метода добавок.
Величина добавки Сд должна удовлетворять условию:
|
Сд = Δл,Х + Δл,Х′, где |
±Δл,Х (±Δл,Х′) - характеристика погрешности (абсолютная погрешность) результатов анализа, соответствующая содержанию компонента в испытуемом образце (расчетному значению содержания компонента в образце с добавкой соответственно), мг/кг; при этом:
|
Δл = ±0,84Δ, где |
Δ - граница абсолютной погрешности, мг/кг:
|
|
δ - граница относительной погрешности методики (показатель точности в соответствии с диапазоном концентраций), %.
Результат контроля процедуры Кк рассчитывают по формуле:
|
Кк
= |
![]() ′, Х, Сд
- среднее арифметическое результатов параллельных определений (признанных
приемлемыми по п. 11)
содержания компонента в образце с добавкой, испытуемом образце, концентрация
добавки соответственно, мг/кг.
′, Х, Сд
- среднее арифметическое результатов параллельных определений (признанных
приемлемыми по п. 11)
содержания компонента в образце с добавкой, испытуемом образце, концентрация
добавки соответственно, мг/кг.
Норматив контроля К рассчитывают по формуле:
Проводят сопоставление результата контроля процедуры (Кк) с нормативом контроля (К).
Если результат контроля процедуры удовлетворяет условию
|
|Кк| ≤ К, |
(2) |
процедуру анализа признают удовлетворительной.
При невыполнении условия (2) процедуру контроля повторяют. При повторном невыполнении условия (2) выясняют причины, приводящие к неудовлетворительным результатам, и принимают меры к их устранению.
13.3. Проверка приемлемости результатов измерений, полученных в условиях воспроизводимости.
Расхождение между результатами измерений, выполненных в двух разных лабораториях, не должно превышать предела воспроизводимости (R):
|
|
(3) |
X1, Х2 - результаты измерений в двух разных лабораториях, мг/кг;
R - предел воспроизводимости (в соответствии с диапазоном концентраций), %.