Информационная система |
| Карта сайта |
Скачать ПР 64-05-001-2002 Правила организации чистых производств и контроля качества изделий медицинского назначения из полимеров, тканых и нетканых материалов, имеющих контакт с кровью
Дата актуализации: 10.08.2017


 ПР 64-05-001-2002
ПР 64-05-001-2002
Правила организации чистых производств и контроля качества изделий медицинского назначения из полимеров, тканых и нетканых материалов, имеющих контакт с кровью
| Обозначение: |   ПР 64-05-001-2002 ПР 64-05-001-2002 |
| Обозначение англ: |   PR 64-05-001-2002 PR 64-05-001-2002 |
| Статус: | действует |
| Название рус.: | Правила организации чистых производств и контроля качества изделий медицинского назначения из полимеров, тканых и нетканых материалов, имеющих контакт с кровью |
| Название англ.: | Regulations for Organization of Clean Production Facilities and Quality Control of Medical Products Made of Polymer, Fabric, and Non-Fabric Materials Coming Into Contact with Blood |
| Дата добавления в базу: | 01.09.2013 |
| Дата актуализации: | 05.05.2017 |
| Дата введения: | 15.04.2003 |
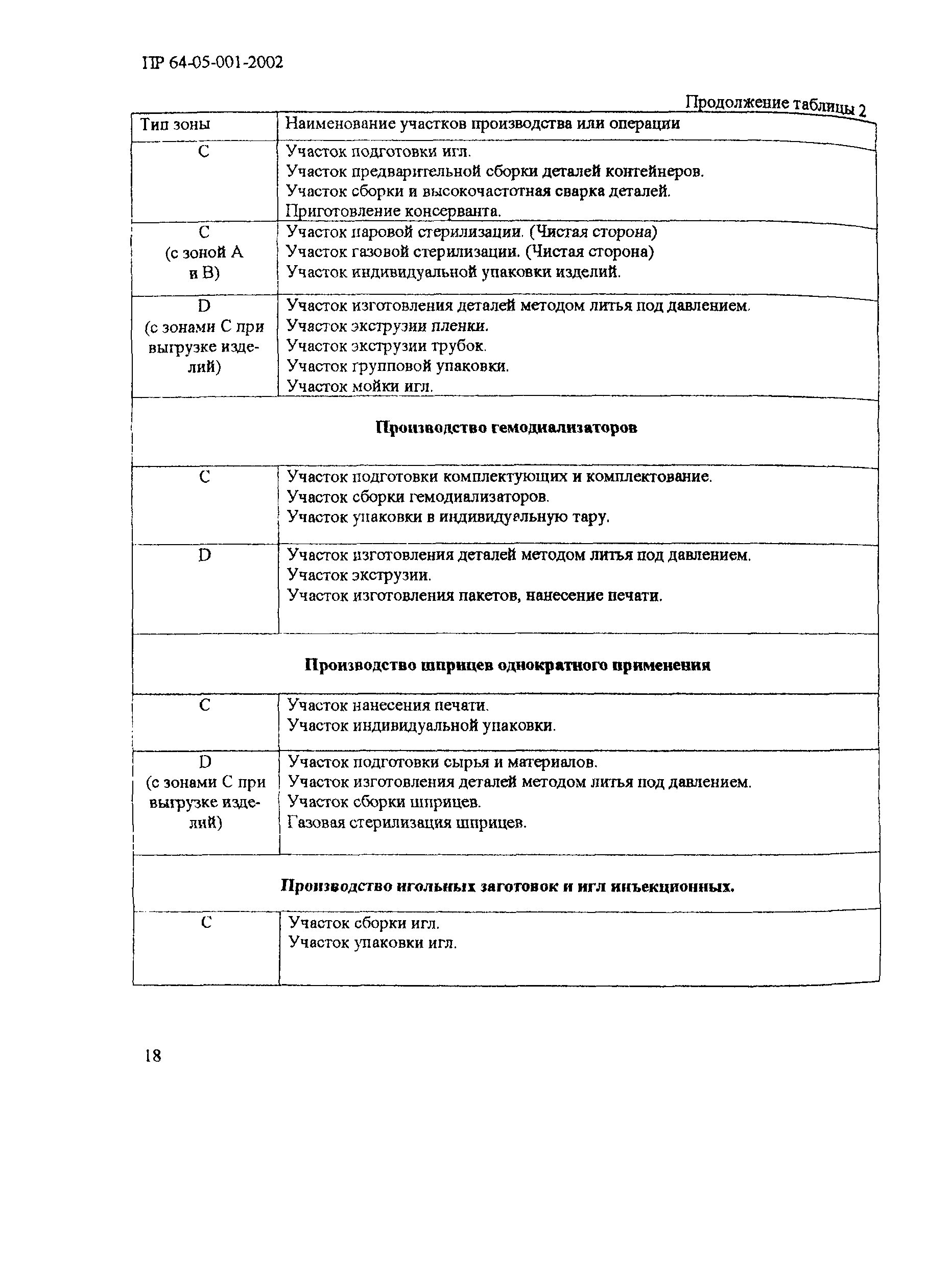
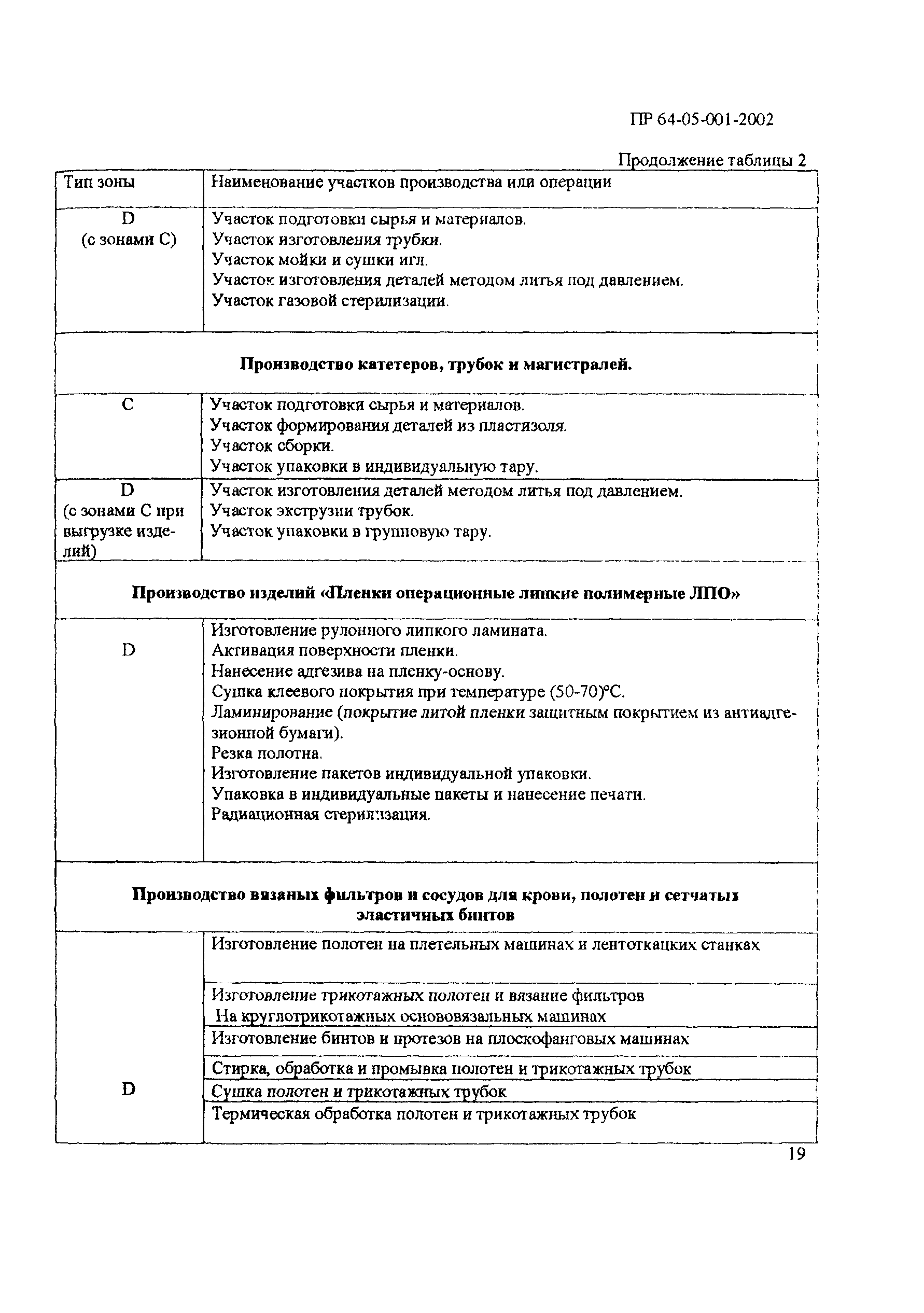
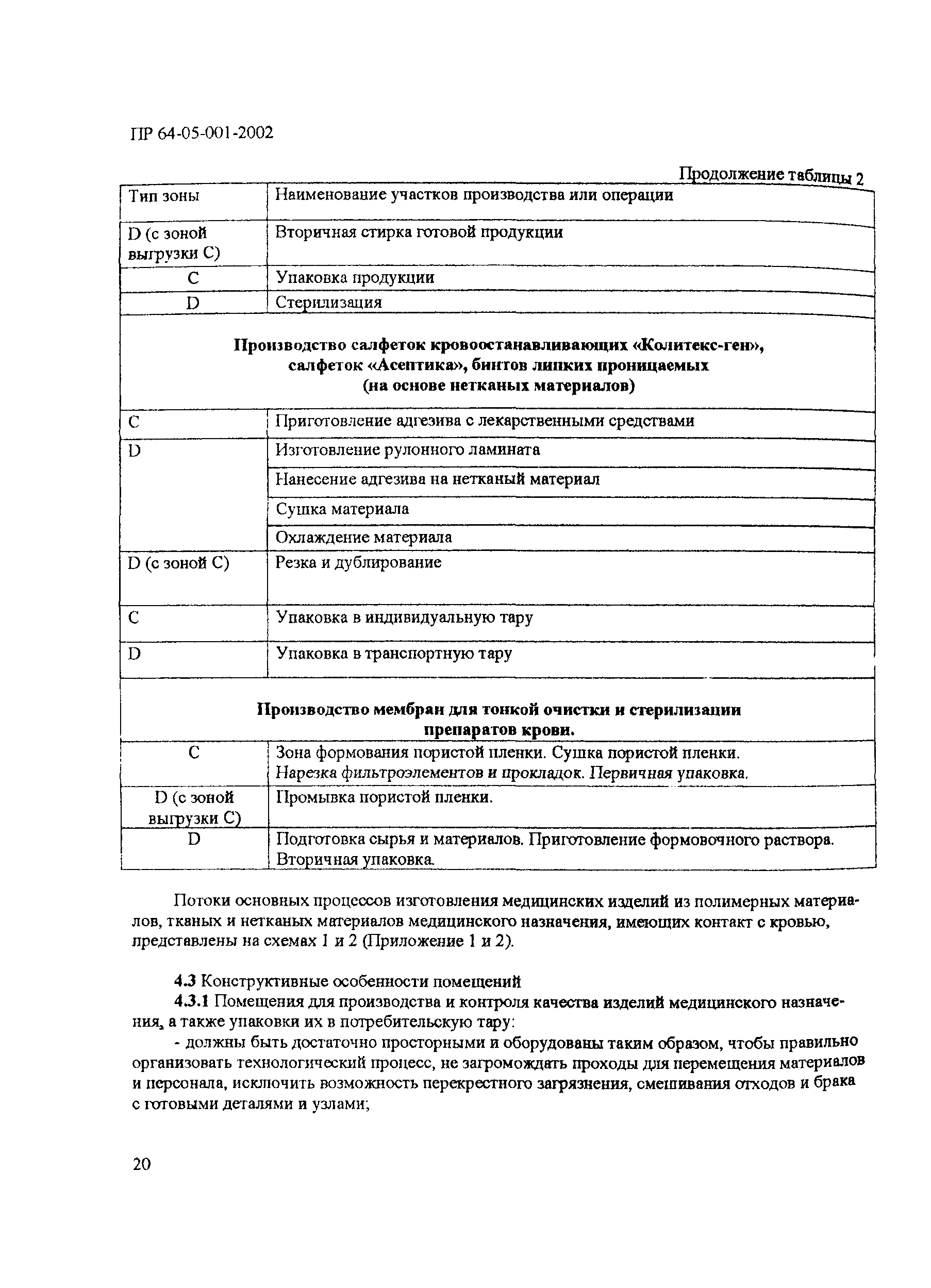
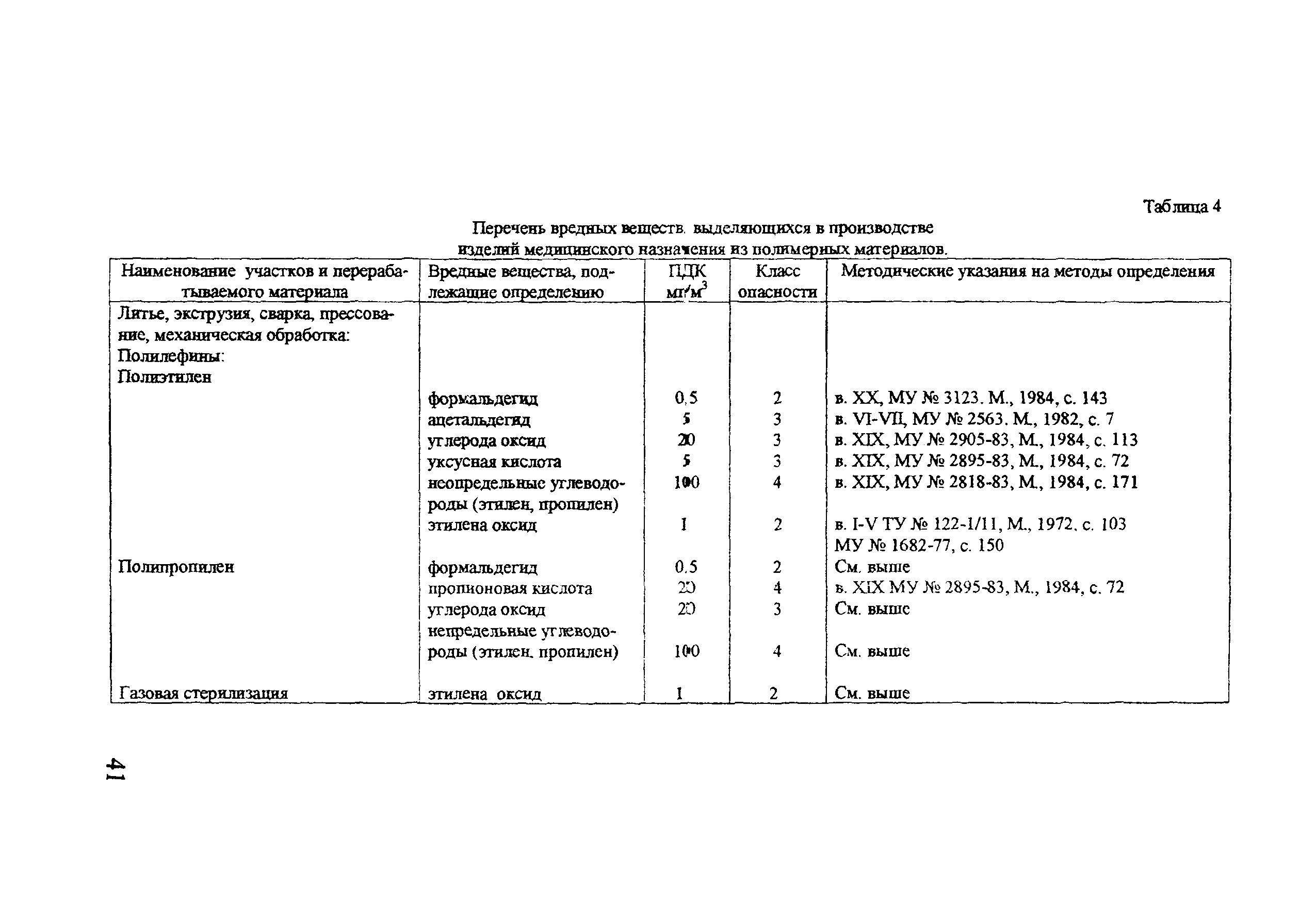
| Область применения: | Документ устанавливает правила организации и контроля чистых производств полимерных изделий, тканых и нетканых материалов медицинского назначения, контактирующих с кровью. Правила распространяются на производства, изготавливающие следующие изделия медицинской техники: - инфузионные, эксфузионные и трансфузионные устройства однократного применения; - контейнеры для заготовки, разделения, хранения и транспортирования крови и ее компонентов однократного применения; - контейнеры для розлива инфузионных растворов и кровезаменителей однократного применения; - различные магистрали и трубки из полимерных материалов к аппаратам искусственного кровообращения; - внутривенные катетеры однократного применения; - шприцы инъекционные однократного применения в комплекте с иглами инъекционными однократного применения; - фильтры вязаные и тканые для фильтрации крови и кровезаменителей; - искусственные вязаные сосуды для имплантации; - мембраны для тонкой очистки и стерилизации препаратов крови. |
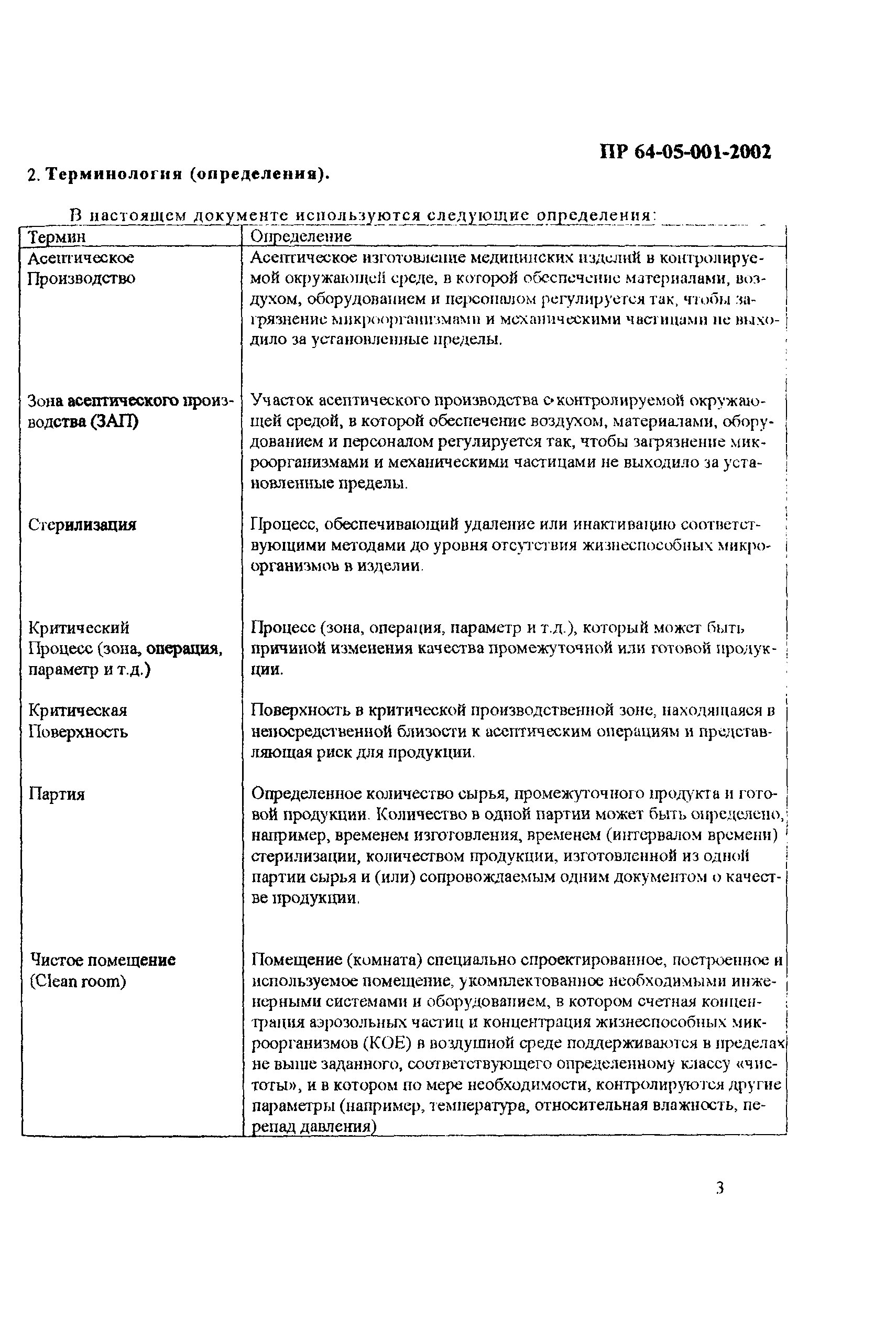
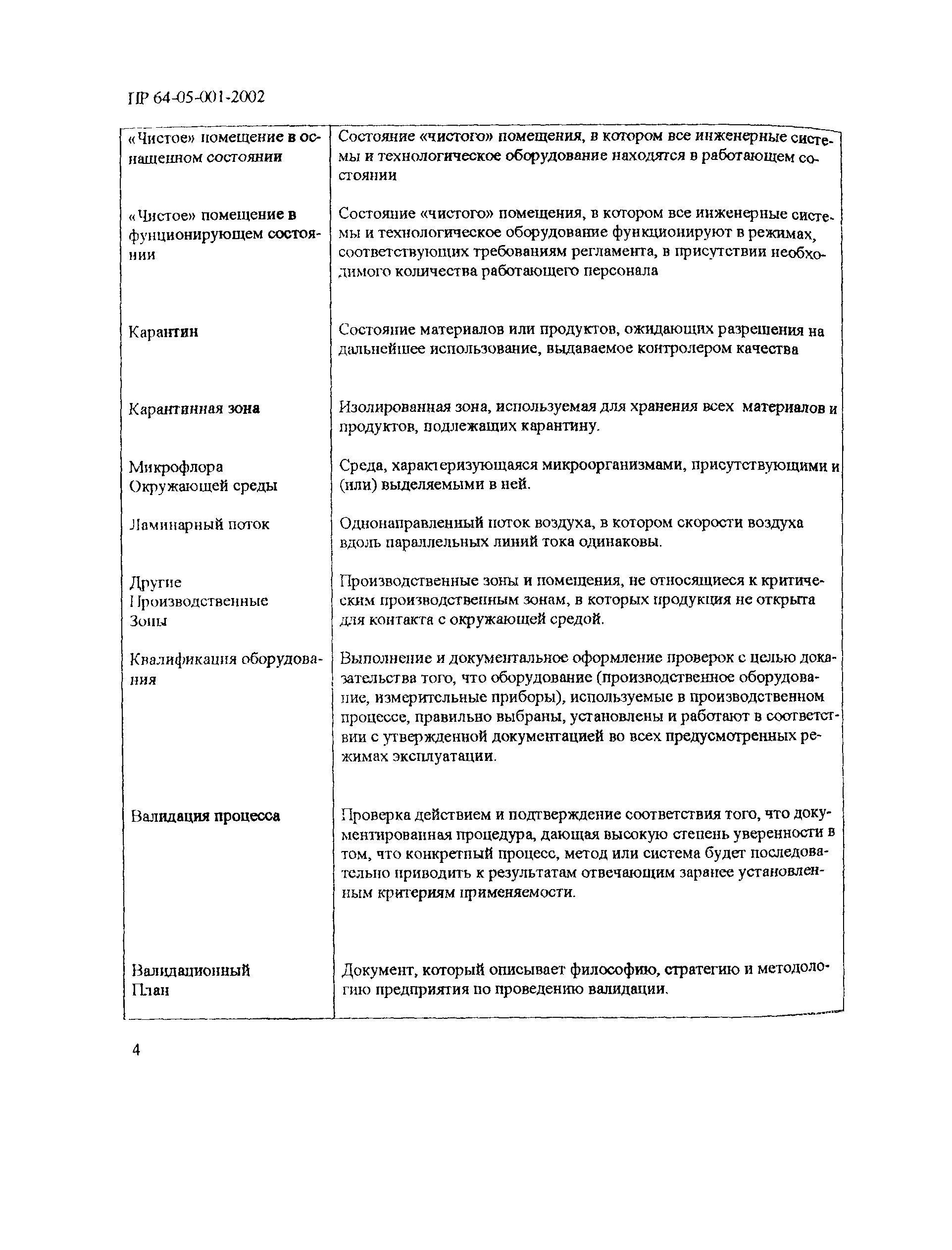
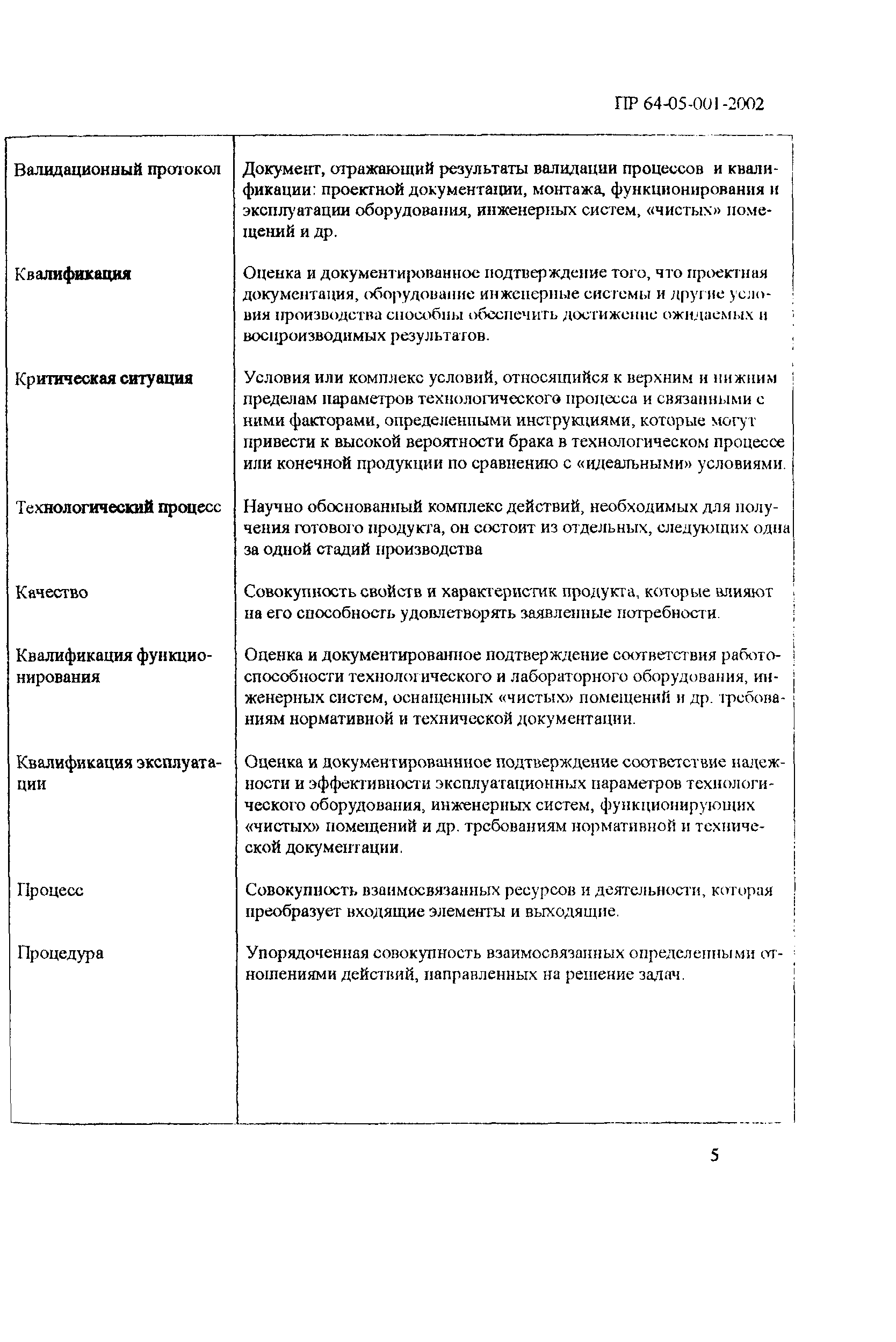
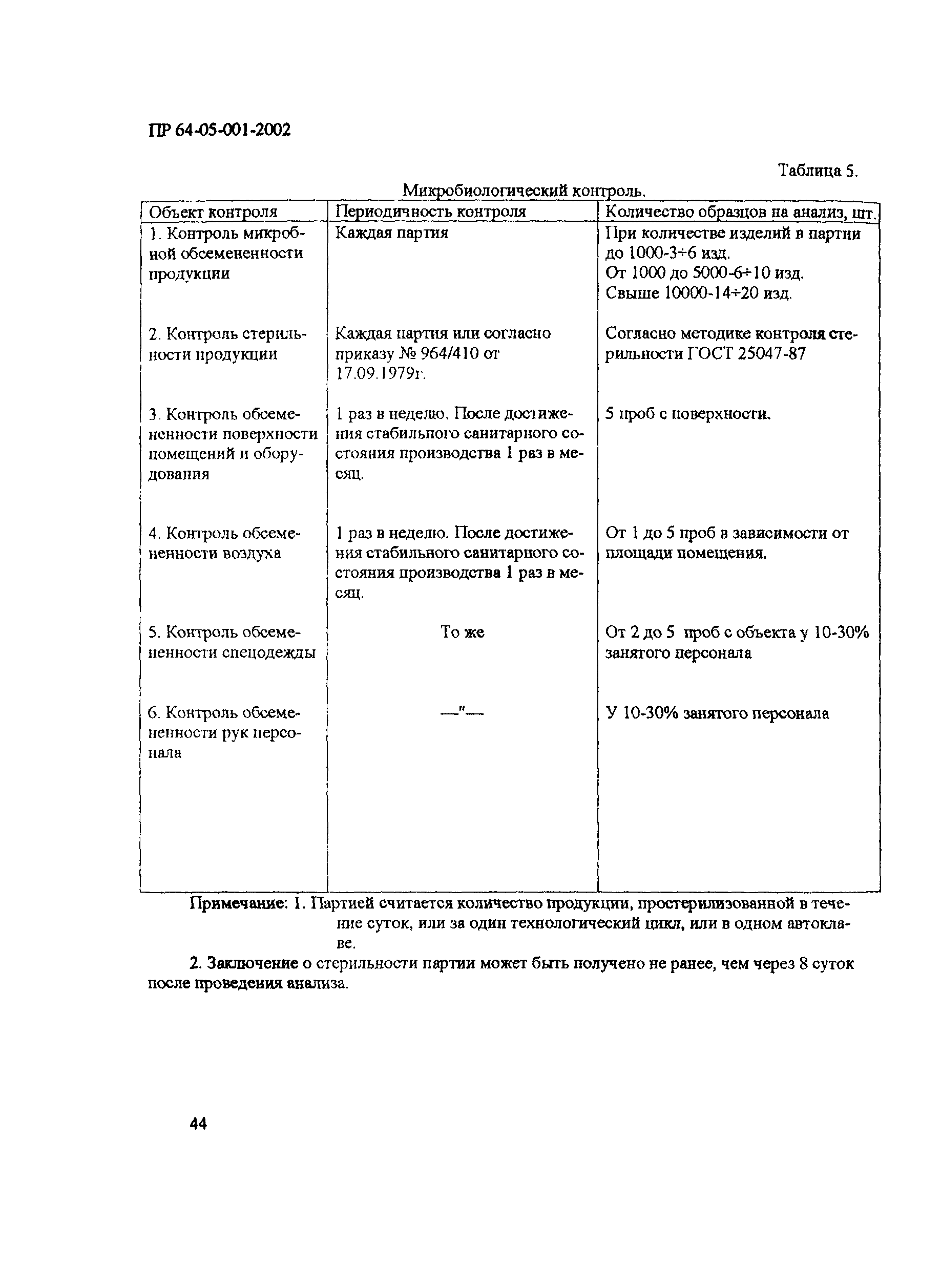
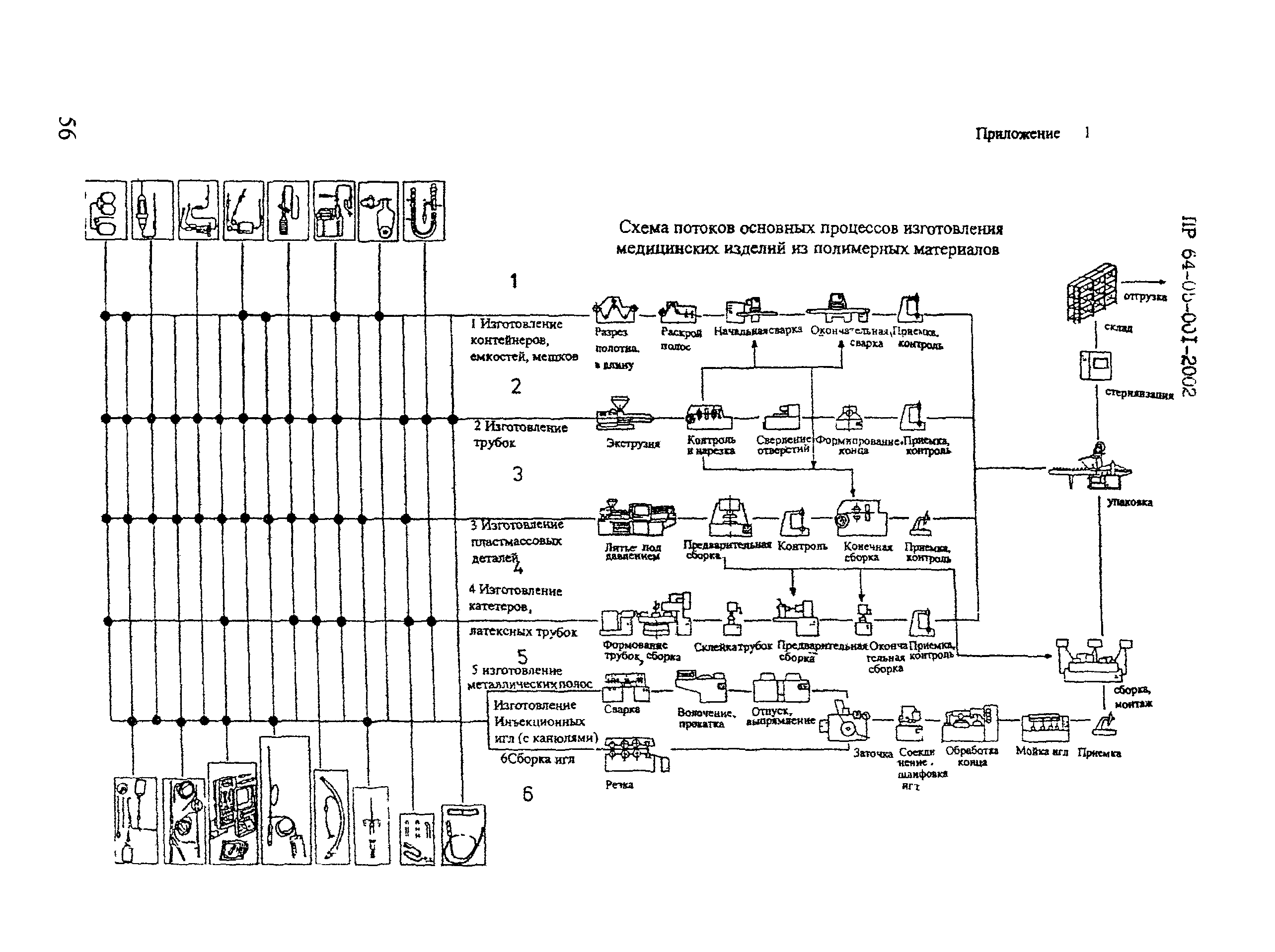
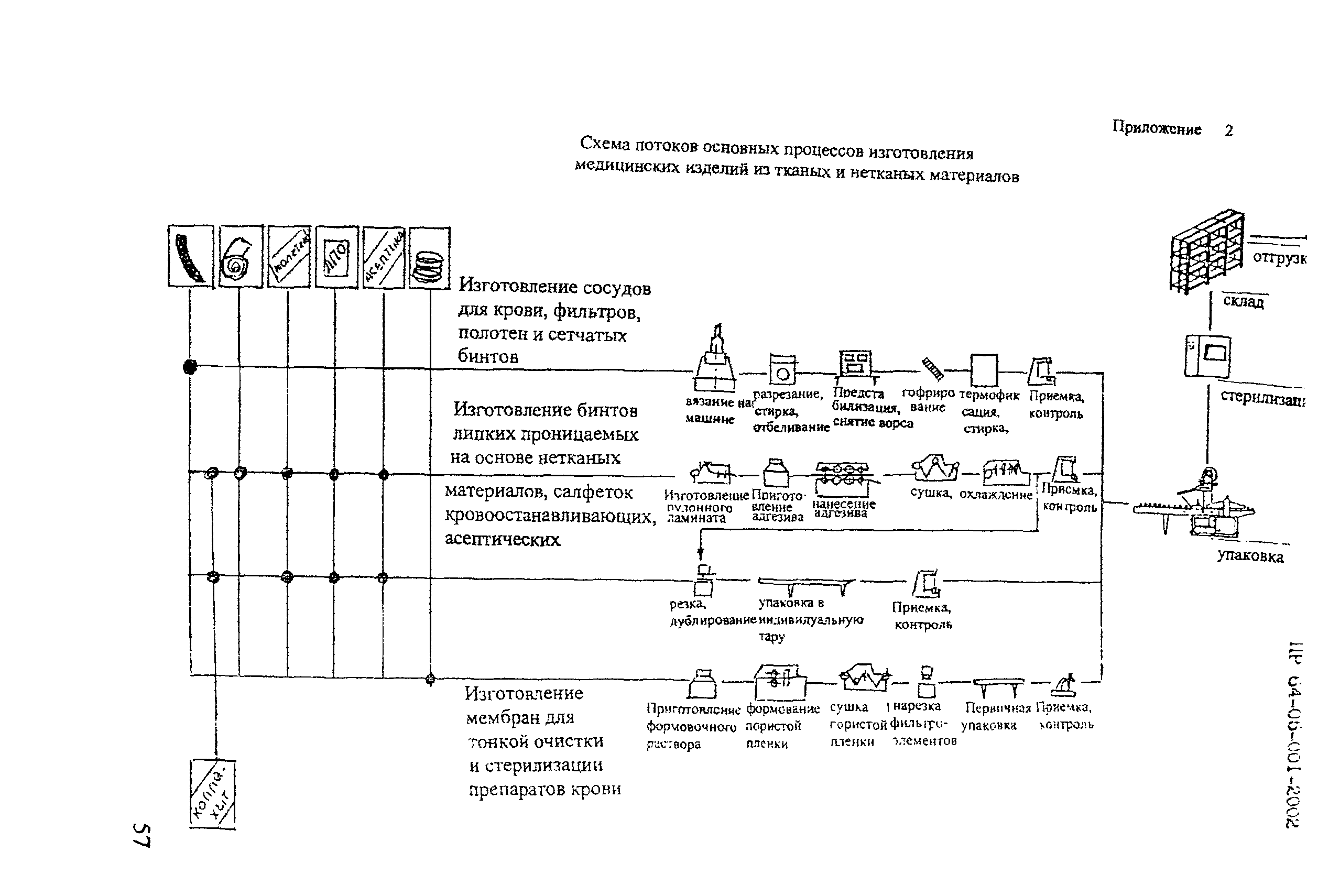
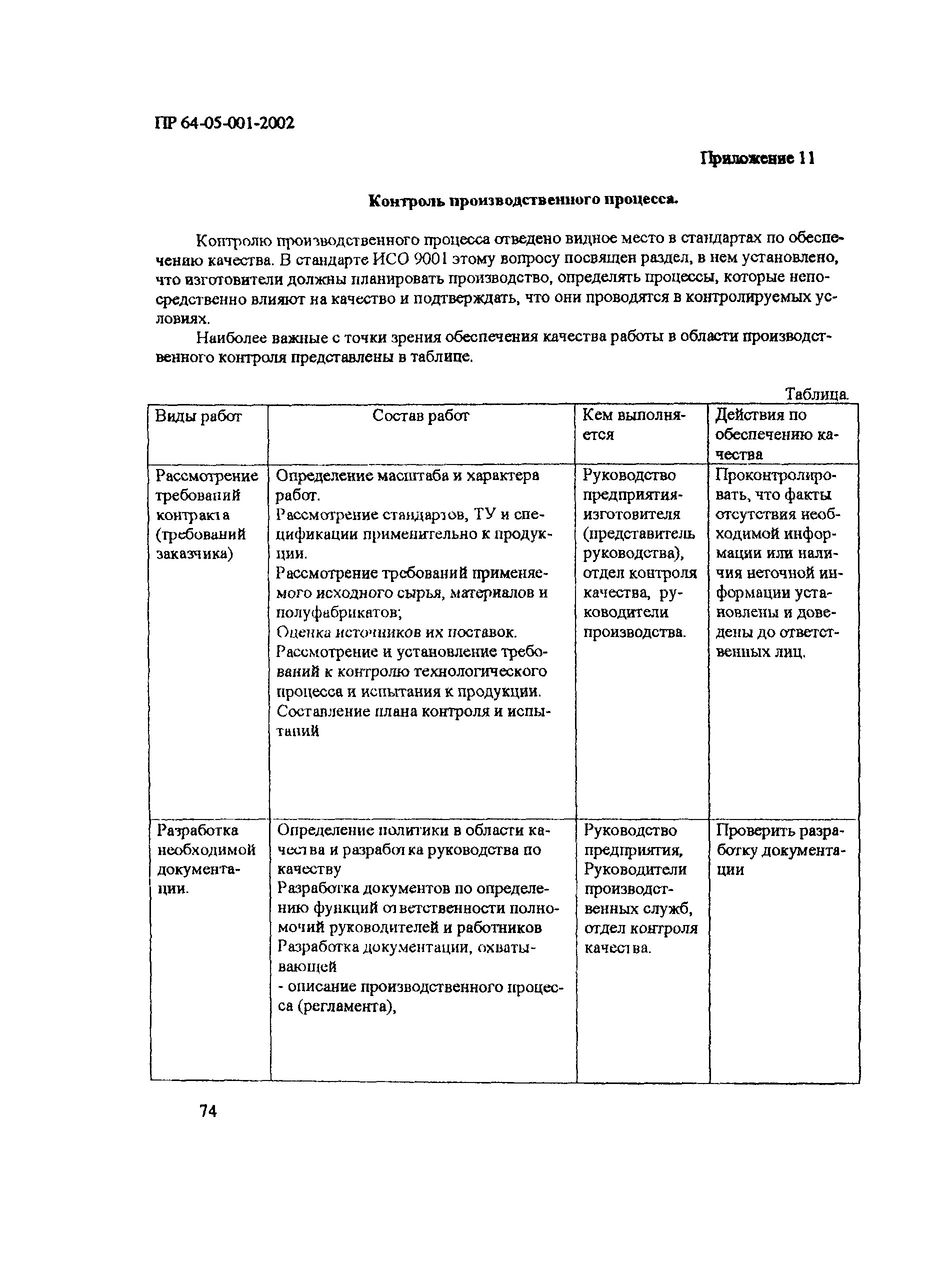
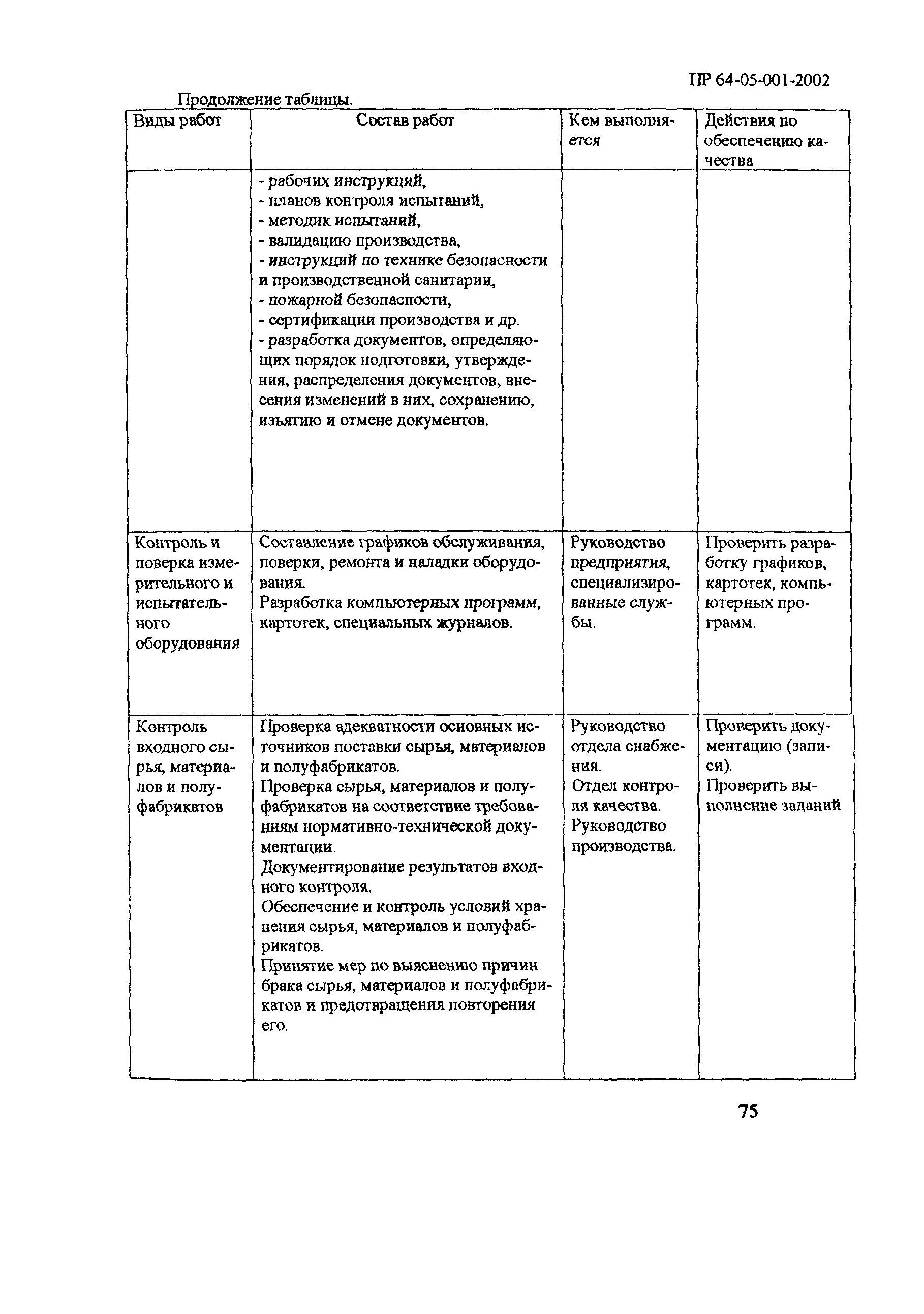
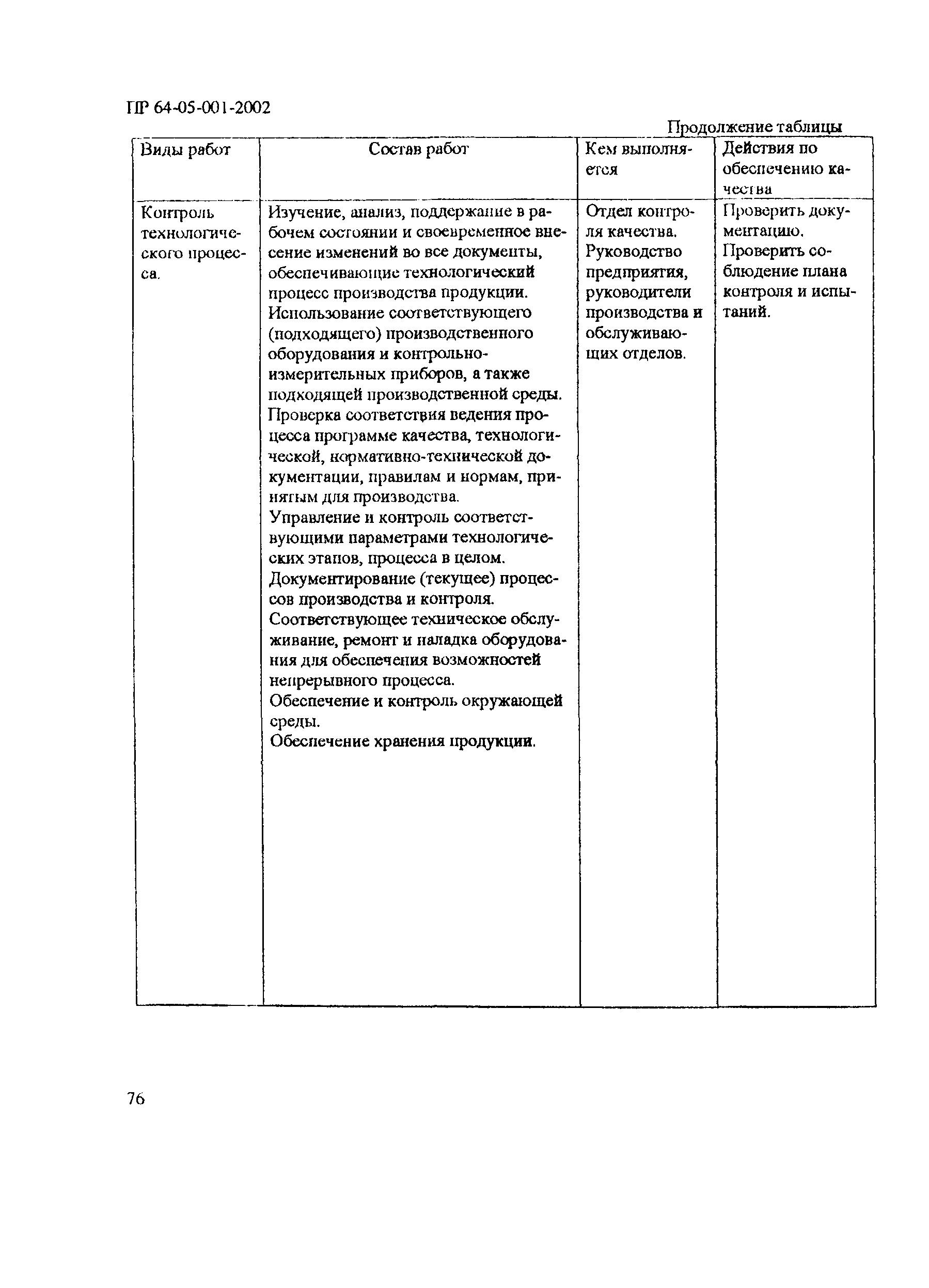
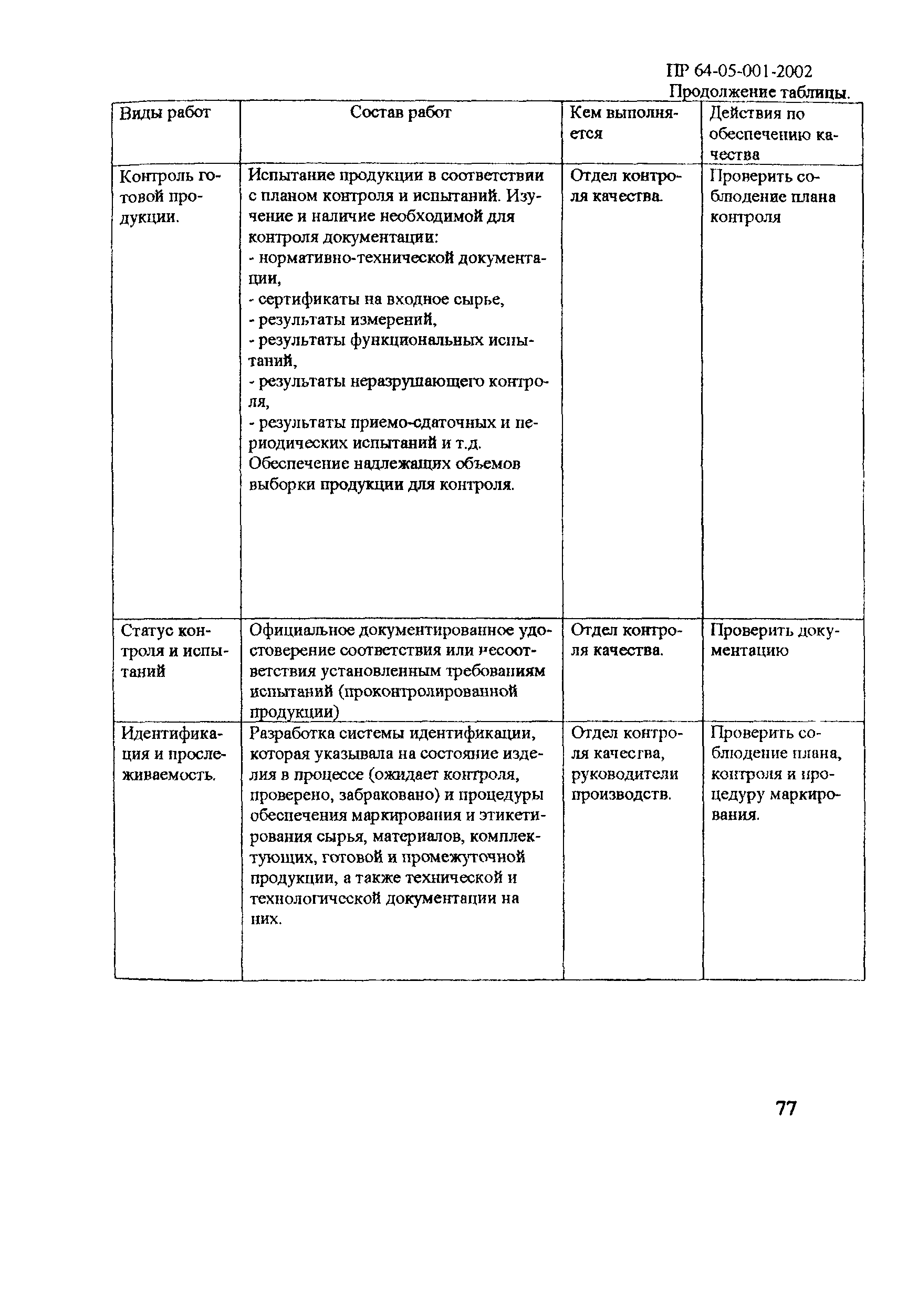
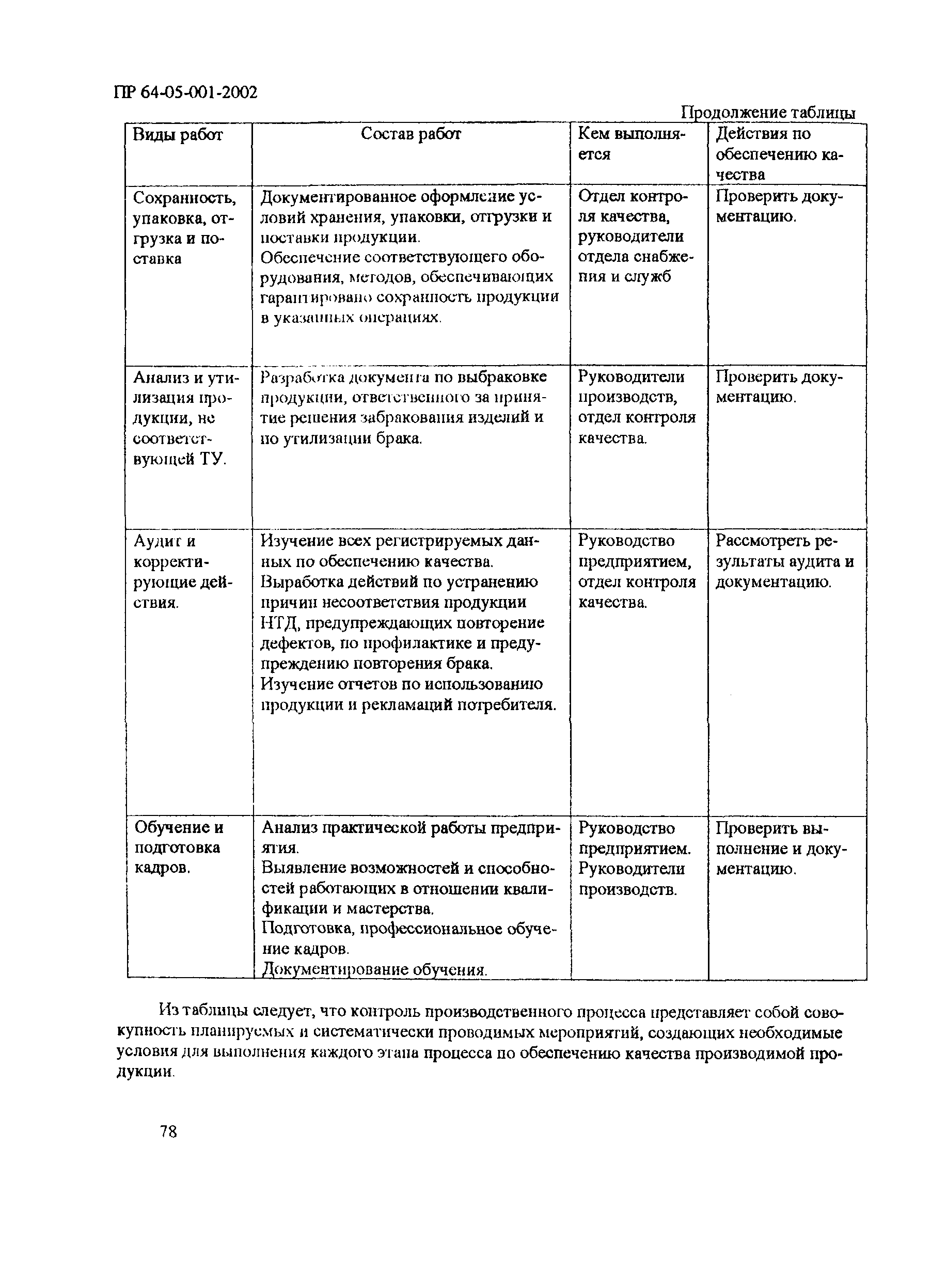
| Оглавление: | 1 Общие положения 2 Терминология (определения) 3 Персонал 3.1 Общие положения 3.2 Руководящий персонал 3.3 Обучение персонала 3.4 Условия работы в чистых помещениях, защитная одежда персонала, гигиена персонала 4 Здания и рабочие помещения 4.1 Общие положения. Требования к генплану и окружающей территории. Классификация помещений 4.2 Классификация помещений 4.3 Конструктивные особенности помещений 4.4 Отопление, вентиляция, кондиционирование 4.5 Освещение 4.6 Водоснабжение, канализация, сточные воды 4.7 Санитария 5 Оборудование 5.1 Общие положения 5.2 Конструкция оборудования 5.3 Размещение оборудования 5.4 Подготовка к работе и эксплуатации оборудования 6 Процесс производства 6.1 Общие положения 6.2 Исходное сырье 6.3 Технологический процесс производства. Контроль производства 6.4 Хранение 6.5 Процесс этикетирования 6.6 Упаковка и маркировка 6.7 Маркировка стерильной продукции 6.8 Стерилизация изделий 6.9 Отходы 6.10 Контроль и регистрация производственных процессов 6.11 Контроль готовой продукции 6.12 Контроль производственной и окружающей среды 6.13 Контроль чистых производственных помещений 7 Документация 8 Валидация 9 Сбор информации о качестве изделий, их эксплуатации. Рекламации и отзыв продукции с рынка 10 Самсоинспекция, самооценка деятельности предприятия Приложение 1 Схема потоков основных процессов изготовления медицинских изделий из полимерных материалов Приложение 2 Схема потока основных процессов изготовления медицинских изделий из тканых и нетканых материалов Приложение 3 Методика определения механических частиц в воздухе помещений производств изделий медицинского назначения из полимерных материалов Приложение 4 Методика определения инициальной контаминации продукции, стерилизуемой радиационным способом Приложение 5 Методика определения радиорезистентных микроорганизмов на предприятиях медицинской промышленности, выпускающих радиационно стерилизуемую продукцию Приложение 6 Порядок обработки дизинфекции помещений (объем работ ежемесячного санитарного дня) Приложение 7 Порядок обработки и дезинфекции вентсистемы Приложение 8 Контроль микробной обсемененности поверхностей оборудования и помещений Приложение 9 Контроль микробной обсемененности рук персонала Приложение 10 Принципы менеджмента качества Приложение 11 Контроль производственного процесса Приложение 12 Идентификация и прослеживаемость продукции на предприятии |
| Разработан: | ГУП Государственный научно-исследовательский институт медицинских полимеров |
| Утверждён: | 15.04.2003 Министерство промышленности, науки и технологий Российской Федерации (Russian Federation Ministry of Industry, Science, and Technology Р-19) |
| Расположен в: | |
| Нормативные ссылки: |
|
















































































© 2013 Ёшкин Кот :-) Карта сайта
 ГОСТ 12.0.004-90 «Система стандартов безопасности труда. Организация обучения безопасности труда. Общие положения»
ГОСТ 12.0.004-90 «Система стандартов безопасности труда. Организация обучения безопасности труда. Общие положения»