| Обозначение: |  ГОСТ Р 52770-2016 ГОСТ Р 52770-2016 |
| Обозначение англ: |  GOST R 52770-2016 GOST R 52770-2016 |
| Статус: | принят |
| Название рус.: | Изделия медицинские. Требования безопасности. Методы санитарно-химических и токсикологических испытаний |
| Название англ.: | Medical devices. Safety requirements. Methods of sanitation-chemical and toxicological tests |
| Дата добавления в базу: | 01.02.2017 |
| Дата актуализации: | 05.05.2017 |
| Дата введения: | 31.10.2016 |
| Дата окончания срока действия: | 01.10.2017 |
| Область применения: | Стандарт распространяется на МИ и устанавливает общий порядок проведения санитарно-химических и токсикологических испытаний (исследований) с целью обеспечения их безопасного применения при использовании в соответствии с назначением.
Стандарт служит в качестве руководства для планирования испытаний (исследований) МИ по санитарно-химическим показателям, показателям биологического действия и микробиологическим показателям. |
| Оглавление: | 1 Область применения
2 Нормативные ссылки
3 Определения
4 Общие положения
5 Основные требования к санитарно-химическим и токсикологическим испытаниям (исследованиям)
5.1 Выбор образцов для испытания (исследования)
5.2 Приготовление экстрактов (вытяжек) из испытуемых (исследуемых) материалов
5.3 Санитарно-химические испытания (исследования)
5.4 Токсикологические испытания (исследования)
5.5 Микробиологические испытания (исследования)
6 Отчетность о результатах
7 Обозначение соответствия настоящему стандарту
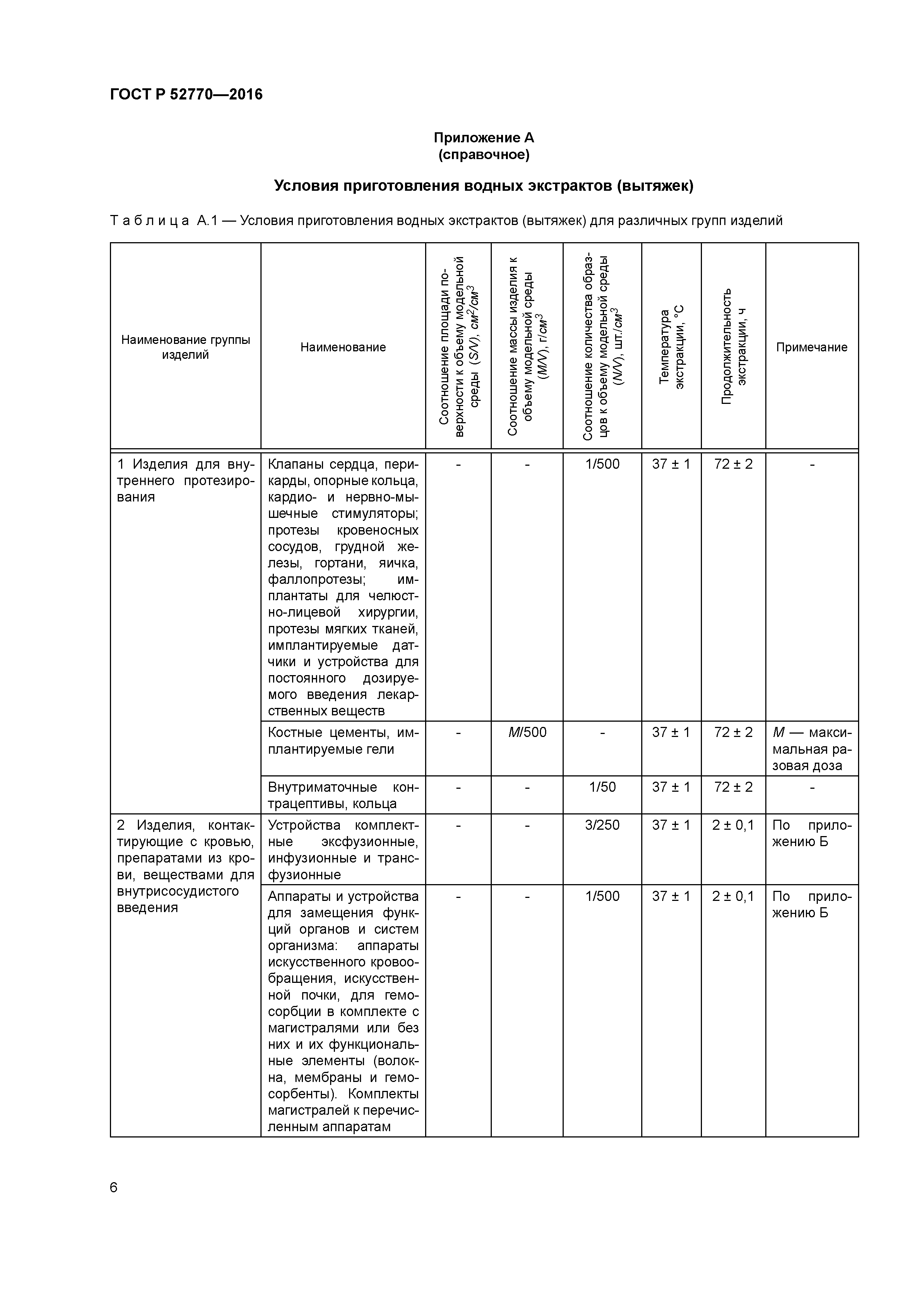
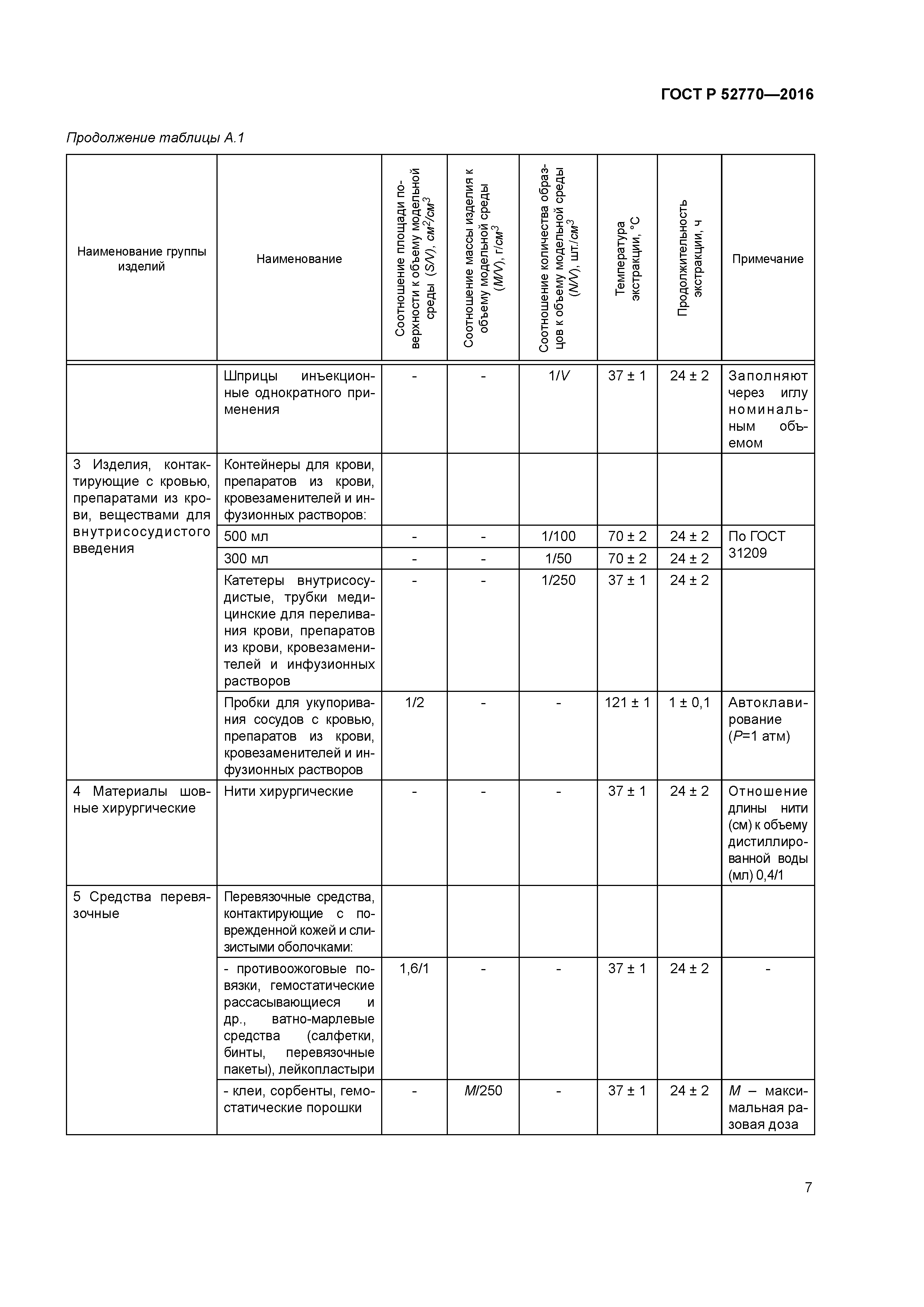
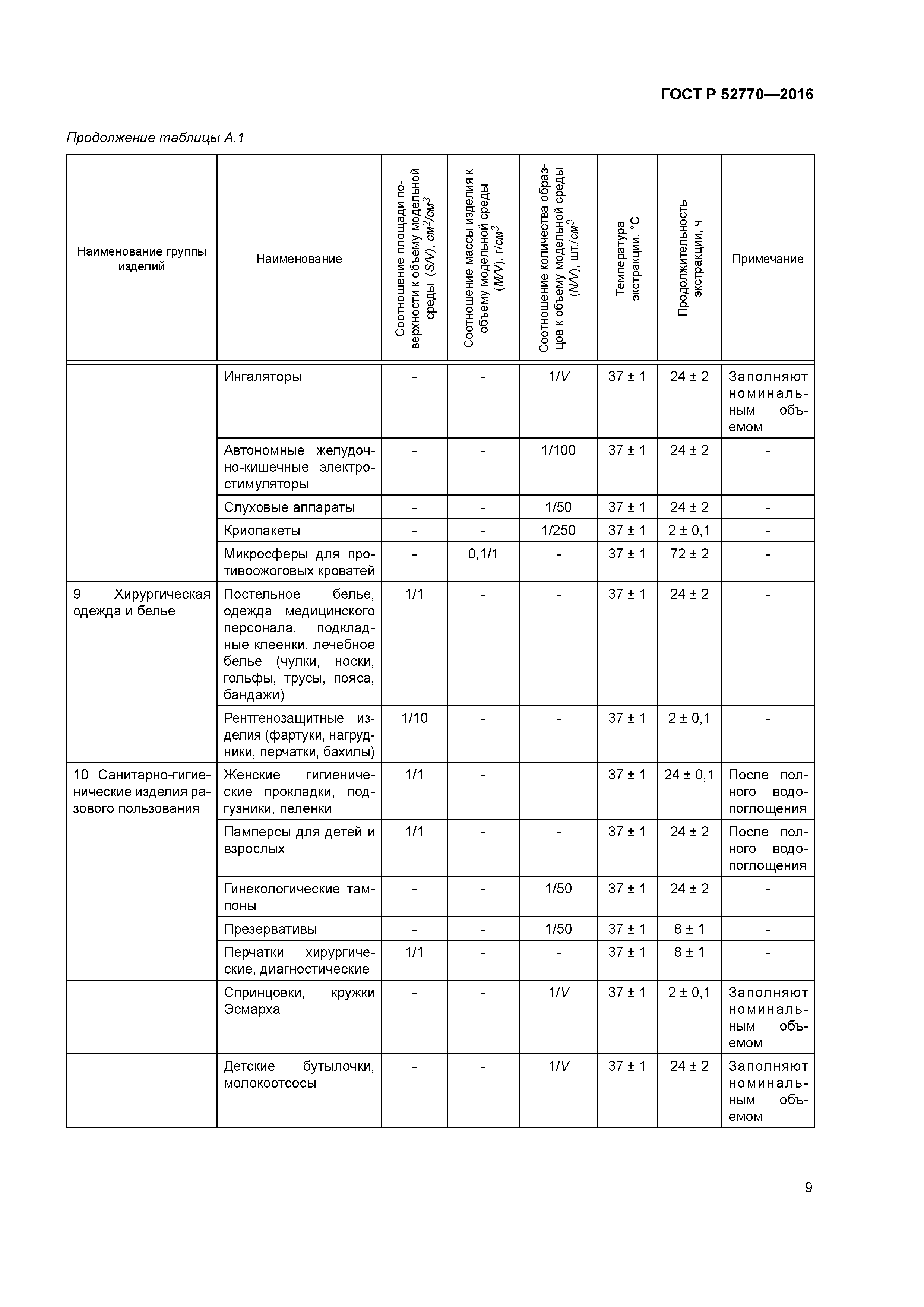
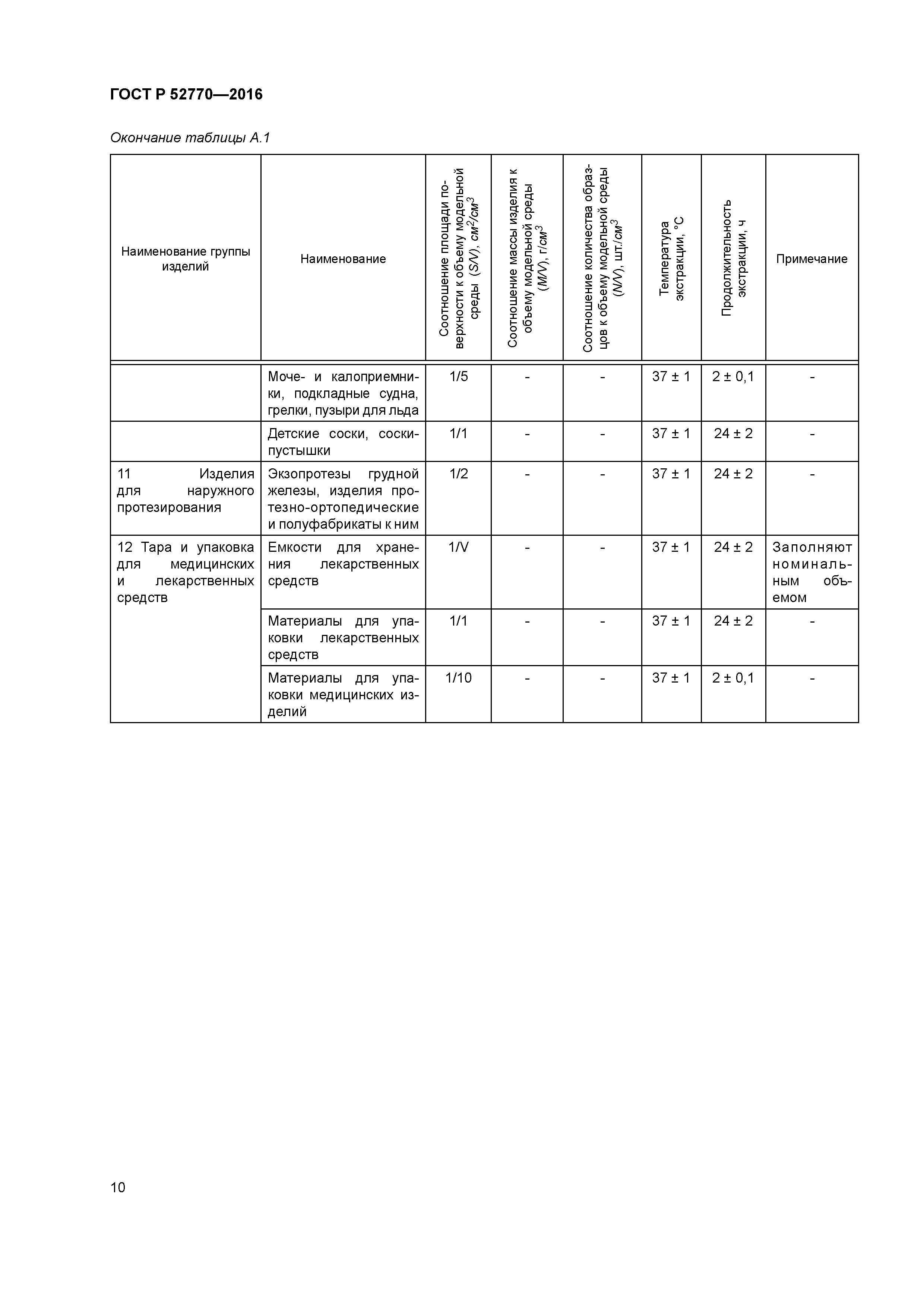
Приложение А (справочное) Условия приготовления водных экстрактов (вытяжек)
Приложение Б (справочное) Методика приготовления экстракта (вытяжки) с использованием стенда
Приложение В (справочное) Наименования и допустимые значения санитарно-химических показателей для медицинских изделий с учетом природы материала
Библиография |
| Разработан: | АНО ИМБИИТ
|
| Утверждён: | 31.10.2016 Федеральное агентство по техническому регулированию и метрологии (1535-ст)
|
| Издан: | Стандартинформ (2016 г. )
|
| Расположен в: |
|
| Заменяет собой: | |
| Нормативные ссылки: |    ГОСТ 6709-72 «Вода дистиллированная. Технические условия» ГОСТ 6709-72 «Вода дистиллированная. Технические условия»   ГН 2.3.3.972-00 «Предельно допустимые количества химических веществ, выделяющихся из материалов, контактирующих с пищевыми продуктами» ГН 2.3.3.972-00 «Предельно допустимые количества химических веществ, выделяющихся из материалов, контактирующих с пищевыми продуктами»   ГОСТ Р 52501-2005 «Вода для лабораторного анализа. Технические условия» ГОСТ Р 52501-2005 «Вода для лабораторного анализа. Технические условия»  ГОСТ Р ИСО 22442-2-2011 «Изделия медицинские, использующие ткани и их производные животного происхождения. Часть 2. Контроль отбора, сбора и обработки» ГОСТ Р ИСО 22442-2-2011 «Изделия медицинские, использующие ткани и их производные животного происхождения. Часть 2. Контроль отбора, сбора и обработки»  ГОСТ Р ИСО 22442-3-2011 «Изделия медицинские, использующие ткани и их производные животного происхождения. Часть 3. Валидация уничтожения и/или дезактивации вирусов и агентов инфекционной губчатой энцефалопатии» ГОСТ Р ИСО 22442-3-2011 «Изделия медицинские, использующие ткани и их производные животного происхождения. Часть 3. Валидация уничтожения и/или дезактивации вирусов и агентов инфекционной губчатой энцефалопатии»   ГОСТ ИСО/МЭК 17025-2009 «Общие требования к компетентности испытательных и калибровочных лабораторий» ГОСТ ИСО/МЭК 17025-2009 «Общие требования к компетентности испытательных и калибровочных лабораторий»  ГОСТ Р ИСО 22442-1-2011 «Изделия медицинские, использующие ткани и их производные животного происхождения. Часть 1. Менеджмент риска» ГОСТ Р ИСО 22442-1-2011 «Изделия медицинские, использующие ткани и их производные животного происхождения. Часть 1. Менеджмент риска»  ГОСТ ISO 10993-10-2011 «Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 10. Исследования раздражающего и сенсибилизирующего действия» ГОСТ ISO 10993-10-2011 «Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 10. Исследования раздражающего и сенсибилизирующего действия»  ГОСТ ISO 14971-2011 «Изделия медицинские. Применение менеджмента риска к медицинским изделиям» ГОСТ ISO 14971-2011 «Изделия медицинские. Применение менеджмента риска к медицинским изделиям»  ГОСТ ISO 10993-6-2011 «Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 6. Исследования местного действия после имплантации» ГОСТ ISO 10993-6-2011 «Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 6. Исследования местного действия после имплантации»  ГОСТ ISO 10993-7-2011 «Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 7. Остаточное содержание этиленоксида после стерилизации» ГОСТ ISO 10993-7-2011 «Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 7. Остаточное содержание этиленоксида после стерилизации»  ГОСТ ISO 10993-14-2011 «Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 14. Идентификация и количественное определение продуктов деградации изделий из керамики» ГОСТ ISO 10993-14-2011 «Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 14. Идентификация и количественное определение продуктов деградации изделий из керамики»  ГОСТ ISO 10993-4-2011 «Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 4. Исследования изделий, взаимодействующих с кровью» ГОСТ ISO 10993-4-2011 «Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 4. Исследования изделий, взаимодействующих с кровью»  ГОСТ ISO 10993-5-2011 «Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 5. Исследования на цитотоксичность: методы in vitro» ГОСТ ISO 10993-5-2011 «Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 5. Исследования на цитотоксичность: методы in vitro»  ГОСТ ISO 10993-9-2011 «Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 9. Основные принципы идентификации и количественного определения потенциальных продуктов деградации» ГОСТ ISO 10993-9-2011 «Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 9. Основные принципы идентификации и количественного определения потенциальных продуктов деградации»  ГОСТ ISO 10993-15-2011 «Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 15. Идентификация и количественное определение продуктов деградации изделий из металлов и сплавов» ГОСТ ISO 10993-15-2011 «Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 15. Идентификация и количественное определение продуктов деградации изделий из металлов и сплавов»   ГОСТ 31814-2012 «Оценка соответствия. Общие правила отбора образцов для испытаний продукции при подтверждении соответствия» ГОСТ 31814-2012 «Оценка соответствия. Общие правила отбора образцов для испытаний продукции при подтверждении соответствия»  ГОСТ ISO 10993-1-2011 «Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 1. Оценка и исследования» ГОСТ ISO 10993-1-2011 «Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 1. Оценка и исследования»  ГОСТ ISO 10993-11-2011 «Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 11. Исследования общетоксического действия» ГОСТ ISO 10993-11-2011 «Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 11. Исследования общетоксического действия»  ГОСТ 31580.5-2012 «Имплантаты офтальмологические. Интраокулярные линзы. Часть 5. Биологическая совместимость» ГОСТ 31580.5-2012 «Имплантаты офтальмологические. Интраокулярные линзы. Часть 5. Биологическая совместимость»  ГОСТ 31209-2003 «Контейнеры для крови и ее компонентов. Требования химической и биологической безопасности и методы испытаний» ГОСТ 31209-2003 «Контейнеры для крови и ее компонентов. Требования химической и биологической безопасности и методы испытаний»  ГОСТ 31576-2012 «Оценка биологического действия медицинских стоматологических материалов и изделий. Классификация и приготовление проб» ГОСТ 31576-2012 «Оценка биологического действия медицинских стоматологических материалов и изделий. Классификация и приготовление проб»  ГОСТ ISO 10993-12-2015 «Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 12. Приготовление проб и контрольные образцы» ГОСТ ISO 10993-12-2015 «Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 12. Приготовление проб и контрольные образцы»  ГОСТ ISO 10993-13-2016 «Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 13. Идентификация и количественное определение продуктов деструкции полимерных медицинских изделий» ГОСТ ISO 10993-13-2016 «Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 13. Идентификация и количественное определение продуктов деструкции полимерных медицинских изделий»  ГОСТ ISO 10993-16-2016 «Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 16. Концепция токсикокинетических исследований продуктов разложения и выщелачиваемых веществ» ГОСТ ISO 10993-16-2016 «Изделия медицинские. Оценка биологического действия медицинских изделий. Часть 16. Концепция токсикокинетических исследований продуктов разложения и выщелачиваемых веществ»  ГОСТ 31214-2016 «Изделия медицинские. Требования к образцам и документации, представляемым на токсикологические, санитарно-химические исследования, испытания на стерильность и пирогенность» ГОСТ 31214-2016 «Изделия медицинские. Требования к образцам и документации, представляемым на токсикологические, санитарно-химические исследования, испытания на стерильность и пирогенность»
|

 ГОСТ Р 52770-2016
ГОСТ Р 52770-2016






















 ГОСТ Р 52770-2007 «Изделия медицинские. Требования безопасности. Методы санитарно-химических и токсикологических испытаний»
ГОСТ Р 52770-2007 «Изделия медицинские. Требования безопасности. Методы санитарно-химических и токсикологических испытаний»